弥漫性中线胶质瘤迎来首款靶向新药
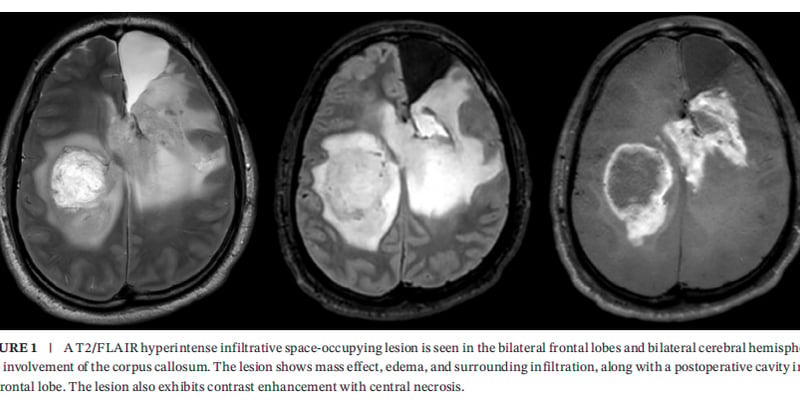
近日,美国食品药品监督管理局(FDA)授予了多达维普酮(dordaviprone,商品名:Modeyso)加速批准,用于治疗既往接受过治疗后病情发生进展、携带H3K27M突变的成人和1岁及以上儿童弥漫性中线胶质瘤(Diffuse Midline Glioma)患者。这一批准标志着该领域的一个重要里程碑,因为多达维普酮是首款获FDA批准用于治疗H3K27M突变弥漫性中线胶质瘤的全身性疗法。
多达维普酮的临床疗效数据
此次批准主要基于一项包含50名复发性H3K27M突变弥漫性中线胶质瘤儿童及成人患者的综合疗效分析。这些数据来源于5项在美国进行的开放标签、非随机临床试验。所有患者在接受多达维普酮单药治疗前,均根据RANO-HGG标准被评估为疾病进展且存在可测量病灶。
经独立盲法中心审查评估,关键疗效结果显示:
- 总缓解率(ORR):达到 22%(95% CI, 12%-36%)。
- 中位缓解持续时间(DOR):为 10.3个月(95% CI, 7.3-15.2)。
在11名获得客观缓解的患者中,73%的患者缓解持续时间超过6个月,27%的患者缓解持续时间超过12个月。这些数据证明了多达维普酮在控制肿瘤方面的显著潜力。
除了肿瘤缩小,还有哪些临床获益?
除了直接的肿瘤缓解效果,研究还观察到多达维普酮为患者带来的其他重要临床获益。在可评估的患者中:
- 激素减量:46.7%的患者(7/15)实现了皮质类固醇剂量减少50%或以上,这有助于减轻激素带来的副作用。
- 功能状态改善:20.6%的患者(6/34)的卡氏或Lansky体能状态评分得到改善,意味着生活质量的提升。
中位起效时间为8.3个月,这提示患者和医生需要一定的耐心来等待药物发挥最佳效果。
多达维普酮的安全性与副作用
在安全性方面,多达维普酮总体耐受性良好。研究中,20%的患者经历了3级治疗相关的不良事件,其中最常见的是疲劳(10%)。值得注意的是,研究中未报告4级治疗相关不良事件,也无患者因此停药或死亡。
尽管如此,患者在用药前仍需了解其潜在风险。多达维普酮的处方信息中包含了关于QTc间期延长、超敏反应和胚胎-胎儿毒性的警告与注意事项。如果您对多达维普酮的治疗方案或副作用管理有任何疑问,可以咨询MedFind的AI问诊服务,获取专业的解答。
专家观点与未来展望
加州大学洛杉矶分校的Timothy Cloughesy博士强调:“弥漫性中线胶质瘤是一种极难治疗的肿瘤。拥有一种有效的治疗选择对我们领域来说是一个巨大的胜利。”他指出,医生们需要意识到这是一种新的治疗选择,它不仅能控制肿瘤,还可能通过缩小肿瘤来改善患者的神经功能。
多达维普酮的成功获批,为预后不佳的原发性脑肿瘤患者带来了新的希望。MedFind致力于为国内患者链接全球最新的药物资源。如果您需要了解多达维普酮(Modeyso)的代购价格、购买渠道等信息,请访问我们的药品信息页面或联系我们的客服获取帮助。