癌症治疗领域正经历着前所未有的变革,免疫疗法,尤其是以PD-1/PD-L1抑制剂为代表的靶向药,为无数患者带来了新的希望。然而,面对复杂的肿瘤微环境,如何进一步提升治疗响应率仍是医学界面临的挑战。近年来,研究人员将目光投向了微生物及其产物在免疫调节中的潜力,其中卡介苗(BCG)作为一种历史悠久的免疫增强剂,不仅是结核病的疫苗,更是膀胱癌的标准免疫治疗药物。尽管BCG在激活局部抗肿瘤免疫方面表现出色,但其如何系统性地影响全身免疫,特别是对造血干细胞(HSPCs)的长期作用机制,一直是个谜。
卡介苗(BCG)重编程造血干细胞的突破性发现
国际权威期刊《Cancer Cell》近期发表了一项突破性研究,题为“Microbial cancer immunotherapy reprograms hematopoiesis to enhance myeloid-driven antitumor immunity”。这项研究通过尖端技术,如单细胞RNA测序和ATAC测序,深入揭示了卡介苗(BCG)如何通过系统性地重编程造血干细胞和祖细胞(HSPCs),从而显著增强髓系细胞驱动的抗肿瘤免疫反应。这一发现为理解BCG的深层作用机制提供了全新视角,也为开发更有效的抗癌药策略奠定了基础。

BCG对HSPCs的系统性影响与髓系细胞生成
研究团队首先证实,即使通过膀胱给药,卡介苗(BCG)也能对HSPCs产生系统性影响。对接受BCG治疗的膀胱癌患者和小鼠模型的HSPCs进行分析发现,BCG处理后的HSPCs在基因表达和表观遗传学层面发生了显著变化。这些变化包括干扰素γ(IFNγ)信号通路和抗原呈递相关基因的上调,表明BCG能够激活HSPCs的免疫功能。更重要的是,这些被重编程的HSPCs在体外表现出更强的髓系细胞生成能力,特别是中性粒细胞和单核细胞,这些都是抗肿瘤免疫的关键组成部分。
增强抗肿瘤免疫反应:T细胞激活与肿瘤抵抗
为了验证BCG重编程HSPCs的抗肿瘤潜力,研究人员构建了骨髓嵌合小鼠模型。结果令人鼓舞:移植了经BCG处理的HSPCs的小鼠,在接种肿瘤后表现出显著的肿瘤生长抑制,且这种抑制作用依赖于T细胞的参与。进一步的实验表明,这些重编程的HSPCs能够产生具有增强抗原呈递能力的髓系细胞(如树突状细胞),从而有效激活T细胞介导的免疫反应。此外,BCG处理的HSPCs还能生成对肿瘤微环境诱导的促肿瘤转化具有抵抗力的中性粒细胞,进一步巩固了其抗肿瘤免疫效果。
与PD-1抑制剂的协同效应:提升治疗效果
令人振奋的是,研究还发现卡介苗(BCG)重编程HSPCs能够与PD-1阻断疗法产生显著的协同作用。在小鼠模型中,接受BCG处理的HSPCs的小鼠在联合PD-1抑制剂治疗后,肿瘤生长抑制效果更为显著,生存率也得到明显提升。这表明,BCG不仅能通过重编程HSPCs增强髓系细胞介导的抗肿瘤免疫,还能与目前广泛使用的PD-1抑制剂等靶向药相结合,进一步提升整体治疗效果。对于寻求最新抗癌药和靶向药的患者而言,这种联合疗法无疑提供了新的希望。
展望与患者支持:获取前沿抗癌药与资讯
这项研究不仅深入揭示了卡介苗(BCG)作为一种抗癌药的全新作用机制,即通过系统性重编程造血干细胞来增强抗肿瘤免疫,更为开发新型免疫治疗策略提供了坚实的理论基础。未来的研究将进一步探索其分子机制,并将其应用于更多类型的癌症治疗。对于全球癌症患者而言,及时获取这些前沿的药物信息和诊疗指南至关重要。如果您正在寻找海外靶向药代购、抗癌药代购或仿制药的海外购药服务,或者需要专业的AI问诊服务来了解最新的治疗方案,MedFind致力于为您提供便捷、可靠的海外靶向药代购服务,并提供全面的抗癌资讯支持。
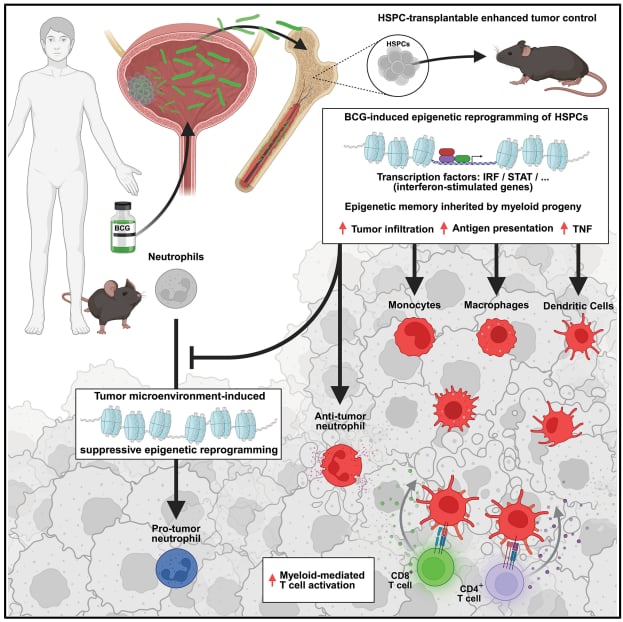
图 本研究模式图
原始出处:
Andrew W. Daman, et al. 2025. Microbial cancer immunotherapy reprograms hematopoiesis to enhance myeloid-driven antitumor immunity. Cancer Cell.