边缘区淋巴瘤预后到底好不好?复发后是不是就很危险?很多患者最关心的,不只是“能不能治”,而是“能稳定多久、复发风险多大、哪些指标提示病情更凶”。边缘区淋巴瘤是一组异质性很强的惰性B细胞淋巴瘤,不同亚型之间的自然病程、复发特点和风险分层工具差异很大。真正有用的判断,不是只看一个“惰性”标签,而是要结合分型、实验室指标、影像学、是否早期进展以及是否存在组织学转化风险综合评估。
边缘区淋巴瘤为什么差异这么大
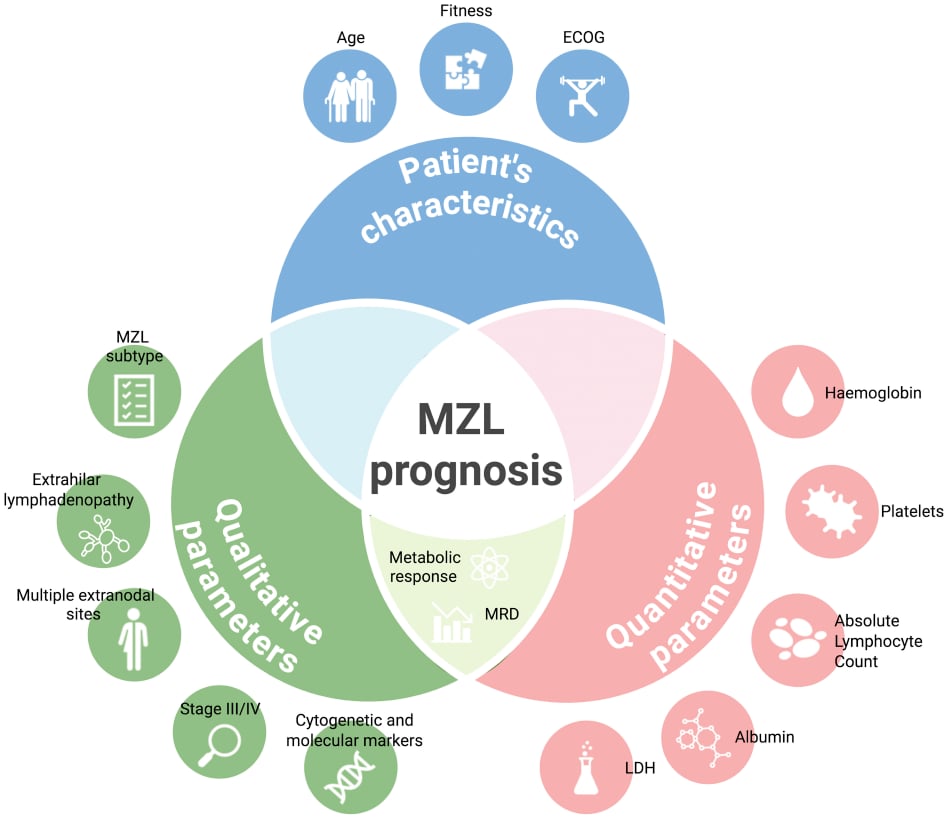
边缘区淋巴瘤(MZL)约占全部非霍奇金淋巴瘤的7%–8%,是常见的惰性B细胞淋巴瘤之一。它并不是单一疾病,而是包括三大主要亚型。
- 结外边缘区淋巴瘤:也常被称为MALT淋巴瘤,常见于胃、眼附属器、肺、唾液腺、甲状腺等黏膜相关部位。
- 脾边缘区淋巴瘤:以脾脏、骨髓、外周血受累更常见。
- 淋巴结边缘区淋巴瘤:主要表现为淋巴结受累。
这类疾病常与长期慢性抗原刺激相关,比如感染因素或自身免疫性疾病。临床上常见相关病原体包括幽门螺杆菌、丙型肝炎病毒、鹦鹉热衣原体等。也正因病因背景、原发部位和生物学行为不同,同样叫“边缘区淋巴瘤”,患者之间的病程可能非常不一样。
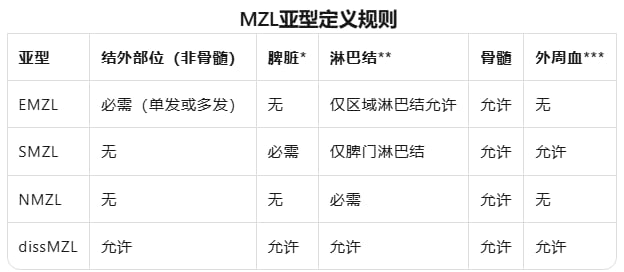
边缘区淋巴瘤并非单一疾病,结外型、脾型和淋巴结型在受累部位和病程上差异明显。
总体预后好,是不是就不用担心
很多资料会提到,边缘区淋巴瘤总体中位生存期可超过10年。这说明它整体属于相对进展较慢的淋巴瘤,但这并不等于“风险都低”。
需要特别理解三点。
- “惰性”不等于“不复发”。很多患者初治后可获得较长缓解,但后续仍可能反复复发。
- 不同亚型差异明显。早期胃MALT淋巴瘤预后相对较好,但并不是所有MZL都如此。
- 少数患者会出现生物学行为改变,比如早期进展或组织学转化,这类情况会显著影响后续生存。
从临床管理角度看,边缘区淋巴瘤真正要防的,不只是“有没有病”,而是“病会不会变快、会不会提早复发、会不会转化”。
复发率和生存期该怎么理解
边缘区淋巴瘤患者最容易被一句“总体预后不错”误导。更有参考价值的,是按亚型看复发和生存。
| 指标 | 临床信息 | 解读重点 |
|---|---|---|
| 总体生存 | 中位生存期超过10年 | 整体病程较长,但并非所有亚型都同样温和 |
| 结外型复发 | 约50%–60%患者复发,中位复发时间约5年 | 即使初治效果不错,长期随访仍非常重要 |
| 脾型病程 | 约1/3患者病程侵袭性较强,中位生存约4年 | 提示脾型内部异质性明显,不能简单按惰性病处理 |
| 组织学转化 | 发生率约5%–10%,年发生率约1% | 虽非高频,但一旦发生,治疗思路和风险都会改变 |
对于患者和家属来说,复发并不一定等于“无药可用”,但它提示后续管理不能只依赖经验判断,必须借助风险模型和动态监测工具来判断疾病节奏。
POD24为什么是危险信号
POD24指的是治疗开始后24个月内疾病进展。这个概念在惰性淋巴瘤中非常重要,因为它往往代表肿瘤生物学行为更差。
在边缘区淋巴瘤中,POD24被认为是明确的不良预后信号,而且与组织学转化风险高度相关。对于复发或难治患者,是否出现POD24,常常比单纯“复发了一次”更能说明问题。
| 分组 | 3年总生存率 | 临床意义 |
|---|---|---|
| 有POD24 | 53% | 提示疾病更具侵袭性,应尽快重新评估治疗路径 |
| 无POD24 | 88% | 总体生物学行为更平稳,后续治疗选择空间更大 |
如果患者在治疗后两年内就出现明显进展,通常需要重点排查以下问题:
- 是否存在初始分期低估
- 是否有组织学转化
- 是否需要重新活检
- 是否应从传统免疫化疗转向靶向治疗或临床试验方案
组织学转化后有多严重
所谓组织学转化,是指原本惰性的边缘区淋巴瘤转变为更具侵袭性的淋巴瘤类型。这类情况在MZL中不是最常见事件,但临床上必须高度重视。
已知转化发生率约为5%–10%,年发生率约1%。转化后5年总生存率约79%,10年总生存率约55%。这组数据说明,转化并不意味着立刻失去治疗机会,但确实意味着后续治疗复杂度明显上升。
目前已观察到的转化风险因素包括:
- 初始治疗后未达到完全缓解
- 乳酸脱氢酶升高
- 4个及以上淋巴结受累
- 多部位黏膜受累
- CD5表达
对患者而言,真正重要的不是机械记住这些名词,而是明白一件事:当复发变快、病灶变多、指标异常或症状明显加重时,不能只按“普通复发”处理,往往需要重新活检确认病理。
POD24和组织学转化是边缘区淋巴瘤预后评估中的关键警报信号。
结外型MALT淋巴瘤如何分层
结外边缘区淋巴瘤,也就是MALT淋巴瘤,是MZL中最常见的一类。它的风险评估常用MALT-IPI。
MALT-IPI看哪3项
MALT-IPI来源于IELSG19研究,包含3个参数,每项1分:
- 年龄>70岁
- Ann Arbor III–IV期
- LDH升高
| 风险分组 | 评分 | 5年EFS |
|---|---|---|
| 低危 | 0分 | 70% |
| 中危 | 1分 | 56% |
| 高危 | 2–3分 | 29% |
这里的核心不是“打分本身”,而是它帮助识别谁更可能早复发、谁需要更密集随访。
修订版MALT-IPI有什么提升
修订版MALT-IPI增加了多部位结外受累这一参数,因此对高危患者的识别更敏感。它把患者分为低危、低中危、中高危和高危四组,能更好识别真正危险的人群。
临床意义主要有两点:
- 高危组比例从17%扩大到26%,减少部分高风险患者被“归错类”
- 对识别POD24风险更有帮助
这意味着,对于看起来“并不重”的MALT淋巴瘤患者,如果存在多部位结外受累,也不能掉以轻心。
脾边缘区淋巴瘤看哪些指标
脾边缘区淋巴瘤的风险评估更强调血液学和全身状态指标。目前较常用的包括IIL评分、HPLL评分以及简化HPLL评分。
IIL评分适合看什么
IIL评分的参数包括:
- 血红蛋白<12 g/dL
- LDH升高
- 白蛋白<3.5 g/dL
| 评分系统 | 主要参数 | 5年生存结果 |
|---|---|---|
| IIL评分 | Hb、LDH、白蛋白 | 癌症特异生存:低危88%,中危73%,高危50% |
它反映的是患者是否已经存在较明显的肿瘤负荷、营养状态下降或疾病活动性增强。
HPLL评分与简化版区别
HPLL评分进一步纳入了血小板和肺门外交感淋巴结相关因素,更适合对脾型患者做更细化分层。
| 评分系统 | 核心参数 | 5年生存结果 |
|---|---|---|
| HPLL评分 | Hb、血小板、LDH、肺门外交感淋巴结 | 淋巴瘤特异生存:低危94%,中危78%,高危69% |
| 简化HPLL | Hb<9.5 g/dL、PLT<80×10⁹/L、LDH升高、肺门外交感淋巴结 | A组95%,B组87%,C组68% |
如果脾型患者已经出现贫血、血小板下降和LDH升高,通常提示疾病对骨髓、脾脏或全身状态的影响已经更明显,后续监测不能放松。
淋巴结型为什么更难判断
淋巴结边缘区淋巴瘤相对少见,且生物学特征更复杂。到目前为止,还没有被广泛确立的NMZL专属预后评分系统。
现阶段,滤泡淋巴瘤常用的FLIPI在部分患者中具有一定参考价值,但并不是专门为NMZL设计,因此解释时要更谨慎。相关研究仍在推进,目标是把分子特征和临床数据整合起来,建立更适合NMZL的风险模型。
这也提醒患者一个现实问题:同样是边缘区淋巴瘤,不同亚型获得的证据强度并不一致。对NMZL患者来说,诊断准确、病理复核和个体化随访尤其关键。
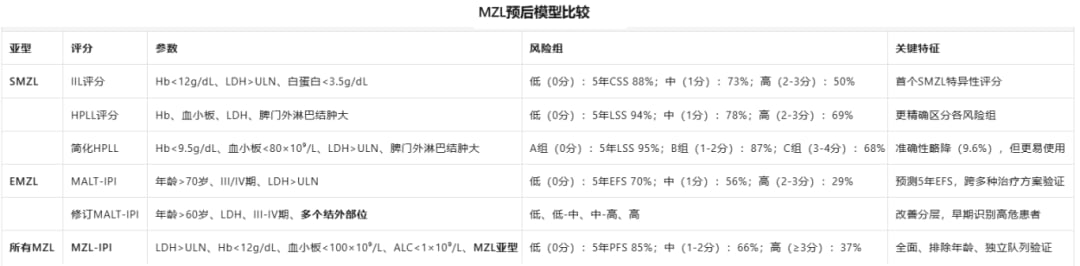
不同亚型对应的评分系统并不相同,统一模型的出现提高了临床可比性。
MZL-IPI为什么值得重点关注
过去的预后模型大多只适用于某一个亚型,临床上不方便横向比较。MZL-IPI的价值,在于它试图建立一个适用于所有MZL亚型的统一预后框架。
MZL-IPI包含哪些变量
基于FIL NF10研究,这一模型主要纳入以下参数,每项赋值1分:
- LDH升高
- 血红蛋白<12 g/dL
- 血小板<100×10⁹/L
- 绝对淋巴细胞计数<1×10⁹/L
- MZL亚型因素
它的优点之一是不包含年龄。这在老年患者占比较高的惰性淋巴瘤中尤其重要,因为年龄往往会干扰治疗决策,而这个模型尽量避免把“年纪大”直接等同于“预后差”。
MZL-IPI能把患者分成几组
| 风险分组 | 评分 | 5年PFS |
|---|---|---|
| 低危 | 0分 | 85% |
| 中危 | 1–2分 | 66% |
| 高危 | ≥3分 | 37% |
这组差异说明,MZL内部并不是“都差不多”。当患者进入高危层级后,未来几年内疾病进展概率明显更高,随访频率、复查策略和治疗规划都应更积极。
MZL-IPI还能预测POD24吗
可以。该模型不仅用于看长期无进展生存,也能帮助预测早期进展风险。
| 风险组 | POD24发生率 | 风险提示 |
|---|---|---|
| 低危 | 6% | 总体较低 |
| 中危 | 15% | 风险升高,OR 2.60,P=0.024 |
| 高危 | 34% | 风险显著升高,OR 7.67,P<0.001 |
这也是MZL-IPI最实用的地方之一:它不只是“回顾性地解释谁预后差”,而是能提前识别谁更需要严密监测和更快调整方案。
PET/CT和ctDNA能帮上什么忙
除了传统临床评分,新兴工具正逐步改变边缘区淋巴瘤的风险评估方式。
PET/CT适合哪些情况
过去很多人认为惰性淋巴瘤做PET/CT价值有限,但在MZL中并非如此。现有数据提示:
- 脾型和淋巴结型中,FDG摄取率可超过75%
- 结外型中,FDG显像能力与病灶部位和大小相关,总体约80%可显示
- 达到完全代谢缓解,即Deauville评分≤2,与更长无进展生存相关
对临床而言,PET/CT的意义不只是“看见病灶”,更在于评估代谢反应、辅助判断疗效,必要时也可帮助识别可疑转化病灶并指导活检部位。
ctDNA会成为未来重点吗
ctDNA属于循环肿瘤DNA检测,是一种非侵入性分子监测手段。在MZL中,它的价值正在逐步显现,主要方向包括:
- 识别高风险患者
- 动态监测治疗反应
- 更早发现分子层面的复发信号
这类技术目前更偏向前沿监测工具,尚未完全取代常规复查,但对复发风险高、病情复杂或疗效判断不清的患者,未来意义很大。
外周血流式结果异常意味着什么
部分患者检查时会发现外周血存在循环淋巴瘤细胞。这个结果常让人紧张,但它并不必然代表预后更差。
现有信息显示:
- 检测到循环淋巴瘤细胞,并不一定提示无进展生存更差
- 在一些分析中,反而可能与更长总生存相关
- 但在结外型患者中,如果接受的是免疫化疗,循环淋巴瘤细胞阳性可能与更短PFS相关
因此,这类结果不能脱离治疗背景和亚型单独解读。最稳妥的做法,是把它作为整体评估中的一部分,而不是看到“阳性”就等同于“很危险”。
播散型边缘区淋巴瘤更难治吗
播散型MZL通常指同时存在结外、脾、淋巴结、骨髓或外周血等多部位受累,但又没有明确原发部位。这类情况之所以重要,是因为它提示疾病更复杂、归类更困难。
在MZL-IPI中,播散型被纳入独立亚型变量,说明它对预后判断具有实际影响。临床上遇到这类患者,往往更需要多学科整合判断,包括病理、影像、血液学和分子检测共同参与。
复发后还有哪些治疗方向
对于复发或难治性边缘区淋巴瘤,目前还没有专门公认的统一预后指数,因此临床上常结合POD24、既往缓解深度、复发节奏、是否转化以及患者基础状态来制定策略。
治疗方向也在从传统方案逐步走向更精准的靶向和免疫治疗,包括:
- 伊布替尼(ibrutinib)
- 泽布替尼(zanubrutinib)
- 奥布替尼(orelabrutinib)
- 匹妥布替尼(pirtobrutinib)
- 来那度胺(lenalidomide)联合利妥昔单抗(rituximab)
- 双特异性抗体,如莫妥珠单抗、艾可瑞妥单抗
- CAR-T细胞治疗,如axi-cel
需要强调的是,不同药物和技术的适应证、证据成熟度、可及性和地区获批状态并不完全一致。患者在复发后最容易遇到的现实难点,往往不是“有没有新药”,而是“不知道自己适不适合、国内能不能用、是否需要跨境获取、怎样评估风险收益”。
日常随访要盯住哪些信号
边缘区淋巴瘤病程长,很多风险变化发生在随访中。比起一次性的“好或坏”,持续观察更重要。
复查时重点看什么
- LDH是否持续升高
- 血红蛋白、血小板、淋巴细胞计数是否下降
- 淋巴结或脾脏是否进行性增大
- 是否出现发热、盗汗、体重下降等B症状
- 病灶是否在短期内快速增加
- 是否在24个月内进展
哪些情况要尽快回医院
- 原本稳定的病灶突然长得很快
- 出现明显乏力、贫血、出血倾向
- 持续低热或夜间盗汗
- 腹胀明显、左上腹不适加重,提示脾脏变化
- 影像提示新发多部位病灶
对惰性淋巴瘤患者来说,规律随访不是“走形式”,而是决定能否及时识别高危进展的重要环节。
患者最该关心的不是分数,而是决策
无论是MALT-IPI、IIL、HPLL,还是MZL-IPI,它们的核心价值都不是给患者贴标签,而是帮助完成三件事:
- 判断病情未来是更可能平稳,还是更可能早进展
- 决定随访该多密,需不需要更积极的复查工具
- 在复发或疑似转化时,更快进入下一步治疗决策
也就是说,评分模型不能替代医生,但能让治疗更少依赖模糊经验。
治疗信息差,往往比疾病本身更耽误时机
边缘区淋巴瘤的难点,常常不是完全无路可走,而是患者很难在短时间内弄清:自己属于哪类风险、复发是不是危险信号、靶向药和新型免疫治疗是否适合、不同地区药物可及性差异有多大。
对需要进一步了解前沿方案的患者,MedFind可以提供两类实际帮助:一是围绕病理分型、治疗路径、复发后选择进行辅助问诊与方案解读,帮助把复杂术语转化成可执行的问题清单;二是针对已明确适合且具备可及性的抗癌药物,提供跨境直邮信息支持,减少因信息滞后带来的等待和盲区。对惰性但可能反复的边缘区淋巴瘤来说,越早把预后判断做清楚,越有机会把每一次治疗窗口用在最合适的地方。
【参考文献】
Haematologica. 2026 Mar 5. doi: 10.3324/haematol.2025.300416