确诊转移性激素敏感性前列腺癌后,最关键的问题不是“先用哪种药”这么简单,而是:要不要做基因检测?哪些突变会影响生存期?高负荷和低负荷差别有多大?mHSPC患者能否提前布局靶向治疗与后续耐药后的方案衔接?这些问题,直接决定治疗强度、监测方式和未来用药窗口。
mHSPC为什么必须重视分层?
mHSPC不是一种“长得都一样”的前列腺癌。临床上至少要同时看三个维度:转移出现时间、转移负荷、分子生物学特征。这三者叠加后,患者的预后和治疗策略往往完全不同。
传统上,医生会先依据影像学把患者区分为同步性转移或异时性转移,以及低负荷或高负荷疾病。常用的高负荷定义包括:至少4处骨转移,且其中超过1处位于脊柱或骨盆之外,和或存在内脏转移。
这不是纸面分类。它直接对应生存差异:异时性、低负荷患者的中位总生存期可接近8年,而新发高负荷患者往往只有3到4年。这也是为什么同样是mHSPC,有人适合双药内分泌强化,有人一开始就要考虑三药方案,甚至尽早进入生物标志物驱动治疗路径。
| 临床分层维度 | 常见类型 | 对治疗决策的意义 |
|---|---|---|
| 转移出现时间 | 同步性转移、异时性转移 | 影响疾病侵袭性判断与强化治疗需求 |
| 肿瘤负荷 | 低负荷、高负荷 | 影响是否考虑三药治疗及局部治疗价值 |
| 分子特征 | BRCA2、PTEN、SPOP、PSMA等 | 影响靶向治疗、预后评估和随访方式 |
为什么说基因检测已不是“可选项”?
对mHSPC患者来说,基因检测的价值至少体现在三件事上。
- 第一,识别遗传风险。胚系突变与家族成员患癌风险相关,尤其是DNA修复相关基因异常。主流指南普遍支持mHSPC患者进行胚系检测。
- 第二,提前布局后续治疗。即使某些靶向药先在mCRPC阶段建立适应证,提前知道BRCA2等突变状态,也有助于一旦进展时迅速切换方案,不错过治疗窗口。
- 第三,筛选当前或未来可用的生物标志物驱动治疗。例如BRCA2异常、PTEN缺失、PSMA表达等,都可能影响是否适合特定靶向治疗或临床研究。
从患者角度看,真正需要警惕的是“只盯着PSA,不做分子分层”。因为PSA只能反映部分AR驱动肿瘤的动态,不能替代基因层面的风险判断。
mHSPC常见基因异常有哪些?
现有研究显示,mHSPC的基因组图谱与局限期前列腺癌和mCRPC有连续性,但侵袭性异常的比例更高。较常见的改变包括TMPRSS2-ERG融合、PTEN异常、TP53异常、BRCA2异常、CDK12异常和SPOP突变等。
其中,患者最需要记住的是三类:
- DNA修复通路异常:如BRCA2、ATM。这类异常与更高侵袭性、遗传风险和PARP抑制剂敏感性密切相关。
- 抑癌基因缺失:如PTEN、TP53、RB1。往往提示病情更凶、进展更快,部分还关联对特定治疗方式的差异反应。
- AR通路相关生物学差异:如SPOP突变、PSMA表达高低、AR转录活性高低。这类信息会影响内分泌治疗获益、监测手段与后续放射性配体治疗机会。
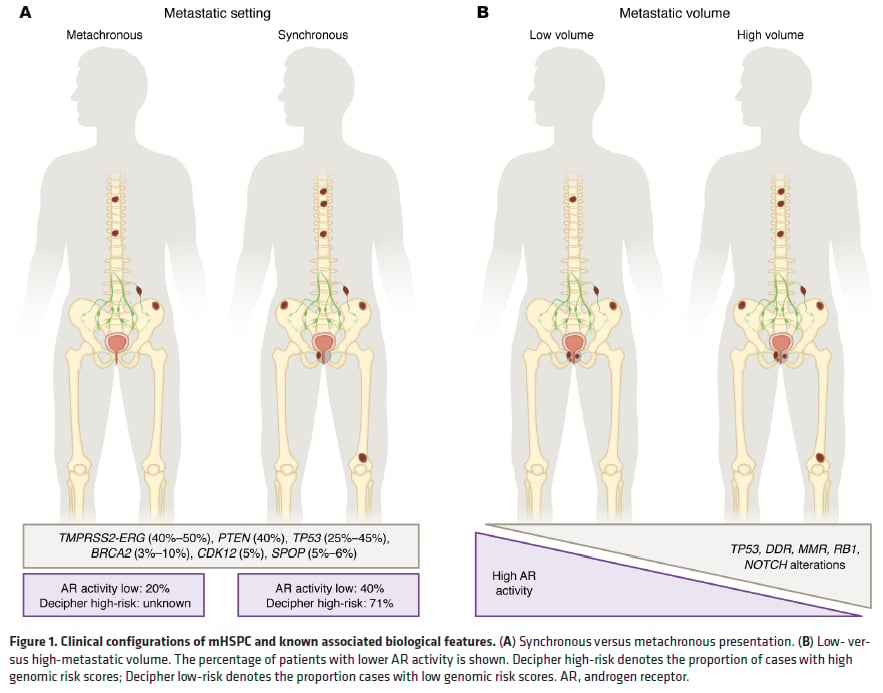
mHSPC中常见基因异常及不同疾病负荷下的富集趋势
一个重要结论是:高负荷mHSPC更容易富集抑癌基因缺失、DNA修复基因异常和WNT通路变异。这解释了为什么部分患者虽然都接受ADT联合ARPI,但疗效持续时间差别很大。
BRCA2突变意味着什么?
BRCA2是mHSPC中最值得优先关注的基因之一。原因很直接:它既关乎遗传风险,又可能直接改变治疗路径。
BRCA2异常的患者,往往肿瘤侵袭性更强,进展速度更快。更值得注意的是,在BRCA变异背景下,传统“低负荷预后更好”的经验可能被削弱,也就是说,分子高危有时比影像学低负荷更重要。
这也是PARP抑制剂被前移研究的核心逻辑。对于同源重组修复基因异常尤其是BRCA2突变患者,在ADT和ARPI基础上加用PARP抑制剂,正在把治疗从“先等耐药再说”改成“早期精准强化”。
PARP抑制剂在mHSPC走到哪一步了?
目前最受关注的数据来自AMPLITUDE研究。在携带BRCA或其他同源重组修复基因突变的mHSPC患者中,尼拉帕利(则乐, Niraparib)联合醋酸阿比特龙(泽珂, Abiraterone acetate),相较安慰剂联合阿比特龙,可显著改善放射学无进展生存期,风险比为0.63。
在323例BRCA2突变患者的探索性分析中,风险比进一步降至0.46,提示BRCA2突变是获益更明确的人群。
| 研究与人群 | 治疗方案 | 核心结果 | 临床意义 |
|---|---|---|---|
| AMPLITUDE,总体HRR突变mHSPC | 尼拉帕利+阿比特龙 vs 安慰剂+阿比特龙 | rPFS风险比0.63 | 支持PARP抑制剂前移 |
| AMPLITUDE,BRCA2突变亚组 | 同上 | rPFS风险比0.46,95% CI:0.32-0.66 | BRCA2是更强获益信号 |
这组结果带来的现实意义非常大:一旦患者在mHSPC阶段就完成规范检测,未来就有机会更早进入更精准的治疗路径,而不是等到病情进展后再仓促补做。
PTEN缺失患者能从AKT抑制剂获益吗?
PTEN缺失是前列腺癌里常见且重要的高危事件。它会激活PI3K-AKT通路,推动肿瘤增殖和治疗耐受。对于这类患者,AKT抑制剂被认为是很有前景的方向。
III期CAPITELLO-281研究评估了PTEN缺失mHSPC患者在ADT加阿比特龙基础上,联合卡匹色替(荃科得, Capivasertib)的效果。研究采用免疫组化定义PTEN缺失:至少90%的恶性细胞无染色。约25%的筛查患者存在PTEN缺陷。
结果显示,加入卡匹色替后,放射学无进展生存期获得统计学显著改善,风险比0.81。并且,PTEN缺失程度越高,获益越明显,提示这不是简单的“阳性或阴性”问题,而是可能存在更精细的分层空间。
临床上这意味着两点:一是PTEN检测值得做;二是检测方法和报告解读非常关键,不能只看一行“有无缺失”。
SPOP、TP53、RB1结果该怎么理解?
并不是每个突变都会立刻对应某个已上市药物,但它们依旧有很强的临床意义。
- SPOP突变:在部分研究中与ADT联合ARPI后的更好预后相关,可能提示对AR通路抑制更敏感。
- TP53异常:常与更侵袭的病程、更多转移灶和更差结局相关。
- RB1异常:与谱系可塑性、神经内分泌分化风险和多部位进展倾向有关。
对患者来说,这些结果最重要的价值不只是“有没有药”,而是帮助医生判断:是否要更早强化治疗,是否不能只靠PSA监测,是否在进展时应尽快复活检。
基因检测用原发灶、转移灶还是ctDNA?
这是门诊里最常见的实际问题之一。答案不是一刀切,而是各有优缺点。
| 检测来源 | 优点 | 局限 | 适用提示 |
|---|---|---|---|
| 原发灶组织 | 获取相对容易,早期克隆驱动事件常可检出 | 可能漏掉后期转移过程中新增变异 | 临床最常见基础方案 |
| 转移灶活检 | 更贴近当前肿瘤状态 | 骨转移尤其硬化灶取材困难 | 条件允许时价值高 |
| ctDNA | 微创,可动态监测 | 低负荷mHSPC肿瘤DNA含量低,ADT后更快下降 | 适合辅助监测,但早期可能灵敏度不足 |
如果只能做一次,优先确保检测质量和解读能力。很多患者不是“没做检测”,而是做了覆盖不足、样本不合格或报告不能指导治疗的检测。
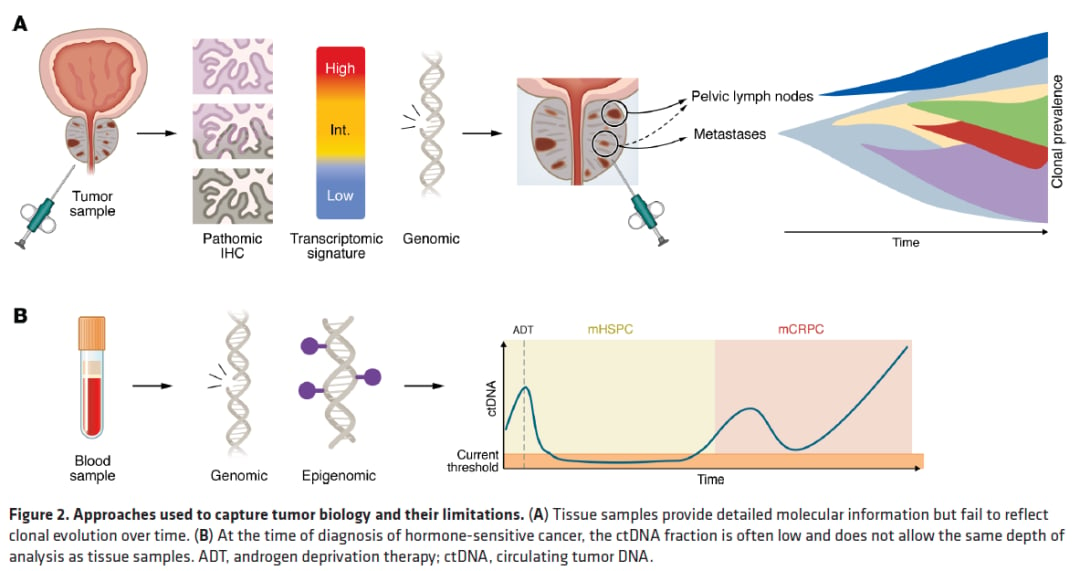
原发灶、转移灶与ctDNA在mHSPC检测中的互补价值
PSMA-PET会改变分期和治疗吗?
会,而且影响越来越大。PSMA-PET正在重塑“是否转移”“是低负荷还是高负荷”“是否属于寡转移”这些传统判断。
研究显示,按PSMA-PET标准,约13%到22%的病例会发生分期迁移,从低负荷被重新归入高负荷。另有研究发现,传统影像学定义为低负荷的患者中,大约30%经PSMA-PET评估后可降为非转移性疾病。
这背后的临床问题非常尖锐:如果分期工具变了,原本建立在传统CT和骨扫描上的治疗分层,还能不能原封不动照搬?
对患者来说,PSMA-PET最大的价值在于更精准识别病灶范围,尤其是寡转移或隐匿转移。但也要知道,影像更灵敏,不等于所有新发现病灶都必须立刻接受同等强度的系统治疗,治疗决策仍需结合生物学风险。
寡转移前列腺癌到底能不能少治一点?
这是很多患者最关心的问题。寡转移并不自动等于“病轻”,它更像一个光谱,而不是固定标签。
部分患者,尤其是原发灶治疗多年后才被PSMA-PET发现少数病灶的异时性寡转移,病程可能相对缓慢。这类患者有机会从转移灶定向治疗中获得较持久控制,甚至延缓ADT启动或延长无ADT生存期。
但另一部分患者的“寡转移”只是检测时看到的冰山一角,很快会发展为广泛转移。现有研究提示,TP53突变、DNA修复基因异常与更多转移灶相关,而多转移和新发mHSPC在分子层面可能更接近。
因此,寡转移患者最不该做的,是仅按病灶数量做决定。更合理的思路是:病灶数量+出现时间+PSMA-PET结果+分子风险一起判断。
转移到骨、肺、肝,预后差别有多大?
转移部位本身就是强预后因素。仅淋巴结转移,或仅低负荷肺转移,通常预后优于广泛骨转移或肝转移。
骨转移是前列腺癌最常见的远处转移形式。骨微环境会帮助肿瘤细胞休眠、再激活和扩张,形成以成骨性病灶为主的表现。针对骨转移,氯化镭-223(多菲戈, Radium-223)已用于去势抵抗阶段伴骨转移患者,且正在mHSPC领域继续探索。
肺转移比较特殊。部分仅肺转移患者的生存结局优于历史对照,提示其生物学可能不同于一般内脏转移。
肝转移则往往提示更差预后,可能与更低AR依赖性、PSMA表达偏低以及更高侵袭性有关。对于这类患者,仅依赖PSA往往不够,影像随访必须更积极。
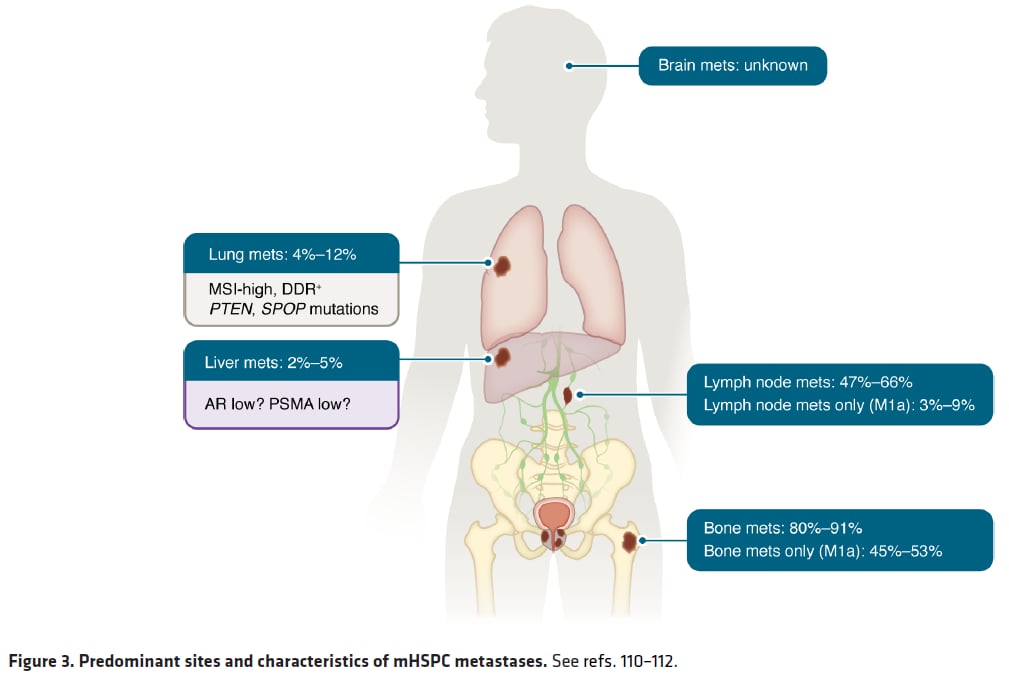
不同转移部位可能对应不同的肿瘤生物学和临床结局
PSMA高低为什么越来越重要?
PSMA不只是影像靶点,也越来越像一个治疗分层工具。一般来说,PSMA高表达常伴随更高AR活性;PSMA低表达肿瘤则更可能表现出低AR活性、基底样表型和较差激素治疗反应。
这意味着:
- PSMA高表达患者,未来接受PSMA靶向放射性配体治疗的概率更高;
- PSMA低表达患者,可能更需要警惕“PSA看起来不算太高,但病情并不温和”;
- 肝转移等部位常见PSMA表达更低、异质性更强,随访更不能偷懒。
III期PSMAddition研究已达到主要终点,提示在PSMA-PET阳性mHSPC中,加用Lu-PSMA-617可使放射学进展或死亡风险降低28%。这说明前列腺癌治疗正在从“按疾病阶段选药”,进一步走向“按分子和表型特征精准加药”。
为什么有些患者PSA不高,病情却更凶?
因为并非所有mHSPC都高度依赖AR通路。部分肿瘤存在低AR转录活性、神经内分泌特征或谱系可塑性,这类患者可能出现PSA与真实肿瘤负荷不匹配的情况。
在PEACE-1等研究中,基线神经内分泌标志物表达,或TP53、RB1、PTEN中至少两种基因异常共存,均与不良预后相关。即使尚未形成典型的小细胞神经内分泌前列腺癌形态,这类患者也往往更需要密集影像监测,而不是只盯PSA。
如果出现以下情况,应警惕“PSA失真”:
- 影像进展明显快于PSA变化;
- 内脏转移尤其肝转移出现;
- 病理提示神经内分泌标志物阳性或Ki-67高表达;
- TP53、RB1、PTEN等高危异常叠加存在。
ADT、ARPI、化疗和靶向药该怎么理解?
当前mHSPC治疗已经进入“组合时代”。基础框架通常是ADT,在此之上叠加ARPI、化疗或生物标志物驱动药物。
- ADT+ARPI:已成为广泛适用的强化基础,适用于绝大多数mHSPC患者。
- ADT+ARPI+多西他赛:更常考虑用于新发高负荷患者,尤其是疾病进展快、内脏转移或高危生物学特征明显者。
- ADT+ARPI+PARP抑制剂:面向BRCA2等同源重组修复异常患者。
- ADT+ARPI+AKT抑制剂:面向PTEN缺失患者。
- ADT+ARPI±PSMA靶向放射性配体治疗:面向PSMA-PET阳性人群,前景正在快速打开。
真正的难点,不是药名多,而是谁需要加,什么时候加,哪些人可以少加。这正是基因检测和生物标志物分层的意义。
副作用和居家管理要提前准备什么?
治疗越精准,越要把副作用管理做在前面。很多患者不是被肿瘤本身打断治疗,而是被可预防、可处理的不良反应拖垮了依从性。
内分泌治疗常见问题
- 潮热、乏力、性欲下降:规律作息,分层运动,避免高温环境和酒精刺激。
- 血压、血糖、血脂波动:家庭血压计、空腹血糖监测要常规化,尤其合并糖尿病或高血压者。
- 骨量流失:补充钙和维生素D前先评估;适度抗阻训练和步行有帮助。
阿比特龙相关管理
阿比特龙使用过程中,要特别关注肝功能、血钾、水肿和血压。出现乏力加重、心悸、肌无力或明显下肢水肿,应尽快复查电解质和肝功能。
PARP抑制剂相关管理
尼拉帕利常需关注血常规、疲劳、恶心等问题。治疗初期建议更密集监测血象。若出现头晕、活动后气促、面色苍白,应警惕贫血。
AKT抑制剂相关管理
卡匹色替治疗中,需要重视腹泻、皮疹、血糖升高等不良反应。合并糖尿病患者更需提前与医生沟通血糖管理方案。
治疗期间如何判断是不是有效?
最实用的观察指标包括PSA下降深度、影像变化和症状改善。其中,治疗后6到8个月PSA降至0.2 ng/mL以下,持续被证明与更好预后相关。
但一定要记住:PSA不是万能尺子。对低AR活性、PSMA低表达、神经内分泌倾向或内脏转移患者,影像和临床症状的重要性会明显上升。
可以把监测理解为三条线并行:
- PSA与睾酮等实验室指标;
- CT、骨扫描或PSMA-PET等影像复评;
- 疼痛、体重、食欲、体能状态等生活质量变化。
药物可及性是患者最现实的难点
很多患者真正焦虑的,不是“有没有新药”,而是“适不适合我”“国内能不能尽快用上”“获批和可及之间差多远”。尤其是生物标志物驱动治疗,往往面临三个现实门槛:
- 检测是否做对、做全;
- 药物在不同国家和地区的获批进度不同;
- 即便有适应证,医院准入、处方路径、经济负担也可能形成延迟。
对mHSPC患者来说,时间窗口非常宝贵。越是BRCA2、PTEN等明确异常人群,越不适合在“等等看”中错过治疗前移机会。
下一步最值得患者立刻行动的三件事
- 补齐分层信息:确认自己属于同步或异时性、低负荷或高负荷,是否做过PSMA-PET。
- 完成关键检测:至少搞清楚胚系检测、肿瘤组织或ctDNA检测是否覆盖BRCA2、PTEN等关键位点。
- 让方案与生物学对上号:如果已经有BRCA2、PTEN、PSMA等结果,就要进一步判断自己是否存在更合适的靶向治疗或更密切的监测路径。
把“信息差”变成治疗机会
mHSPC正在快速进入精准治疗时代。对于患者和家属来说,真正决定结局的,往往不是单一药物本身,而是能否尽早识别高危生物学特征,尽早进入合适方案。
如果正在面对“基因检测怎么选”“报告看不懂”“某个前沿药物是否适合自己”“国内外可及性差异太大”等问题,尽快把这些关键问题问清楚,通常比盲目换药更重要。
MedFind持续更新全球前列腺癌前沿证据、药物信息与真实可及路径。对于已经明确生物标志物、希望进一步了解前沿药物方案的患者,可通过辅助问诊梳理检测结果与治疗思路;如确有合规可及需求,也可进一步了解跨境直邮服务,让重要药物信息不再停留在“知道”,而是真正走向“用得上”。
【参考文献】
Bernard-Tessier, Alice, and Himisha Beltran. “Exploring the biology of metastatic hormone-sensitive prostate cancer: on the road to precision medicine.” The Journal of Clinical Investigation vol. 136,3 e200920. 2 Feb. 2026, doi:10.1172/JCI200920