胶质母细胞瘤治疗的困境与挑战
胶质母细胞瘤(Glioblastoma, GBM)是成人中最常见且最具侵袭性的原发性脑肿瘤。尽管采用了手术、放疗和化疗等综合治疗手段,其复发率仍高达90%以上,给患者和家庭带来了巨大的挑战。近年来,以PD-1/PD-L1抑制剂为代表的免疫检查点阻断(ICB)疗法在多种癌症中取得了革命性成功,但在胶质母细胞瘤的治疗中却效果有限。其主要原因在于,GBM术后形成的肿瘤微环境(pTME)是一种典型的“免疫冷”环境,缺乏能够杀伤肿瘤的细胞毒性T淋巴细胞(CTL),使得免疫治疗药物无的放矢。
创新性复合设备HFCD的诞生
为了攻克这一难题,一项发表于《细胞》子刊Cell Biomaterials的最新研究带来了一线曙光。研究团队成功开发出一种创新的水凝胶纤维复合设备(hydrogel-fiber composite device, HFCD),旨在通过局部精准调控,将“免疫冷”的术后微环境“加热”,从而有效激活免疫系统,抑制胶质母细胞瘤的复发。

HFCD如何“唤醒”免疫系统?
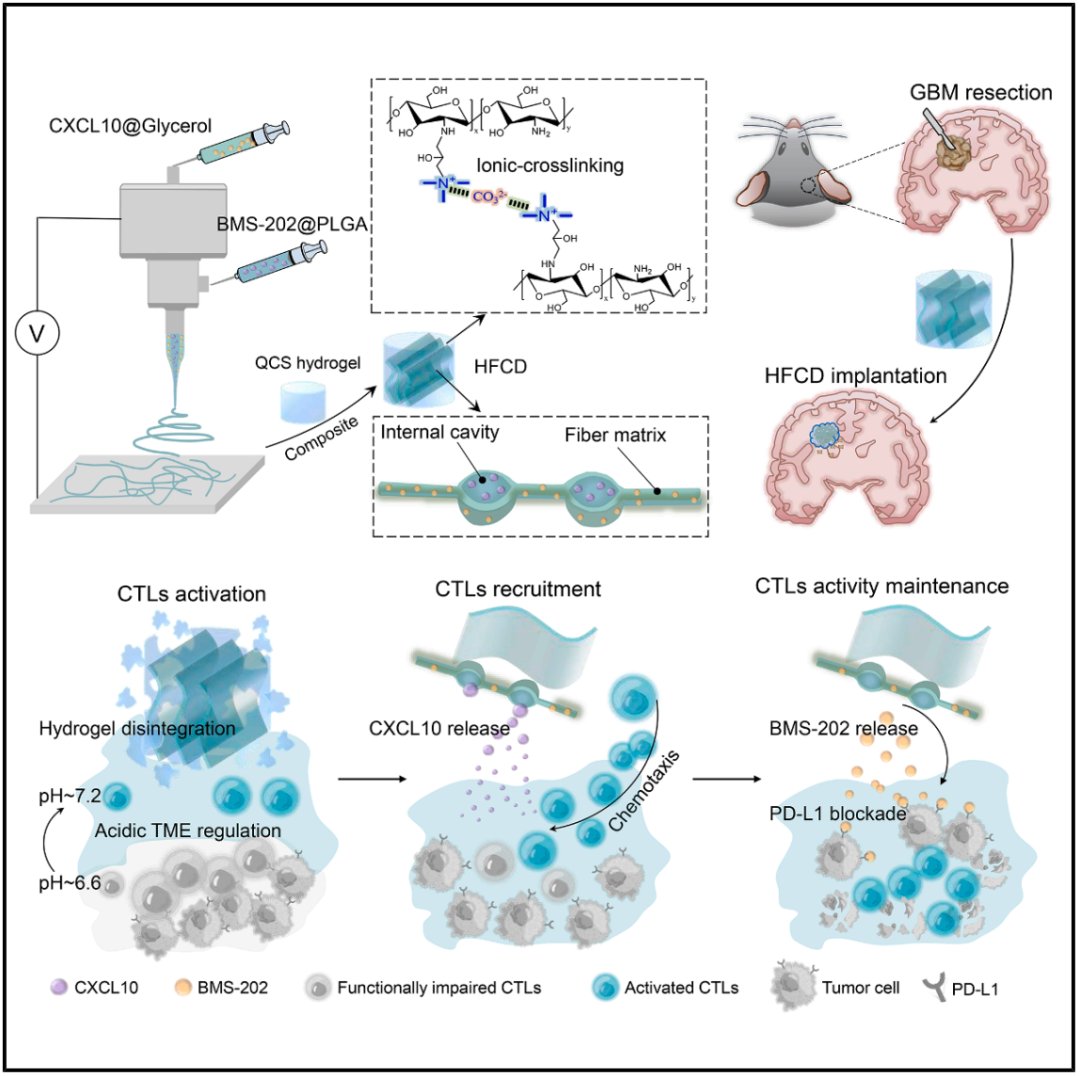
这种精巧的设备是如何发挥作用的呢?HFCD的设计实现了对免疫反应的时空协同调控,其作用过程可分为关键几步:
- 第一步:改善“土壤”:HFCD设备中的水凝胶成分含有碳酸钠,在植入GBM切除腔后,它能首先中和酸性的肿瘤微环境,为免疫细胞创造一个更适宜生存和战斗的“土壤”。
- 第二步:招募“士兵”:随着水凝胶的分解,内部包裹的静电纺丝纤维暴露出来。这些纤维会释放趋化因子CXCL10,如同发出“集结号”,特异性地将作为免疫系统主力军的细胞毒性T淋巴细胞(CTL)大量招募到肿瘤区域。
- 第三步:解除“束缚”:在T细胞集结后,纤维基质会持续缓慢地释放PD-L1抑制剂。这种药物能够解除肿瘤细胞对T细胞的“束缚”(免疫抑制),让T细胞恢复并维持其强大的肿瘤杀伤能力,精准清除残余的癌细胞。
临床前研究结果:显著抑制肿瘤复发
在胶质母细胞瘤的原位切除动物模型中,HFCD展现了令人鼓舞的治疗效果。研究结果显示:
- 接受HFCD治疗的组别中,有40%的病例实现了肿瘤的完全抑制,未出现复发。
- 治疗组的中位生存期被显著延长至49天,远超对照组。
- 更重要的是,该疗法还成功诱导了持久的免疫记忆反应,这意味着免疫系统未来能够更好地识别并对抗可能复发的肿瘤。
展望未来:GBM治疗的新希望
这项研究成果表明,HFCD作为一种极具前景的胶质母细胞瘤辅助治疗设备,通过局部、程序化地重塑肿瘤免疫微环境,成功解决了当前ICB疗法在GBM治疗中的核心痛点。它不仅为抑制这种恶性脑瘤的复发提供了一种全新的、广泛适用的策略,也为其他“免疫冷”肿瘤的治疗带来了新的启示。
虽然该技术距离临床应用还有一段路要走,但它无疑为胶质母细胞瘤患者带来了新的希望。对于正在寻求前沿治疗方案的患者,了解最新的科研动态至关重要。如果您想获取更多关于癌症治疗的个性化信息,可以考虑使用MedFind AI问诊服务进行咨询。