2025年1月1日起康方生物两款双抗,执行国谈价格!
康方双抗首次纳入国家医保:

全球第一款肿瘤免疫双抗(卡度尼利单抗)
全球第一款靶免双抗(依沃西单抗)
卡度尼利:由6166元/瓶降到1860元/瓶,复发转移性宫颈癌还可医保报销!
依沃西:由2299元/瓶降到736元/瓶,EGFR-TKI失败nsq-NSCLC可享受医保报销!(来源网络,仅供参考)
康方坐拥两个双抗上市产品:
PD-1/VEGF双抗依沃西单抗(AK112)、
开坦尼®(PD-1/CTLA-4双特异抗体,AK104,卡度尼利单抗注射液)。另有派安普里单抗(PD-1单抗)。
3项头对头PD-1单抗 :双抗 VS PD-1单抗,孰优孰劣,会有分晓,敬请期待~
目前,依沃西在国内已经有1项新药上市申请获得国家药品监督管理局受理,在全球范围内已启动/正在开展另外4项关键注册性III期临床试验,其中3项是以PD-1单抗为阳性对照药物的头对头研究:
🔹AK112-303研究:依沃西单药对比帕博利珠单抗单药一线治疗PD-L1表达阳性的NSCLC的注册性III期临床研究,已完成入组。
🔹HARMONi/AK112-301研究:依沃西联合化疗用于经第三代EGFR-TKI治疗进展的EGFR突变、局晚期或转移性非鳞状非小细胞肺癌的国际多中心注册性III期临床研究
🔹AK112-306研究:依沃西联合化疗对比替雷利珠单抗联合化疗一线治疗局部晚期或转移性鳞状非小细胞肺癌的注册性III期临床研究
🔹HARMONi-3研究:依沃西联合化疗对比帕博利珠单抗联合化疗一线治疗转移性鳞状非小细胞肺癌的国际多中心注册性III期临床研究
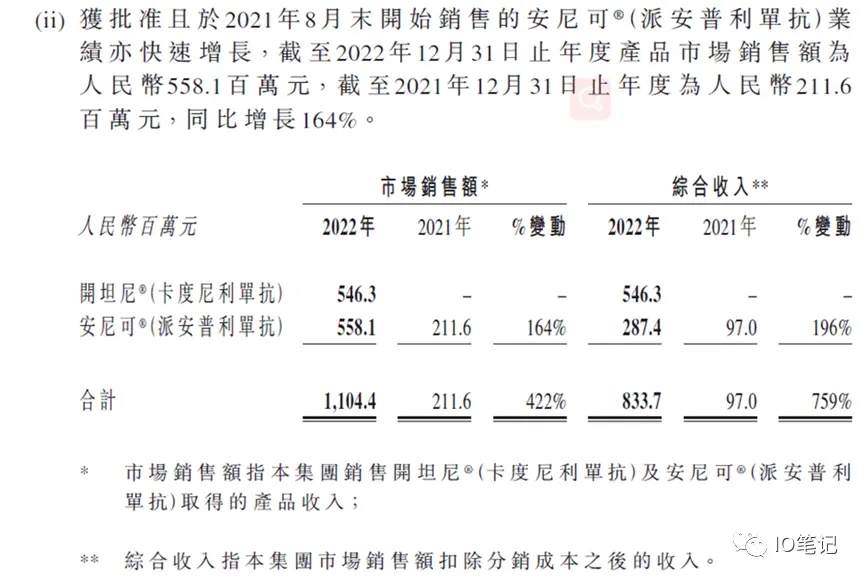
此外,2023年3月15日,康方生物发布2022年业绩报:全球首创卡度尼利双抗上市首6个月,销售额5.46亿人民币。(2022年6月29日,国家药品监督管理局通过优先审评审批程序附条件批准康方药业有限公司卡度尼利单抗注射液(商品名:开坦尼)上市。
该药品为我国自主研发的创新双特异性抗体,适用于既往接受含铂化疗治疗失败的复发或转移性宫颈癌患者的治疗。)
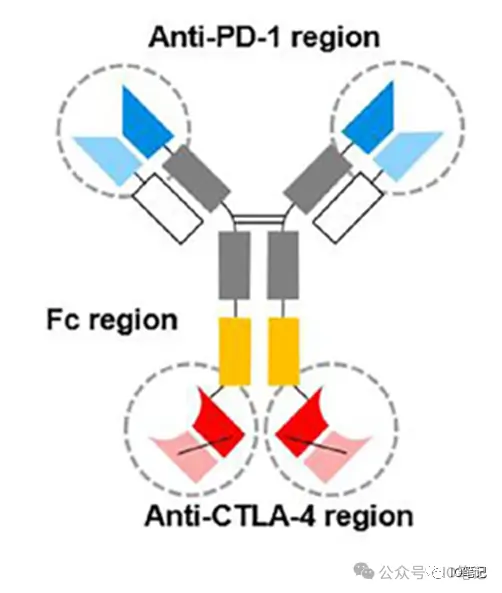
上图 开坦尼®(PD-1/CTLA-4双特异抗体,卡度尼利单抗注射液)结构示意图 卡度尼利单抗注射液是一种靶向人PD-1和CTLA-4的双特异性抗体,可阻断PD-1和CTLA-4与其配体相互作用,从而阻断PD-1和CTLA-4信号通路的免疫抑制反应,促进肿瘤特异性的T细胞免疫活化,进而发挥抗肿瘤作用。
卡度尼利单抗是全球首款PD-1/CTLA-4双抗,在国内享受优先审评审批程序,基于II期单臂试验上市的抗肿瘤创新药,采用单臂研究设计,研究终点选择的是ORR。 卡度尼利单抗的获批是基于一项关键性临床研究,入组患者为既往接受含铂化疗治疗失败的复发或转移性宫颈癌(R/M
CC)的全人群患者。 该研究的结果已于2022年美国妇科肿瘤学会(SGO)年会上发表。在100例可评估疗效的全人群(无论PD-L1表达阳性或阴性)患者中,经独立影像学评估委员会(IRRC)确认的客观缓解率(ORR)为33.0%,其中完全缓解(CR)率为12.0%,6个月和12个月持续反应时间(DOR)率分别为77.6%和52.9%,中位无进展生存期(mPFS)为3.75个月,中位生存期(mOS)为17.51个月。在PD-L1阳性(CPS≥1)患者中,ORR更高达43.8%,mPFS高达6.34 个月,mOS数据尚未成熟。在国内已获批的疗法中,宫颈癌患者二线治疗的中位总生存约5~9个月,相较之下,卡度尼利单抗在全人群复发或转移性宫颈癌患者中的中位总生存期达17.51个月,比已获批疗法延长8~13个月的总生存期,为中国患者带来了颠覆性的治疗选择。
附:康方双抗管线附:派安普里单抗(PD-1单抗)目前获批2个适应症:霍奇金淋巴瘤、一线肺鳞癌。
附:康方双抗管线
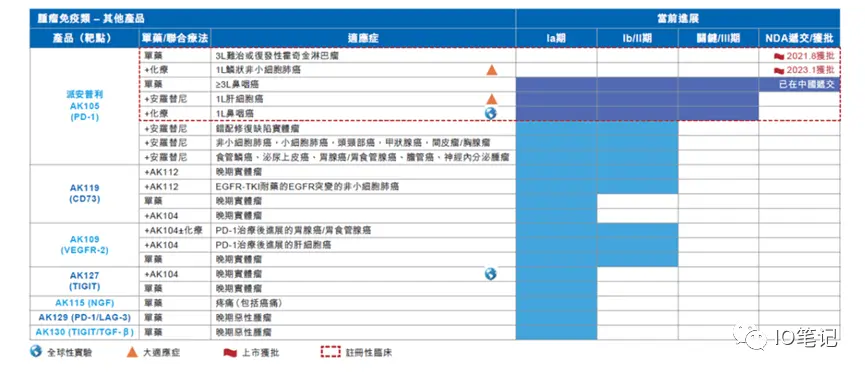
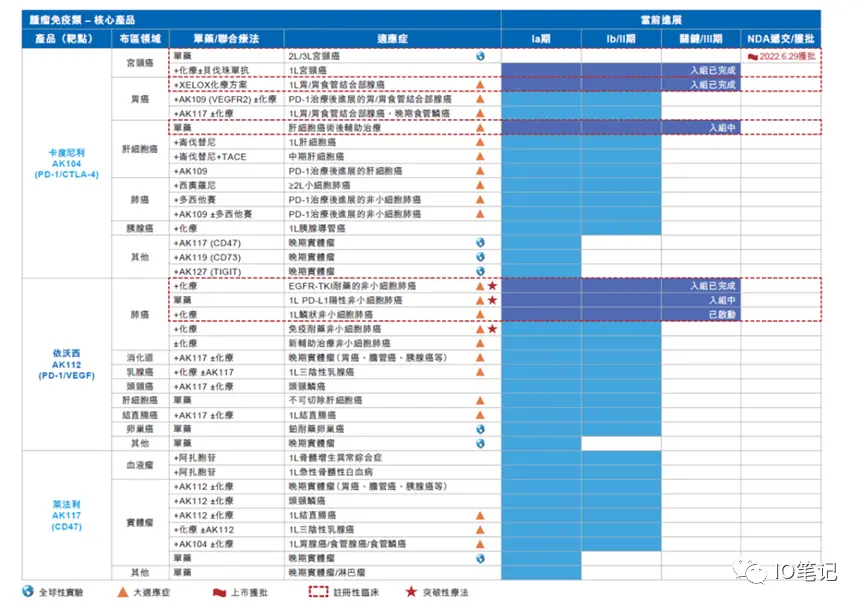
附:派安普里单抗(PD-1单抗)目前获批2个适应症:霍奇金淋巴瘤、一线肺鳞癌。
出处:2022康方财报
http://cj.sina.com.cn/announcement/detail?type=hk¬ice_id=732266263872&symbol=hk09926&from=singlemessage
转自:IO笔记