面对三阴性乳腺癌(TNBC),许多患者和家属的第一反应是“难治”。作为乳腺癌中最具侵袭性的亚型,它因为缺乏雌激素受体、孕激素受体和HER2受体,使得常规的激素治疗和靶向治疗几乎无用武之地。化疗和放疗成了患者最后的“盾牌”。然而,放射治疗(RT)在临床应用中常面临一个残酷的悖论:为了杀灭肿瘤,需要加大放射剂量,但高剂量射线会对周围健康组织造成不可逆的损伤;而如果降低剂量,肿瘤内部那层由胶原纤维堆积而成的“物理屏障”又会阻碍药物和活性氧的渗透,导致疗效大打折扣。如何能在不伤害身体的前提下,精准“爆破”肿瘤核心?中国医学科学院放射医学研究所的最新研究,为我们带来了一个令人振奋的答案。
肿瘤的“盔甲”:为什么普通放疗难以彻底清除三阴性乳腺癌
要理解这项研究的突破性,我们首先要看看三阴性乳腺癌的生存环境。这类肿瘤非常聪明,它们在生长过程中会分泌大量的胶原蛋白,在肿瘤组织周围形成一层厚厚的、质地坚硬的“细胞外基质”。这就像是给肿瘤穿上了一层厚重的“防弹衣”,或者说是在癌细胞周围筑起了一道“高墙”。普通的纳米药物和放疗产生的活性氧(ROS)很难穿透这层墙,只能在表面徘徊,而深层的癌细胞则躲在墙后继续生长、甚至发生转移。此外,放疗的原理是利用高能射线产生自由基来破坏癌细胞的DNA,但这种“地毯式轰炸”往往杀敌一千自损八百,导致患者出现放射性炎症、免疫力低下等副作用。因此,寻找一种既能“拆除高墙”,又能“精准点穴”的增敏策略,是目前全球抗癌研究的重中之重。
黑科技登场:肖特基异质结如何变身抗癌“钻头”
由刘鉴峰研究员和杨丽军研究员团队研发的这种新型材料,全称是Hf-TCPP/Nb₂C@PEG肖特基异质结(HTNCP)。这个名字虽然晦涩,但我们可以将其形象地比喻为一个自带“破障器”和“增强引擎”的精准导航炸弹。它主要由两个核心部件组成:Hf-TCPP纳米金属有机框架(Hf-TCPP nMOF)和Nb₂C MXene纳米片(Nb₂C MXene)。
第一步:光热破障,拆掉肿瘤的“围墙”
研究团队巧妙地利用了Nb₂C MXene优异的近红外二区光热转换能力。当这种药物进入人体并富集在肿瘤部位后,医生只需用特定波长的近红外激光照射肿瘤。此时,Nb₂C MXene就像一块高效的吸光板,将光能转化为温和的热能。这种热能并不足以烧焦组织,但却能精准地降解掉肿瘤周围那层坚硬的胶原纤维基质。这就好比用温火融化了城墙的粘合剂,让肿瘤的“盔甲”变得疏松多孔,为后续的药物进入扫清了障碍。
第二步:放射动力学杀伤,实现“精准爆破”
当围墙倒塌后,真正的重头戏——放射动力学治疗(RDT)开始了。研究中引入了高原子序数的元素铪(Hf),它具有极强的X射线吸收能力。当少量的X射线照射到HTNCP上时,Hf-TCPP nMOF会吸收能量并产生电子。重点来了:在普通的材料中,电子很容易和空穴重新结合,能量就白白浪费了。但由于这是一种特殊的“肖特基异质结”结构,Nb₂C MXene像一个强力磁铁,能迅速把产生的电子吸走,实现“电子-空穴分离”。这种高效的能量转换机制,使得材料能产生大量的活性氧(ROS)。这些ROS就像无数把微型手术刀,从内部彻底粉碎癌细胞的DNA和线粒体,引发癌细胞的凋亡。

HTNCP异质结的“破障-杀伤”序贯治疗策略
1 Gy的奇迹:超低剂量下的高效杀伤
在医学界,放疗的剂量通常以戈瑞(Gy)为单位。为了达到治疗效果,常规放疗往往需要累积极高的剂量。然而,在这项研究中,研究人员在三阴性乳腺癌小鼠模型上,仅使用了1 Gy × 5的极低X射线剂量。这是一个非常惊人的数字。实验数据显示,在经过“先光热破障,后RDT杀瘤”的序贯治疗后,肿瘤的生长受到了显著抑制。通过对比实验可以清晰地看到,如果不进行光热破障,仅仅依靠放疗,肿瘤依然会疯长;而一旦加入了“拆墙”步骤,即使是极低剂量的射线,也能让肿瘤迅速萎缩。
| 治疗方案 | 肿瘤抑制率 | X射线剂量 | 主要机制 |
|---|---|---|---|
| 单纯放疗(RT) | 较低 | 高剂量 | 直接损伤DNA,易受屏障阻碍 |
| 单纯RDT | 中等 | 低剂量 | 产生ROS,但渗透性差 |
| HTNCP序贯疗法 | 极高 | 1 Gy × 5(超低剂量) | 光热破障 + 异质结增强ROS |
更令人欣喜的是,这种疗法不仅杀死了眼前的肿瘤,还产生了所谓的“远隔效应”。研究发现,当一侧的原发肿瘤被治疗后,另一侧未受照射的远端肿瘤也出现了萎缩。这是因为HTNCP在杀伤癌细胞的同时,触发了“免疫原性细胞死亡(ICD)”,释放出肿瘤相关抗原,激活了小鼠自身的免疫系统。这就好比在体内进行了一场针对癌细胞的“全网通缉”,让免疫细胞能识别并消灭那些躲藏在远处的残余癌细胞,极大地降低了复发和转移的风险。
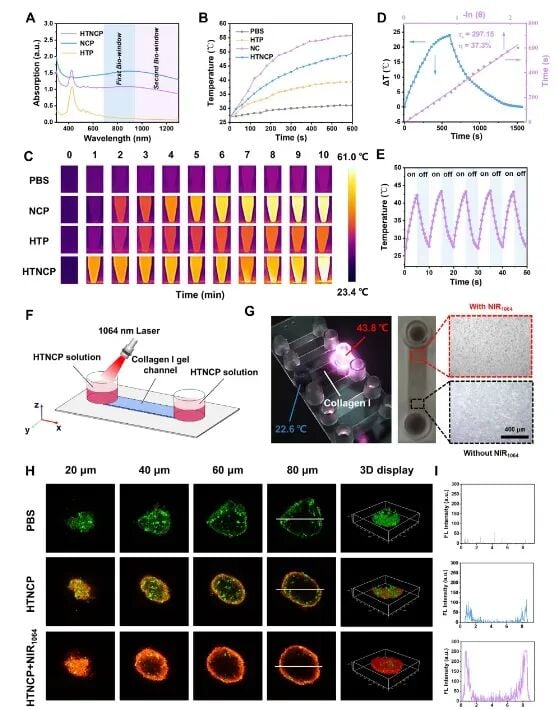
HTNCP显著提升了药物在肿瘤组织中的渗透深度
居家管理与科普建议:放疗期间如何守护生活质量
虽然HTNCP这类前沿技术还在临床前研究阶段,但它所代表的“增敏与保护”理念对正在接受放疗的患者极具指导意义。在放疗过程中,患者常会面临皮肤损伤、乏力、食欲不振等副作用。以下是MedFind主编为您整理的居家管理干货:
- 皮肤护理:放疗区域的皮肤非常脆弱,严禁使用肥皂、沐浴露揉搓。应穿宽大棉质内衣,避免摩擦。若出现红斑或轻微脱皮,可在医生指导下使用专门的放射防护喷雾或软膏。
- 基质管理(饮食建议):虽然我们不能像纳米机器人一样精准降解基质,但通过补充优质蛋白、维生素C等营养素,可以帮助正常组织修复,提高机体对放疗的耐受力。
- 心理调节:放疗的恐惧往往来源于“未知”。了解像HTNCP这样不断进步的科技,能帮助患者建立必胜信心。记住,现在的放疗正变得越来越精准、痛苦越来越小。
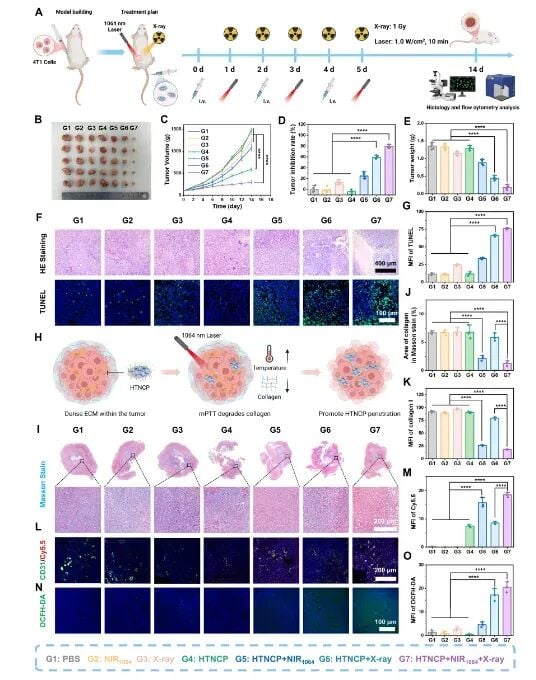
疗效验证:序贯治疗诱导产生强烈的免疫激活效应
总结与希望
中国医学科学院放射所的这项研究,通过巧妙的材料设计,解决了放疗“渗透难”和“剂量高”的两大痛点。这不仅为三阴性乳腺癌的治疗提供了新的思路,也为未来多功能序贯治疗平台的构建开辟了道路。目前,该研究已发表于顶级学术期刊《Advanced Materials》。
对于广大患者而言,科技的进步就是生命的希望。虽然从实验室走向临床还需要时间,但全球范围内类似的创新疗法、新型靶向药物和免疫疗法正在加速获批。MedFind作为您的抗癌信息伙伴,始终致力于打破这种“信息不对称”。如果您正在寻求全球范围内最新的放疗增敏药物、前沿的PD-1/L1抑制剂,或者希望通过“跨境直邮服务”获取国内尚未上市的创新药品,MedFind的专业团队将为您提供全方位的支持。同时,我们的AI辅助问诊系统可以为您解读复杂的检查报告,助您在治疗决策中更有底气。抗癌路上,您并不孤单,让我们一起期待更多如HTNCP般的“黑科技”早日造福临床。
参考信息
Li, Y., Yang, L., Liu, J., et al. (2025). A Stepwise-Enhanced Schottky Heterojunction Enables Ultra-Low-Dose Radiodynamic Therapy via Matrix Remodeling and Electron–Hole Separation. Advanced Materials. DOI: 10.1002/adma.202521580.