胰腺癌一直以来被医学界公认为“癌中之王”,其隐匿性高、进展快且极易产生耐药性,令无数患者和家属感到绝望。许多患者在初次化疗时效果尚可,但很快肿瘤就会卷土重来。近日,顶级学术期刊《Cell》发表的一项突破性研究,终于为我们揭开了胰腺癌这种“不死之身”背后的生物学机制。研究发现,胰腺癌细胞竟然拥有一种类似“生存开关”的本领,能够根据周围环境的变化,在“疯狂生长”与“休眠躲避”之间灵活切换。
癌中之王的秘密武器:能屈能伸的“生存智慧”
为什么化疗药物往往难以彻底清除胰腺癌?这篇由纽约大学朗格尼医学中心领导的研究指出,答案藏在胰腺癌细胞的“环境感知能力”中。在肿瘤组织内,癌细胞并非孤立存在,它们被一种称为细胞外基质(ECM)的纤维组织紧紧包裹。这些纤维就像是癌细胞赖以生存的“土壤”。
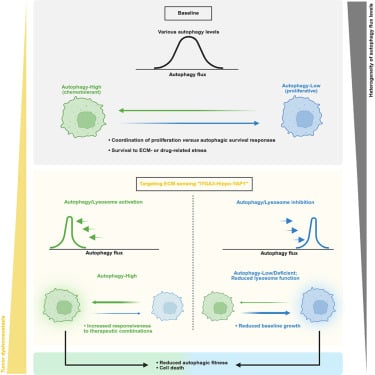
研究人员发现,胰腺癌细胞通过其表面的整合素亚基α3蛋白质,能够像雷达一样探测周围的ECM纤维。当癌细胞紧贴着这些纤维时,它们感到安全,于是开启“生长模式”,疯狂地分裂和增殖。然而,当癌细胞远离这些纤维,或者环境变得恶劣时,它们会立刻切换到另一种状态——自噬(Autophagy)。
自噬:癌细胞的“辟谷生存法”
所谓自噬,字面意思就是“自我进食”。在这种状态下,癌细胞会主动分解自身的非核心成分,将其转化为维持生命所需的营养物质。更重要的是,处于自噬状态的癌细胞会停止分裂。由于大多数化疗药物(如吉西他滨或白蛋白紫杉醇)的原理是攻击快速分裂的细胞,这些“休眠”中的、正在“辟谷”的癌细胞就能完美地躲过化疗的杀伤,从而形成耐药性。

这一发现极大地解释了为什么单一治疗方案往往难以奏效。在同一个胰腺肿瘤内部,其实存在着两群截然不同的癌细胞:一群在积极生长,另一群则在自噬潜伏。这种高度的异质性,让传统的“一刀切”疗法顾此失彼。
羟氯喹:老药新用,能否打破胰腺癌的僵局?
既然自噬是癌细胞的避风港,那么如果我们封死这个避风港,是否就能提高疗效?研究人员将目光投向了目前唯一获得FDA批准的自噬阻断剂——羟氯喹(赛能, Hydroxychloroquine)。
在过去的临床尝试中,羟氯喹作为单一药物治疗胰腺癌的效果并不理想。通过本次研究,科学家找到了原因:因为在自然状态下,并不是所有的癌细胞都在进行高水平的自噬。然而,当研究人员通过基因手段抑制了癌细胞的“传感器”——整合素α3时,奇迹发生了:几乎所有的癌细胞都被迫进入了“高自噬模式”。
这时,再联用羟氯喹进行攻击,杀伤效果显著提升。实验数据显示,这种联合策略导致癌细胞的存活率比单独使用羟氯喹降低了50%。这意味着,如果我们能通过药物精准地将癌细胞逼入自噬死角,再用羟氯喹封喉,胰腺癌的治疗格局将发生翻天覆地的变化。
寻找突破口:NF2蛋白与溶酶体的新靶点
除了整合素α3,研究团队还发现了另一个关键角色——NF2蛋白。NF2负责在细胞内传递环境信号。当研究人员敲除NF2后,癌细胞内部的溶酶体功能受损,导致自噬过程无法完成,癌细胞最终因无法获取能量而死亡。这一发现为未来的新药研发指明了方向:同时靶向ECM感知路径和溶酶体功能,可能会带来比传统化疗更持久的抗肿瘤反应。
临床指标解读:什么是患者的“救命数据”?
对于患者家属来说,这些前沿研究最终都会转化为临床试验中的核心数据:
1. 无进展生存期(PFS):指的是从治疗开始到肿瘤再次长大的时间。通过阻断自噬,我们有望显著延长PFS。
2. 总生存期(OS):即患者的总寿命。破解耐药性是提升OS的关键。
3. 客观缓解率(ORR):肿瘤缩小的比例。联合用药有望让原本对化疗不敏感的肿瘤产生缓解。
给患者及家属的行动建议
面对“癌中之王”,我们不能仅寄希望于传统方案的重复,更需要关注前沿资讯和全球同步的诊疗手段。作为深耕抗癌领域的平台,MedFind 始终致力于消除医疗信息差,为患者寻找那一线生机。
1. 关注联合治疗方案:目前羟氯喹在胰腺癌中的应用多处于临床研究或特定方案联用阶段。若常规化疗效果不佳,建议咨询主治医生,评估是否可以加入自噬抑制剂或其他靶向药物。
2. 重视药物获取渠道:前沿靶向药物和原研药物的获取往往存在时差。患者可以通过合法的跨境直邮渠道,确保用药的及时性与精准性。
3. 副作用居家管理:如果正在使用羟氯喹,需要注意其可能带来的眼底毒性(长期使用)以及胃肠道反应。定期进行眼科检查和血常规监测是必要的。
4. AI辅助问诊与方案解读:现代医学发展迅速,家属可以利用AI工具对复杂的基因检测报告或病理报告进行深度解读,从而在与医生沟通时更有针对性。
胰腺癌的治疗正在步入“精准感知、精准打击”的新时代。虽然前路艰辛,但随着像《Cell》所报道的这类研究不断涌现,我们手中的“武器库”正在变得越来越强大。科学每前进一步,患者的希望就增加一分。不要放弃,每一个新发现都可能是通往治愈的阶梯。
参考文献
Mohamad Assi et al, Extracellular matrix sensing regulates intratumoral heterogenity of autophagic flux, Cell (2026). DOI: 10.1016/j.cell.2025.12.053.





