透明细胞肾细胞癌(ccRCC)是肾癌中最常见也最棘手的一种,许多患者在接受靶向药物舒尼替尼治疗后,会面临药物耐药的困境,使得治疗效果大打折扣。面对这一难题,首都医科大学贺俊崎教授团队近期在国际顶尖学术期刊《Advanced Science》上发表了一项突破性研究,揭示了肾癌耐药背后一个神秘的“脂肪开关”——PDZK1-ULK1轴。这项发现不仅有望帮助我们理解为何癌细胞会对药物产生抵抗,更指出了通过激活ULK1来逆转舒尼替尼耐药的新策略,为无数肾癌患者重燃了治疗的希望。深入了解这一机制,或许能为患者带来更精准、更有效的治疗方案。
透明细胞肾细胞癌(ccRCC):难以逾越的“脂肪”困境?
肾癌是泌尿系统常见的恶性肿瘤之一,在全球范围内,每年有数十万人被诊断出肾癌。其中,透明细胞肾细胞癌(ccRCC)是肾癌中最常见的病理类型,约占所有肾细胞癌病例的75%-80%。与其他癌症类型相比,ccRCC具有独特的生物学行为和代谢特征,这使得其治疗面临特殊的挑战。一个显著的病理特征是,ccRCC细胞内会异常蓄积大量的脂滴(LDs),这些脂滴看起来就像癌细胞自己建造的“能量储备库”。
过去,人们认为脂滴只是被动的脂质储存单元,用于在细胞需要时提供能量。然而,最新的研究颠覆了这一传统观念。现在我们知道,脂滴是高度动态的细胞器,它们与细胞内的各种功能密切相关,例如调节氧化应激、减少内质网(ER)应激,并维持细胞的代谢稳态。在快速增殖的癌细胞中,这些功能被异常增强,以满足其旺盛的代谢需求。脂滴能够帮助癌细胞保持内质网的完整性,清除有害的活性氧(ROS),从而支持癌细胞的存活和生长。因此,脂滴的异常积累,不再是简单的能量储存,而是一种深度参与癌症病理生理过程的关键机制。
具体到ccRCC,脂滴的异常蓄积是癌细胞代谢重编程的重要组成部分。例如,富含胆固醇的脂滴能够通过促进肿瘤细胞的增殖和存活来推动ccRCC的进展。此外,由缺氧诱导因子HIF-2α通路调控的脂滴储存,也能够帮助ccRCC细胞维持内质网稳态和细胞活力。这种异常的脂质积累,是由于脂质生物合成增加和脂质分解代谢受损共同作用的结果。其中,脂噬(Lipophagy)作为一种选择性自噬形式,是脂滴降解的关键途径。然而,在ccRCC中,脂噬功能常常发生异常,导致病理性脂滴蓄积,进而显著促进肿瘤进展和治疗耐药,特别是对靶向药物舒尼替尼(Sunitinib)等。
舒尼替尼是一种多靶点酪氨酸激酶抑制剂,通过抑制血管内皮生长因子受体(VEGFR)、血小板源性生长因子受体(PDGFR)等多个靶点,阻断肿瘤血管生成和肿瘤细胞增殖,是晚期ccRCC的一线治疗药物。然而,尽管舒尼替尼初期疗效显著,但许多患者在治疗一段时间后,癌细胞会逐渐对其产生耐药性,导致疾病进展和治疗失败。了解并克服这种耐药性,是当前肾癌治疗领域面临的巨大挑战,也是迫切需要解决的临床问题。
破解耐药谜团:首都医科大学发现“脂肪开关”PDZK1-ULK1轴
面对透明细胞肾细胞癌的耐药困境,首都医科大学贺俊崎教授团队的最新研究为我们带来了新的曙光。他们深入探索了ccRCC中脂滴异常积累以及由此带来的药物耐药背后的分子机制,并在国际顶尖学术期刊《Advanced Science》上发表了一项突破性研究。这项研究论文,题为“PDZK1-ULK1轴通过触发脂噬抑制透明细胞肾细胞癌的肿瘤进展和舒尼替尼耐药”,详细阐述了一个名为“PDZK1-ULK1轴”的调控通路,它就像一个精密的“脂肪开关”,控制着癌细胞内脂滴的积累与清除。
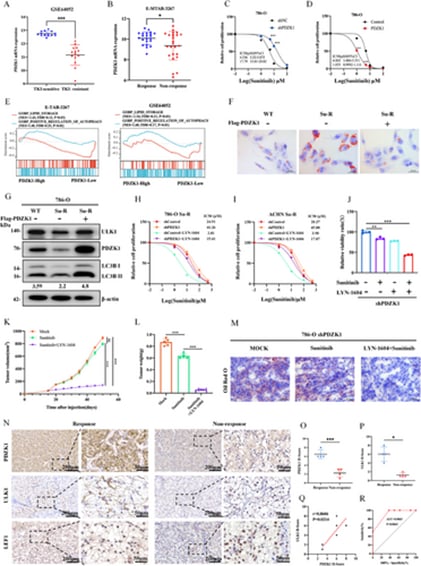
研究首先发现,在ccRCC患者的肿瘤组织中,PDZK1蛋白的表达水平通常显著降低。更重要的是,PDZK1表达的降低与患者体内脂滴的异常积累和不良预后密切相关。这意味着PDZK1在抑制脂滴蓄积和改善患者生存方面发挥着至关重要的作用。通过先进的单细胞RNA测序技术,研究人员进一步证实,PDZK1表达的下调确实导致了ccRCC细胞中脂滴降解能力的严重受损,使得脂滴无法被有效清除。
那么,PDZK1是如何精确地影响脂滴降解的呢?研究揭示,PDZK1能够通过上调ULK1的表达并激活脂噬(Lipophagy)来抑制脂滴的过度蓄积。脂噬是细胞内一种特殊的“自我清理”机制,它专门负责识别、包裹并降解细胞内多余或受损的脂滴。我们可以将ULK1(Unc-51样自噬激活激酶1)理解为这个“脂滴回收站”的关键启动器或“总开关”。当PDZK1水平正常时,ULK1被充分激活,脂噬功能得以高效运作,使得脂滴能够被有效清除,维持细胞内部的代谢平衡。然而,当PDZK1水平降低时,ULK1的活性也随之下降,脂噬功能受损,导致脂滴在癌细胞内大量堆积,最终促进肿瘤的进展和对药物舒尼替尼的耐药性。这一发现提示,PDZK1-ULK1轴有望成为提高舒尼替尼疗效的潜在治疗靶点。

核心机制揭秘:PDZK1如何“指挥”ULK1的“开关”?
为了更深入地理解PDZK1-ULK1轴在微观层面上的运作机制,贺俊崎教授团队进行了精密的分子生物学实验。他们发现,ULK1的基因表达(也就是ULK1蛋白被制造出来的过程)受到一个名为LEF1的转录抑制因子的精确调控。简单来说,LEF1就像一个“看门人”,通常情况下,它会进入细胞核,结合到ULK1基因的启动子区域,从而阻止ULK1基因被“开启”和表达,起到抑制ULK1生成的作用。
然而,PDZK1的出现改变了这种抑制局面。研究证实,PDZK1能够通过其C端的一个特定区域,直接与LEF1相互作用。这种相互作用的结果是,PDZK1能够将LEF1“滞留”在细胞质中,阻止其顺利进入细胞核。由于LEF1无法到达细胞核去执行其抑制ULK1转录的功能,ULK1基因的“刹车”就被巧妙地解除了。这样一来,ULK1的转录得以顺利进行,细胞内ULK1蛋白的表达水平随之显著上调,并进一步激活了细胞的自噬(包括脂噬)活性。这就是PDZK1如何通过间接却高效的方式,解除对ULK1的抑制,使其能够正常发挥清除脂滴的功能。
这项深入的机制研究,不仅为我们清晰地描绘了PDZK1-ULK1轴的分子调控网络,更重要的是,它为我们提供了精准干预的可能性。如果能够找到一种方法,直接针对LEF1或PDZK1与LEF1的相互作用进行调控,从而增强ULK1的活性,就有望成为克服透明细胞肾细胞癌药物耐药性,特别是舒尼替尼耐药性的全新策略。这一发现为开发靶向ULK1的治疗药物奠定了坚实的理论基础。
治疗新策略与预判:激活ULK1重燃舒尼替尼疗效
理论上的发现最终要落实到实际的治疗应用中,才能真正惠及患者。贺俊崎教授团队的进一步研究,将这一理论转化为了令人振奋的实验结果。他们采用了一种名为LYN‑1604的药理学激动剂,这种药物能够特异性地激活ULK1。实验结果表明,在PDZK1表达水平被人工降低的ccRCC细胞中(这种状态模拟了耐药肿瘤的特征),通过使用LYN‑1604激活ULK1,这些细胞对舒尼替尼的敏感性得到了显著恢复。这就像是给原本已经“失灵”的抗癌药重新插上了“电源”,使其能够再次发挥作用,有效抑制癌细胞的生长。
为了验证这一策略在活体内的效果,研究人员在动物异种移植模型中进行了验证。他们将人类ccRCC癌细胞移植到免疫缺陷小鼠体内,形成肿瘤模型,然后对这些小鼠进行治疗。结果发现,LYN‑1604与舒尼替尼联合使用时,展现出了显著的协同作用。这意味着这两种药物共同作用,能够比单一用药更有效地减少肿瘤生长和脂滴蓄积,从而显著抑制肿瘤的进展。这一体内实验结果强有力地支持了“通过激活ULK1靶向PDZK1-ULK1轴是克服舒尼替尼耐药的新策略”的结论,为未来的临床转化提供了坚实的证据。
更令人鼓舞的是,ULK1不仅有望成为潜在的治疗靶点,还有望成为预测舒尼替尼疗效的重要生物标志物。研究人员对临床患者的肿瘤组织数据进行了深入分析,发现肿瘤组织中ULK1的表达水平与舒尼替尼的治疗反应高度相关。通过受试者工作特征(ROC)曲线分析,ULK1作为预测性生物标志物的曲线下面积(AUC)高达0.9063。这意味着,通过检测患者肿瘤组织中ULK1的表达水平,医生可以在患者开始舒尼替尼治疗前,就对治疗效果进行较为准确的预判。例如,ULK1高表达的患者可能对舒尼替尼更敏感,而低表达的患者则可能需要考虑其他治疗方案或联合治疗。这种精准的患者分层策略,有助于避免无效治疗,节省宝贵的治疗时间和金钱,并为患者提供更个性化、更优化的治疗方案。
对于正在积极寻求最新抗癌资讯的患者和家属来说,了解这类前沿研究进展至关重要。例如,通过MedFind这样的信息共享平台,您可以及时获取最新、最权威的药物信息和诊疗指南,并辅助构建安全可靠的跨境购药渠道,以应对国内未上市新药或个体化治疗的需求,从而争取最佳的治疗机会。
展望未来:肾癌治疗的希望与挑战
首都医科大学贺俊崎教授团队的这项突破性研究,无疑为透明细胞肾细胞癌的治疗带来了令人鼓舞的全新希望。他们不仅深刻揭示了PDZK1-ULK1轴在调控脂滴稳态和舒尼替尼耐药中的关键作用,更重要的是,他们提出并通过严谨的实验验证了激活ULK1作为克服耐药的新策略,并且发现了ULK1作为预测性生物标志物的巨大潜力。
这项研究的意义是多方面的:首先,它加深了我们对ccRCC耐药机制的理解,为靶向脂质代谢以对抗肿瘤提供了新的理论依据。其次,它明确指出了ULK1这一关键靶点,为未来抗癌药物的研发开辟了新的方向。未来,科学家们将可能围绕ULK1,开发出更特异、更有效的ULK1激动剂药物,或者探索将其与现有靶向药物(如舒尼替尼)进行联合使用的最佳方案。这种联合治疗有望在未来显著提高治疗响应率,延长患者的生存期。此外,ULK1作为生物标志物的应用,也预示着肾癌的精准医疗将迈出更大步伐,医生可以根据患者的ULK1表达水平,更科学地制定个性化治疗策略。
对于正在与肾癌抗争的患者和家属而言,这意味着未来可能有更多、更有效的治疗选择和更精准的治疗指导。虽然这项研究目前仍处于基础研究阶段,离真正的临床应用还有一段距离,需要更多大规模的临床试验来验证其安全性和有效性,但它无疑为我们描绘了一幅充满希望的蓝图。我们期待未来的研究能够进一步深化这些发现,并将其尽快转化为临床实践,真正帮助到每一位与肾癌抗争的患者。持续关注这类前沿医学研究,积极与您的主治医生沟通交流,了解最适合您的治疗方案,是患者和家属在抗癌路上不可或缺的一部分。我们坚信,随着医学研究的不断突破和转化,肾癌的治疗将迎来更多希望。
参考文献
He J, et al. PDZK1-ULK1 Axis Triggers Lipophagy to Inhibit Tumor Progression and Sunitinib Resistance in Clear Cell Renal Cell Carcinoma. Advanced Science. 2026 Feb 16. DOI: 10.1002/advs.202511606.