当癌症降临,尤其是对年轻的生命而言,无疑是一场突如其来的风暴。脑胶质瘤,作为常见的颅内肿瘤之一,其复杂性和挑战性让无数家庭陷入困境。然而,随着现代医学的飞速发展,特别是基因检测技术的突破,我们正逐步迈向精准治疗的新时代。本文将深度解析一个16岁男性患者被诊断为毛细胞型星形细胞瘤的案例,重点关注其KIAA1549-BRAF融合和CDKN2A/B缺失这两项关键分子变异。我们将共同探讨这些基因改变如何影响诊断、预后以及未来的治疗选择,特别是针对性的靶向药物,为面临类似困境的患者和家庭提供一份全面、温暖且专业的指南。了解这些信息,是您和家人做出明智决策的第一步,也是我们共同对抗疾病的信心来源。
脑胶质瘤:一场需精准导航的生命之旅
脑胶质瘤是起源于大脑胶质细胞(这类细胞在大脑中支持神经元功能)的恶性肿瘤,是颅内最常见的原发性肿瘤之一。它种类繁多,从生长缓慢、恶性程度较低的低级别胶质瘤,到进展迅速、极具侵袭性的高级别胶质瘤(如胶质母细胞瘤),每一种都对患者的生命和生活质量构成不同程度的威胁。对于患者和家属来说,初次诊断往往伴随着巨大的不确定和焦虑。常见的症状可能包括持续性头痛、视力障碍、癫痫发作、性格改变或肢体无力,这些症状的出现与肿瘤生长的位置和大小密切相关。诊断过程通常涉及神经影像学检查(如MRI)、神经功能评估,最终通过活检或手术切除的组织进行病理学分析。
幸运的是,随着医学科技的进步,我们不再仅仅依靠传统的病理形态学来判断肿瘤性质,分子病理学检测正成为精准诊断和制定治疗方案的核心支柱。它就像一张详细的地图,指引着我们穿越疾病的迷雾,找到最适合患者的航向。在脑胶质瘤的诊疗过程中,精准的基因检测扮演着越来越重要的角色。正如《中国肿瘤整合诊治指南(CACA)脑胶质瘤》所强调的,胶质瘤的病理诊断必须整合组织学分型和相关的分子标记物。传统的组织病理学只能提供肿瘤的基本形态信息,例如细胞的形状、排列和核分裂活跃度,这些只能给出初步的“画像”。而分子病理学则能深入到基因层面,揭示肿瘤细胞内部更深层次的基因变异特征,这些才是肿瘤真正“身份”和“行为模式”的决定因素。这些变异不仅能帮助医生更准确地进行诊断分型,更重要的是,它们能直接影响患者的预后,并指导靶向治疗方案的选择。对于许多患者而言,这意味着从“大海捞针”到“精准打击”的转变,使治疗策略更具针对性和有效性。
毛细胞型星形细胞瘤(Pilocytic Astrocytoma):儿童和青少年最常见的低级别胶质瘤
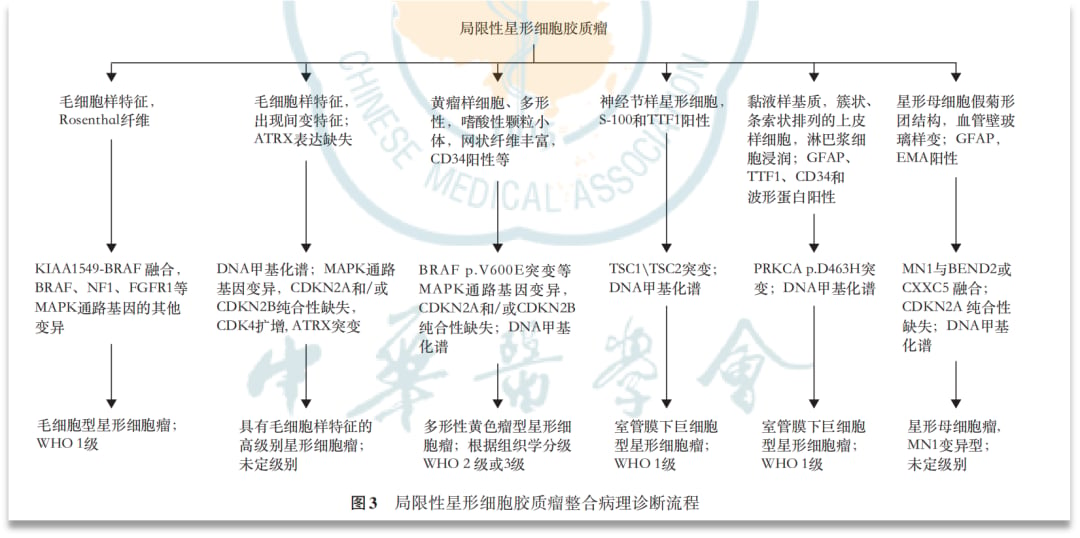
在各类脑胶质瘤中,毛细胞型星形细胞瘤(Pilocytic Astrocytoma,PA)是一个相对特殊的亚型。它通常被归类为WHO 1级肿瘤,属于低级别胶质瘤,这意味着它的生长速度相对缓慢,恶性程度较低,通常边界清晰,不易侵犯周围脑组织。毛细胞型星形细胞瘤约占所有原发性脑肿瘤的5%,是儿童期最常见的胶质瘤,好发于20岁以前的青少年,没有明显的性别差异。这种肿瘤可以发生在脑和脊髓的任何部位,其中最常见的是小脑(占约60%),也可能出现在视神经通路、脑干和大脑半球。由于其生长缓慢的特性,通常预后良好,通过手术切除常能达到治愈的目的。然而,在某些情况下,如果肿瘤位于关键功能区而无法完全切除,或出现复发,这时分子诊断和靶向治疗的重要性就凸显出来。区分低级别胶质瘤(如PA)与高级别胶质瘤(如胶质母细胞瘤)至关重要,因为两者的治疗方案和预后截然不同。精准的分子诊断可以避免对低级别肿瘤患者进行过度治疗,也能防止高级别肿瘤患者错过早期积极治疗的最佳时机。
16岁患者案例解析:KIAA1549-BRAF融合与CDKN2A/B缺失的双重挑战
我们来看一个真实的案例,这名16岁男性患者被诊断为左颞顶低级别胶质瘤,组织学初步考虑为毛细胞型星形细胞瘤。为了进一步确诊并指导后续治疗,医生建议进行分子病理检测。患者送检了肿瘤组织切片和对照血样本,进行了深入的“脑胶质瘤1299基因”检测。这份详细的基因检测报告,揭示了患者肿瘤内部的两个关键分子秘密,这些秘密不仅印证了诊断,更提供了至关重要的治疗线索:

关键发现一:KIAA1549-BRAF融合突变。 报告显示,患者检测出KIAA1549-BRAF融合突变,且变异丰度高达37.88%。这种融合变异被归类为I类临床意义变异,已被明确证实是导致肿瘤发生发展的驱动因素。简单来说,它就像一个“开关”,异常地打开了肿瘤细胞增殖的信号通路,持续不断地刺激肿瘤生长。
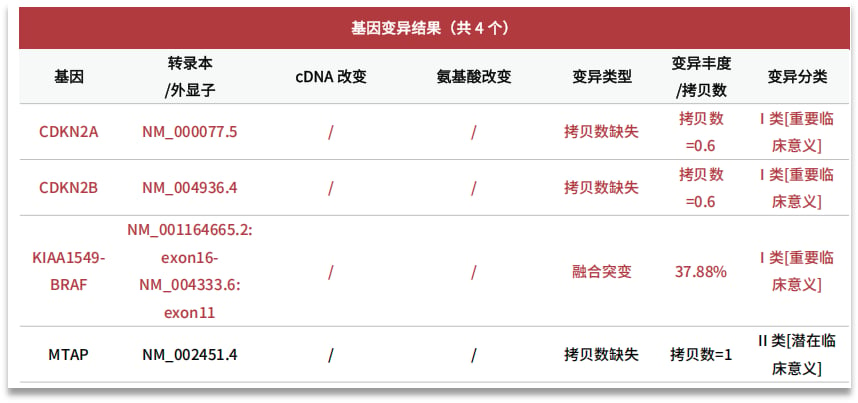
关键发现二:CDKN2A和CDKN2B基因缺失。 除了KIAA1549-BRAF融合,患者还检出了CDKN2A和CDKN2B基因的纯合性缺失。这些基因是重要的肿瘤抑制基因,它们的功能是抑制细胞的异常增殖,就像细胞周期的“刹车片”或“门卫”,确保细胞在正确的时间和地点进行分裂,并在出现问题时启动细胞死亡程序。它们的缺失通常意味着细胞失去了重要的“刹车”功能和“门卫”把关,可能导致肿瘤细胞异常增殖,生长加速,肿瘤细胞更容易无限期地增殖。
解密KIAA1549-BRAF融合:毛细胞型星形细胞瘤的“身份标识”与治疗靶点
要理解KIAA1549-BRAF融合的意义,我们需要先了解BRAF基因。BRAF是MAPK信号通路中的一个关键基因,这条信号通路是细胞内部一条复杂的“信息传递链”,就像工厂里的流水线,负责精确调控细胞的生长、增殖和分化。正常情况下,这条通路是受严格控制的,只有在需要时才会被激活。然而,当BRAF基因发生变异,例如常见的V600E点突变或基因融合时,这条“信息传递链”就会持续被激活,不断地向细胞发出“快生长,快分裂”的错误指令,从而驱动肿瘤细胞的异常增殖、侵袭和转移。
在胶质瘤中,BRAF基因的变异,特别是BRAF V600E突变和基因融合,在毛细胞型星形细胞瘤、胶质神经元肿瘤等类型中较为常见。而患者检出的KIAA1549-BRAF融合,更是一个具有特殊诊断价值的分子变异。所谓“融合基因”,是指两个原本独立的基因,因为染色体结构变异而连接在一起,形成一个新的、功能异常的基因。KIAA1549-BRAF融合就是KIAA1549基因和BRAF基因连接在一起,导致BRAF基因的活性异常升高。专家共识指出,这种融合主要发生在毛细胞型星形细胞瘤中,也可见于弥漫性软脑膜胶质神经元肿瘤以及少量儿童型弥漫性低级别胶质瘤和局限性星形细胞胶质瘤。


《中国肿瘤整合诊治指南(CACA)脑胶质瘤》也明确指出,BRAF融合可在毛细胞型星形细胞瘤、有毛样特征的高级别星形细胞瘤和混合性胶质神经元肿瘤中发现,具有重要的辅助诊断价值。
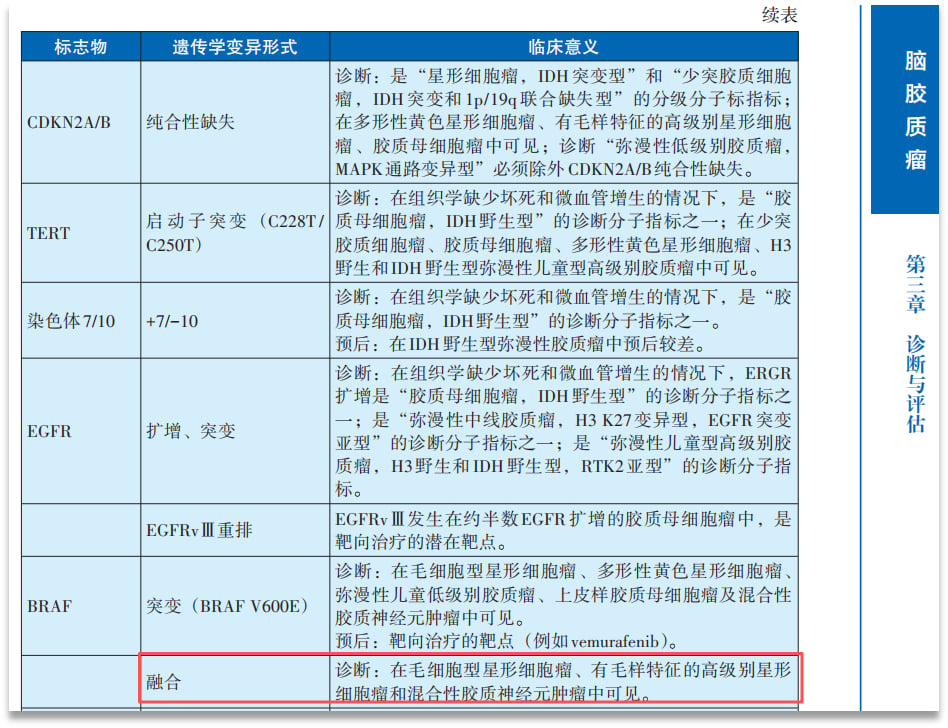
更重要的是,《中国脑胶质瘤分子诊疗指南》提到,KIAA1549-BRAF融合在毛细胞型星形细胞瘤中的发生率很高,高达50%—70%,而在其他级别胶质瘤或其他肿瘤中却很少见。这意味着,KIAA1549-BRAF融合可以被视为毛细胞型星形细胞瘤的一个重要“身份标志”。在组织学上,毛细胞型星形细胞瘤有时会与胶质母细胞瘤(GBM)混淆,因为它们都可能存在微血管增生,形态上难以精确区分。但在分子层面,如果检测到KIAA1549-BRAF融合,则能高度提示为毛细胞型星形细胞瘤,这对于准确诊断和后续治疗方案的制定至关重要,避免了误诊和不必要的治疗。

总结来说,KIAA1549-BRAF融合的检出,不仅从分子层面支持了“毛细胞型星形细胞瘤”的诊断,更重要的是,它为患者的精准治疗提供了明确的靶点,指明了治疗的“方向盘”。
CDKN2A/B基因缺失:隐藏的预后警示与更积极的应对策略
除了BRAF融合,患者还被检出CDKN2A及CDKN2B基因的纯合性缺失。这两个基因被称为“肿瘤抑制基因”,它们的功能是抑制细胞的异常增殖,就像细胞周期的“刹车片”或“门卫”,确保细胞在正确的时间和地点进行分裂,并在出现问题时启动细胞死亡程序。当这些基因发生纯合性缺失(即两个拷贝都丢失)时,细胞就会失去这种重要的“刹车”功能和“门卫”把关,导致细胞增殖失控,加速肿瘤的生长,肿瘤细胞更容易无限期地增殖。
现有文献研究表明,CDKN2A/B纯合缺失在毛细胞型星形细胞瘤中相对少见(约3.8%),但它的出现往往伴随着肿瘤细胞增殖活性升高、生长速度加快,并可能与不良的临床预后相关。在具有毛状细胞特征的高级别星形细胞瘤(HGAP)中,这种缺失更为常见,可能代表着儿童低级别胶质瘤中预后更差的高危亚群。虽然其临床意义仍需更多研究进一步明确,但对于携带该分子特征的患者,临床医生可能会建议采取更积极的手术切除策略,尽可能最大化切除肿瘤,并进行更密切的影像学随访监测,以期及早发现并干预任何复发或进展,从而争取更好的预后。
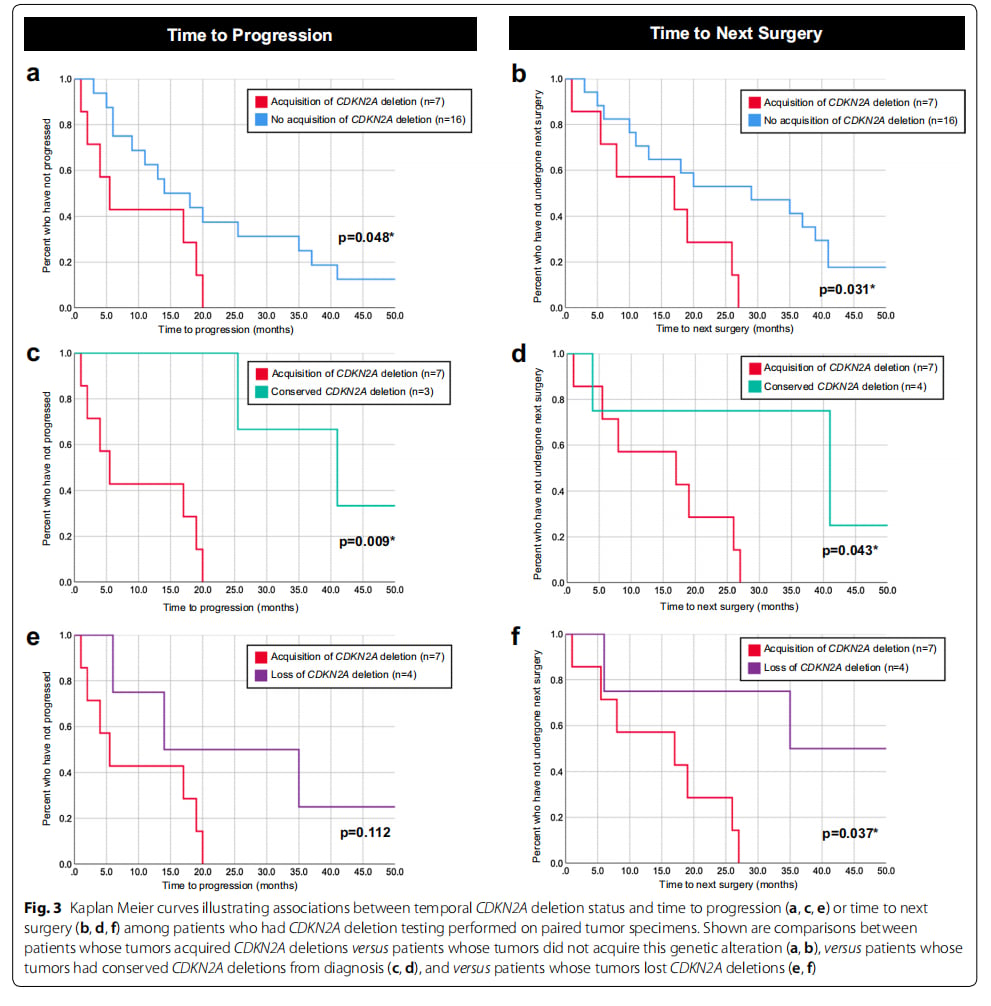
上图(Kaplan–Meier曲线)清晰地显示了CDKN2A缺失对患者无进展生存期(PFS)和再次手术时间的影响。无进展生存期(PFS)指的是患者在接受治疗后,疾病没有出现进展(即肿瘤没有增大或扩散)的时间长度,是评估治疗效果和疾病控制情况的重要指标。从图中可以看出,伴有CDKN2A缺失的患者,其PFS可能相对较短,再次手术的时间也可能更早,这提示了这种基因缺失对预后可能带来的负面影响。这进一步强调了对这类患者进行个性化、积极管理的重要性。
精准治疗的曙光:靶向药物的选择与应用
KIAA1549-BRAF融合的检出,最令人振奋的意义在于它为患者开启了精准靶向治疗的大门。由于这种融合导致MAPK信号通路的持续激活,我们可以通过特定的靶向药物来“关闭”或“减弱”这条异常的信号通路,从而抑制肿瘤的生长。目前,针对BRAF融合的靶向药物主要包括BRAF抑制剂和MEK抑制剂,它们在不同的环节上阻断MAPK通路,达到抗肿瘤的目的,实现对肿瘤细胞的“精准打击”,同时尽量减少对正常细胞的伤害。
托沃拉非尼(Tovorafenib):BRAF融合胶质瘤的新希望
2024年4月,美国FDA批准了托沃拉非尼(Tovorafenib)用于治疗年龄6个月及以上、携带BRAF融合或重排或BRAF V600突变的复发或难治性儿童低级别胶质瘤(LGG)患者。这是医学界的一项重大突破,标志着托沃拉非尼成为首个且唯一一个被FDA批准用于治疗这类疾病的单药疗法,为患儿和家庭带来了巨大的希望。托沃拉非尼作为一种BRAF抑制剂,能够精准地抑制由BRAF融合或突变引起的异常信号,有效阻断MAPK信号通路的过度激活,从而抑制肿瘤细胞的增殖和生存。其在临床试验中展现出显著的客观缓解率(ORR)和持久的缓解时间,意味着很多患者的肿瘤能够缩小或稳定,并且疗效可以维持较长时间。对于本案例中携带KIAA1549-BRAF融合的患者而言,托沃拉非尼无疑是一个非常具有吸引力的治疗选择。

司美替尼(Selumetinib)与曲美替尼(Trametinib):MEK抑制剂的补充作用
除了BRAF抑制剂,MEK抑制剂也是针对MAPK通路的重要靶向药物。它们通过阻断BRAF下游的MEK蛋白,达到相同的抑制通路激活的效果。目前,有两款MEK抑制剂在临床实践中被提及:
- 司美替尼(Selumetinib):《脑胶质瘤靶向和免疫治疗专家共识(2025版)》推荐,对于毛细胞型星形细胞瘤、局限性节细胞胶质瘤/神经胶质瘤/胶质神经元瘤、多形性黄色星形细胞瘤(WHO 2级)等低级别胶质瘤,若存在BRAF融合或V600E激活突变,或NF1突变者,可考虑应用司美替尼。NCCN中枢神经系统肿瘤临床实践指南也指出,对于BRAF融合、BRAF V600突变或NF1突变的患者,司美替尼可作为MEK抑制剂的选择。司美替尼已在部分儿童神经纤维瘤病1型(NF1)相关丛状神经纤维瘤患者中显示出良好疗效,其在BRAF融合胶质瘤中的应用潜力也备受关注。
- 曲美替尼(Trametinib):同样被指南提及,适用于BRAF变异(包括融合或V600突变)的患者。曲美替尼是一种选择性、可逆性MEK1/2抑制剂,能够有效阻断MAPK通路。
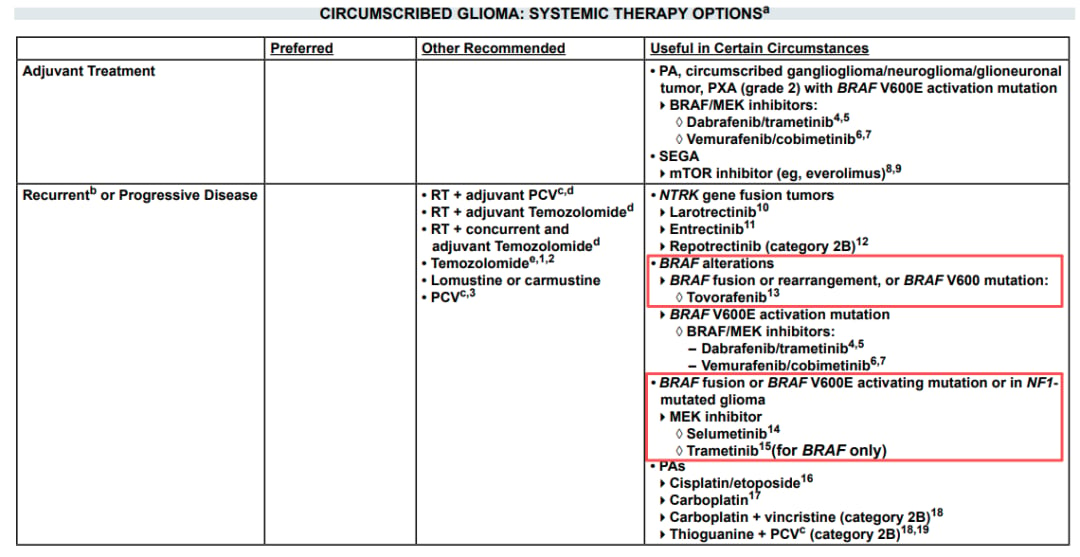
这些靶向药物的选择需要结合患者的具体情况、肿瘤的分子特征、以往的治疗史以及医生的专业判断,进行多学科团队(MDT)的综合评估。MDT团队通常由神经外科医生、肿瘤内科医生、放射科医生、病理科医生、放疗科医生等组成,共同为患者制定最佳的治疗方案。对于携带KIAA1549-BRAF融合的患者,这些MEK/BRAF抑制剂提供了明确的精准治疗方向,从基因层面证实了当前靶向治疗的理论基础和可行性,为患者带来了新的治疗希望。
靶向治疗的常见副作用及管理建议(通用性建议,请务必遵医嘱)
尽管靶向药物相较于传统化疗有更高的选择性和精准性,能够更特异性地作用于肿瘤细胞,但它们仍可能引起一系列副作用。了解并妥善管理这些副作用对于患者保持治疗依从性和生活质量至关重要。患者和家属应积极与医生沟通,详细了解可能的副作用,并在治疗期间密切监测自身状况。常见的BRAF/MEK抑制剂副作用可能包括:
- 皮肤反应:如皮疹(可能像痤疮样或红斑样)、皮肤干燥、指甲变化(如甲沟炎)、光敏感(对阳光敏感)等。建议患者保持皮肤清洁湿润,使用温和的护肤品,避免阳光直射,外出时做好防晒措施。对于严重的皮疹,应及时告知医生,可能需要局部或口服药物进行对症处理。
- 胃肠道反应:如恶心、呕吐、腹泻或便秘等。可尝试少食多餐,选择清淡、易消化的食物,避免辛辣刺激性食物。在医生指导下,可使用止吐或止泻药物。保持充足的水分摄入对于缓解腹泻引起的脱水尤为重要。
- 疲劳:这是一种常见的非特异性副作用,患者可能感到持续的虚弱和精力不足。保持充足的休息,进行适度的轻体力活动(如散步),调整生活节奏,并保持积极乐观的心态有助于缓解疲劳。
- 发热:部分患者可能出现药物引起的发热,有时伴有寒战。应密切监测体温,及时就医排除感染,并在医生指导下使用退热药物。
- 水肿:手足、面部或眼周可能出现肿胀。抬高患肢,避免长时间站立或久坐,避免过咸食物,必要时遵医嘱使用利尿剂。
- 心脏毒性:如心功能下降(射血分数降低)。治疗期间需定期进行心脏功能监测(如超声心动图),以便及时发现并干预。
- 眼部毒性:如视力模糊、视网膜病变(如浆液性视网膜病变)。患者应注意观察视力变化,并定期进行眼科检查,尤其是在治疗初期。
- 肝功能异常:部分患者可能出现肝酶升高。需定期抽血检查肝功能。
请注意:以上仅为一般性建议。每位患者的反应不同,副作用的严重程度也因人而异。务必在医生和药师的指导下进行副作用管理,切勿自行增减药物剂量或中断治疗。当出现新的或加重的症状时,应立即联系您的医疗团队。
跨境购药与MedFind:架起希望的桥梁,触手可及的创新疗法
面对脑胶质瘤这样的复杂疾病,许多创新药物和治疗方案往往首先在欧美等发达国家上市,并被纳入其权威诊疗指南。对于中国患者而言,获取这些新药可能面临时间差、审批流程漫长和高昂价格等多重挑战。当国内尚未引入或药物可及性有限时,跨境购药成为了许多患者寻求生机、不错过最佳治疗时机的途径。
MedFind正是为此而生。作为由癌症患者家属发起的信息共享平台,我们深知每一位患者和家庭在抗癌路上的焦虑与不易。MedFind致力于汇集和分享全球最新的抗癌资讯、前沿诊疗指南和详细的药物信息,帮助患者和家属更好地了解疾病、药物和治疗选择。我们提供的药物信息公正、客观,旨在为患者提供透明的决策依据。
更重要的是,我们协助患者构建安全、可靠、合规的跨境购药渠道,让患者能够及时获取到像托沃拉非尼这样在国外已获批、但国内尚未上市的创新靶向药物。通过MedFind,您可以了解这些药物的最新动态、海外价格参考以及合法的获取方式,大大缩短了药物可及性的“时间差”,让希望不再遥远。我们提供的服务不仅限于抗癌药品跨境直邮,还包括前沿抗癌资讯的持续更新、专业的诊疗指南解读,以及AI辅助问诊服务,旨在为患者提供更全面、更便捷的信息支持和专业的指导。我们承诺,所有信息都将严格遵守医学事实,以通俗易懂的方式呈现,确保您在抗癌路上不再孤单迷茫,能够做出最明智的医疗决策。
展望未来:精准医学点亮生命之光
毛细胞型星形细胞瘤虽然属于低级别胶质瘤,但其分子层面的复杂性,尤其是KIAA1549-BRAF融合和CDKN2A/B缺失的存在,提醒我们必须采取更加精准、个性化的诊疗策略。通过先进的基因检测,我们不仅能够获得更准确的诊断,避免误诊,更能为患者量身定制最有效的治疗方案,甚至预判疾病的进展趋势,从而在疾病发展初期就能积极干预,争取主动权。未来,随着更多靶向药物的研发和上市,以及基因检测技术的不断进步,我们有理由相信,精准医学将为脑胶质瘤患者,特别是像本案例中的年轻患者,带来更长的生存期和更高的生活质量,让他们有更多的时间去体验生命的美好。
对于正在与脑胶质瘤抗争的您或您的家人,请记住,科学与希望同在。积极了解病情,选择权威的基因检测,与医生紧密合作,并寻求像MedFind这样的专业平台支持,您就掌握了战胜疾病的关键。我们坚信,每一次精准的诊断,每一种创新的治疗,都是点亮生命之光的希望。如果您对本文提及的药物或疾病有任何疑问,或需要了解跨境购药渠道,欢迎通过MedFind平台进行咨询,我们将竭诚为您服务,共同迎接更好的未来。