面对癌症,每一次治疗方案的更新都承载着无数患者和家庭的希望。传统的T细胞免疫疗法虽然为许多肿瘤患者带来了生的转机,但在其高效杀伤癌细胞的同时,也常常因为“误伤”正常组织而带来严重的副作用。这种“瘤外靶效应”是当前免疫治疗领域亟待攻克的难题。然而,2025年《Cell》杂志上的一项突破性研究,为我们描绘了一个更安全、更精准的癌症治疗新蓝图——那就是创新性的GlyTR(聚糖依赖性T细胞招募剂)“魔术贴”疗法。这项研究不仅有望解决传统疗法的毒性困境,更可能为多种癌症的治疗打开新的大门。MedFind始终关注全球抗癌前沿资讯,致力于为患者提供最及时、最全面的药物信息和治疗方案,帮助您在抗癌路上少走弯路。
第一章:T细胞免疫治疗:希望与挑战并存
1.1 什么是T细胞免疫治疗?
癌症,是身体细胞“叛变”失控的疾病。而我们的免疫系统,特别是T细胞,是体内对抗这些叛变细胞的“精锐部队”。T细胞免疫治疗,顾名思义,就是通过各种方式增强或引导T细胞去识别并杀死癌细胞。当前最受关注的T细胞免疫疗法主要包括两种:
- 双重特异性抗体(Bispecific Antibodies):这类抗体就像一把“双面胶”,一端能识别癌细胞表面的特定抗原,另一端则能抓住T细胞,把T细胞“拉”到癌细胞旁边,促使T细胞攻击癌细胞。
- CAR-T细胞疗法(Chimeric Antigen Receptor T-cell Therapy):这是一种更复杂的“活药物”疗法。医生会从患者体内抽取T细胞,在体外通过基因工程技术,给这些T细胞装上一个特殊的“导航系统”——嵌合抗原受体(CAR)。这个“导航系统”能精准识别癌细胞,被改造后的CAR-T细胞再输回患者体内,就能像“精确制导导弹”一样,直奔癌细胞并将其消灭。
这些疗法在白血病、淋巴瘤等血液系统肿瘤中取得了令人振奋的成果,让许多原本无药可治的患者获得了长期缓解甚至治愈。
1.2 “双刃剑”的困境:为何精准是关键?
尽管T细胞免疫治疗前景广阔,但它也像一把“双刃剑”,在带来希望的同时,也伴随着不小的挑战。其中最突出的就是“瘤外靶效应(on target, off cancer)”毒性。这是什么意思呢?
想象一下,癌细胞表面有一些独特的“标志”或“身份牌”(医学上称为抗原),免疫疗法就是通过识别这些“身份牌”来锁定癌细胞。然而,问题在于,许多癌细胞上的“身份牌”并非癌细胞独有,正常细胞上也可能少量存在,只是浓度比较低。传统的T细胞免疫疗法(特别是高亲和力的抗体)在识别癌细胞时,往往会因为其超高的结合能力,不小心也识别并攻击了正常组织中那些低表达相同“身份牌”的细胞。这就好比,警察要抓一个穿红衣服的罪犯,但因为警察的“识别灵敏度”太高,连街上穿粉红色衣服的好人都一起抓了,造成了不必要的伤害。
这种“误伤”可能导致各种严重的副作用,例如:
- 神经毒性:如细胞因子释放综合征(CRS)导致的脑水肿、意识障碍等。
- 心脏毒性:对心肌细胞的损伤。
- 肝肾功能损害:影响重要脏器的正常运作。
- 骨髓抑制:导致白细胞、红细胞和血小板减少。
为了避免这些毒性,科学家们一直在苦苦寻找一种理想的“身份牌”——它要么只存在于肿瘤细胞上,要么虽然也存在于正常细胞,但在正常细胞上的表达量极低,而癌细胞上却高表达,并且这些正常组织不是人体维持生命的关键器官。这项寻找工作,正是当前肿瘤免疫治疗领域最核心的难题之一。
第二章:揭秘肿瘤的“糖衣炮弹”:肿瘤相关糖抗原(TACAs)
2.1 癌症细胞表面的特殊“身份证”
除了蛋白质,“癌细胞的表面”其实还穿着一层特殊的“糖衣”——由各种糖类复合物组成的,我们称之为“肿瘤相关糖类抗原(tumor-associated carbohydrate antigens, TACAs)”。你可能想不到,这些糖类抗原在癌细胞的身份识别中扮演着非常重要的角色。
为什么说TACAs特殊呢?
- 普遍性:几乎所有的肿瘤细胞表面蛋白都存在糖基化修饰,这意味着TACA几乎存在于所有癌细胞的表面。
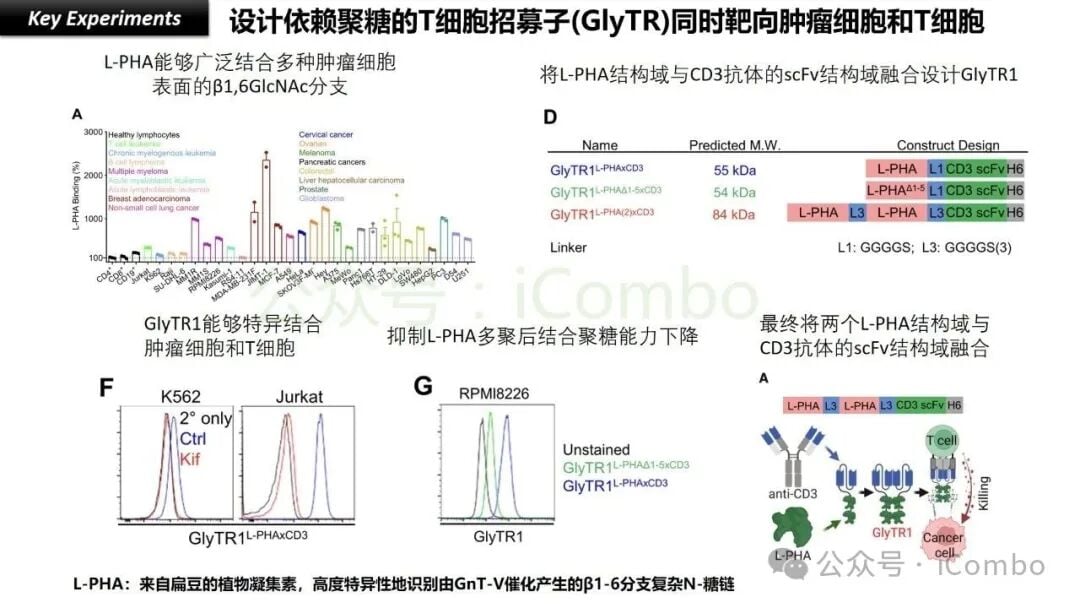
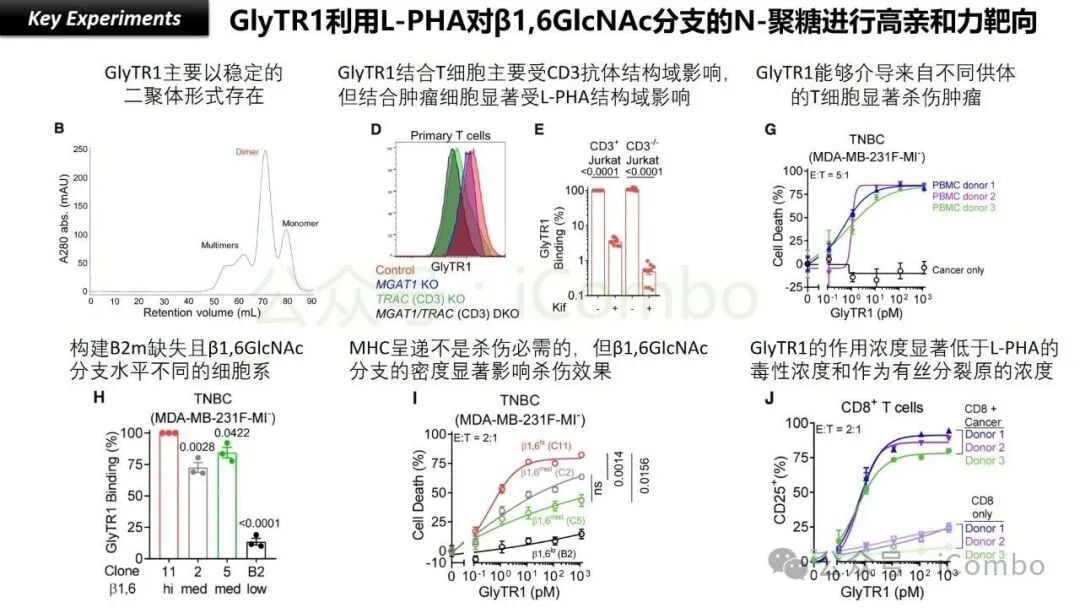
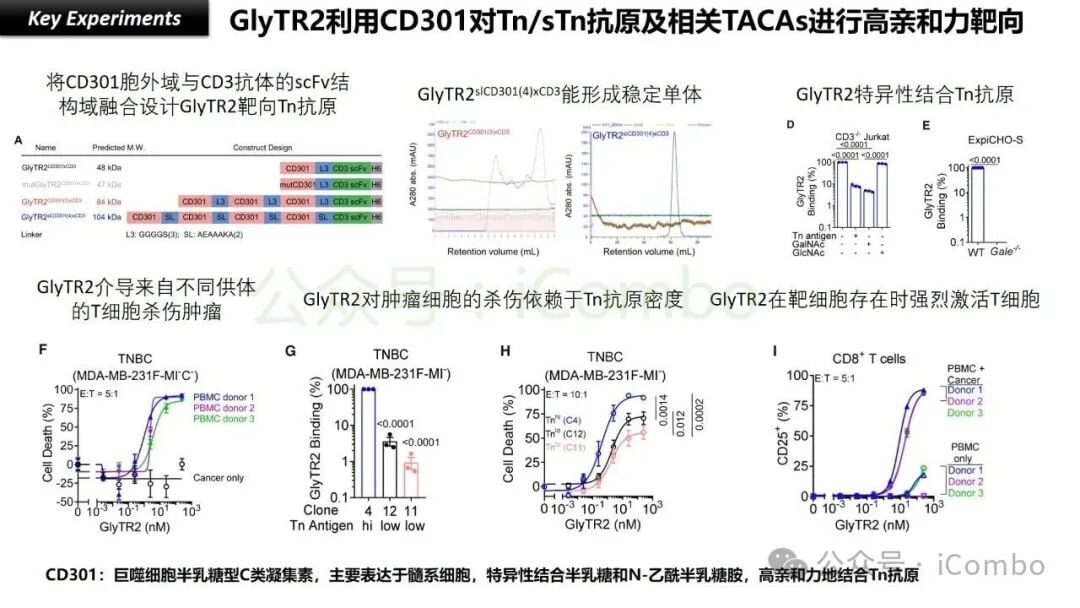
- 高丰度:与传统的蛋白质抗原相比,TACAs的丰度可能高出1000到10000倍!这就像癌细胞表面密密麻麻地贴满了某种特殊的“糖类贴纸”,数量惊人。例如,像β1,6GlcNAc branched N-glycans和Tn抗原,这两种糖类抗原在大多数肿瘤中都高表达,而且它们的出现往往预示着肿瘤的恶性程度更高,能够促进肿瘤的增殖、侵袭和转移。
- 差异性:正常细胞表面虽然也有糖链,但癌细胞往往会异常表达一些特殊的、结构改变的或高密度的糖链,这使得TACAs成为区分癌细胞和正常细胞的潜在“密码”。
正是由于这些特性,TACAs被视为非常有潜力的肿瘤治疗靶点,如果能有效靶向它们,就有可能实现对多种癌症的广谱治疗。
2.2 传统靶向糖抗原的困境:亲和力不足
既然TACAs如此有潜力,为什么之前没有被广泛用于肿瘤免疫治疗呢?问题出在“亲和力”上。
传统抗体,无论是用于诊断还是治疗,都依赖于与靶点之间高亲和力的“锁-钥”式结合,就像一把钥匙精确地插入锁孔。然而,靶向糖类的抗体普遍存在一个致命弱点:它们的亲和力比靶向蛋白的抗体低1000到100000倍!这意味着,传统的抗体很难像“强力胶”一样牢牢地抓住癌细胞表面的糖抗原,导致治疗效果大打折扣。这就好比用一把松动的钥匙去开锁,很难成功。因此,尽管TACAs的丰度很高,但长期以来,由于缺乏有效的靶向工具,它们在肿瘤免疫治疗领域的巨大潜力一直未能被充分挖掘。
第三章:革命性突破:GlyTR“魔术贴”策略如何实现精准打击?
面对传统T细胞免疫治疗的毒性难题和靶向糖抗原的亲和力困境,科学家们从未停止探索。2025年《Cell》杂志发表的一项研究,正是为了解决这些挑战而诞生的突破性创新——“聚糖依赖性T细胞招募剂(Glycan-dependent T cell Recruiter, GlyTR)”。
3.1 GlyTR:从“锁-钥”到“魔术贴”的飞跃
传统的抗体结合模式是“锁-钥”式的,追求的是单个“锁”与单个“钥”之间极高的亲和力。而GlyTR则抛弃了这种思路,开辟了一条全新的道路——它采用了类似“魔术贴(velcro-like)”的结合策略。
什么是“魔术贴”策略?
- 多点微弱结合:魔术贴并非依靠单个钩子与单个毛圈的强力结合,而是通过成千上万个微小的钩子和毛圈的弱结合,最终形成一个整体上非常牢固的连接。
- 整体效应:GlyTR正是借鉴了这一原理。它不再追求单个分子与单个糖抗原的超高亲和力,而是设计成一个能够同时与癌细胞表面多个TACA进行多点、多价(multiple weak interactions)结合的分子。单个结合可能不强,但当这些微弱的结合点数量足够多时,就能产生极强的整体粘附力。
这种创新性的设计,巧妙地绕过了传统靶向糖类抗体亲和力不足的难题,让GlyTR能够像强力魔术贴一样,牢牢地粘附在癌细胞表面。这标志着肿瘤免疫治疗从追求“超强结合”到利用“协同效应”的理念飞跃。

3.2 “密度依赖性”识别:只攻击癌细胞的秘密
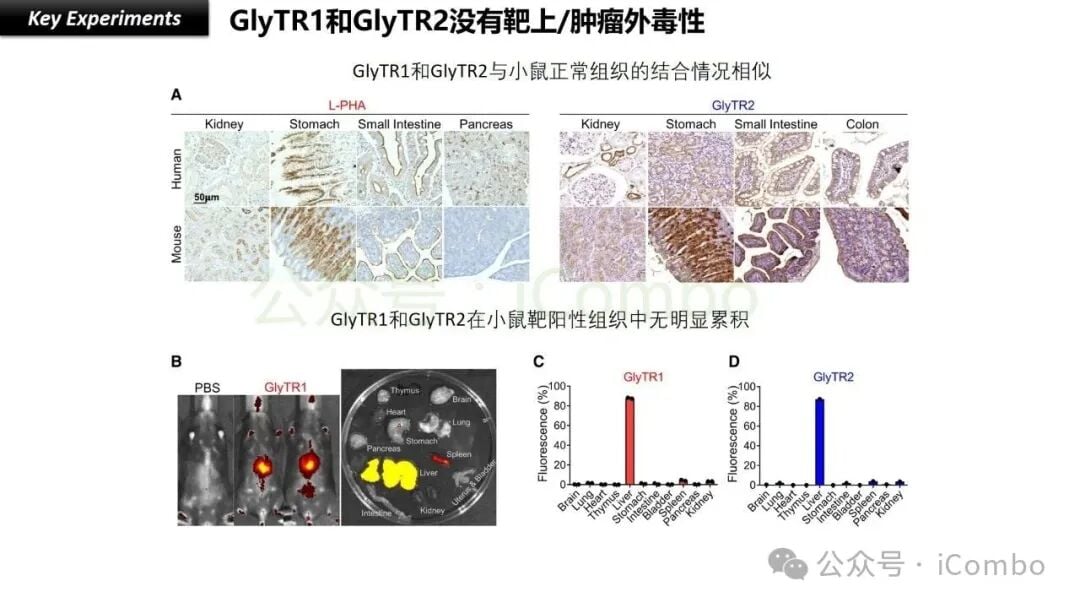
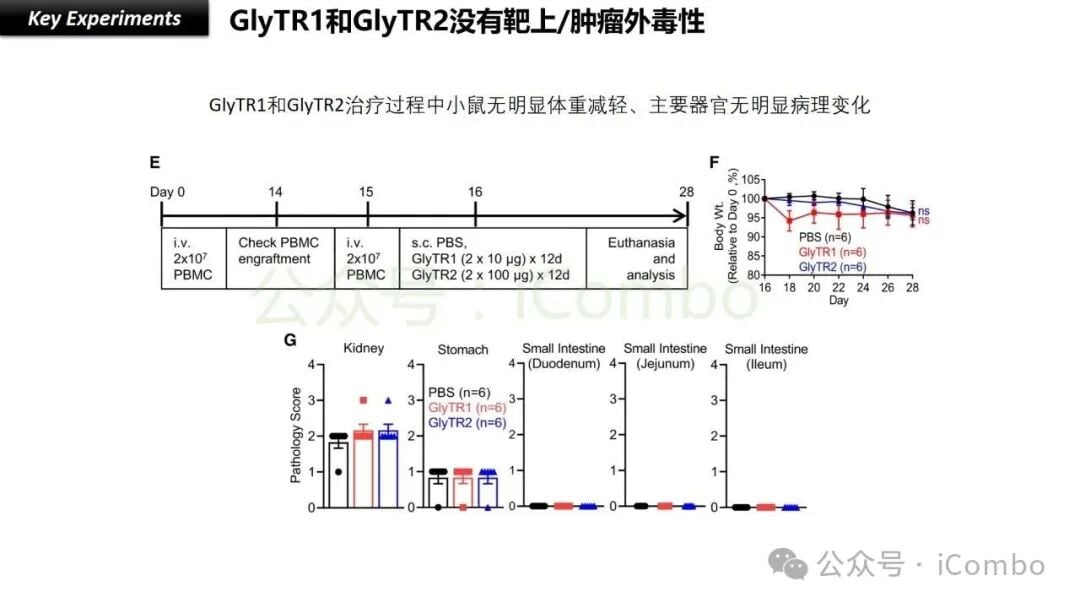
GlyTR的“魔术贴”策略不仅仅解决了亲和力问题,更关键的是,它还完美地解决了“瘤外靶效应”的毒性难题,实现了对癌细胞的“密度依赖性识别”。这是GlyTR最核心的优势之一。
还记得我们前面提到的吗?许多癌细胞表面的糖抗原(TACAs)在正常细胞上也可能少量存在。传统高亲和力的抗体无法区分“少量”和“大量”,导致误伤。而GlyTR的“魔术贴”特性,让它能够聪明地只识别那些“糖链密度”非常高的癌细胞,而忽略正常细胞表面低密度的糖链。
- 癌细胞:高密度“糖衣”:癌细胞为了快速增殖和转移,其表面的TACAs往往会异常地高表达,就像穿上了一层密不透风的“糖衣”,其密度远超正常细胞。
- 正常细胞:低密度“糖链”:正常细胞表面虽然也有糖链,但其密度相对较低。
GlyTR的多个结合点只有在接触到高密度的糖链时,才能同时发生足够的微弱结合,从而产生强大的整体粘附力,像魔术贴一样牢牢“粘住”癌细胞。而当它遇到正常细胞表面的低密度糖链时,由于无法形成足够数量的多点结合,就无法有效粘附。这就好比,一块魔术贴只能粘住毛茸茸的表面,而光滑的表面则无能为力。
这种精妙的“密度依赖性”识别机制,确保了GlyTR能够高度特异性地靶向癌细胞,从而极大地降低了对正常组织的伤害,有望实现更低的毒性和更高的安全性。这项技术被称为“Safe immunosuppression-resistant pan-cancer immunotherapeutics by velcro-like density-dependent targeting of tumor-associated carbohydrate antigens”,其核心就在于这个“魔术贴”般的结合原理。

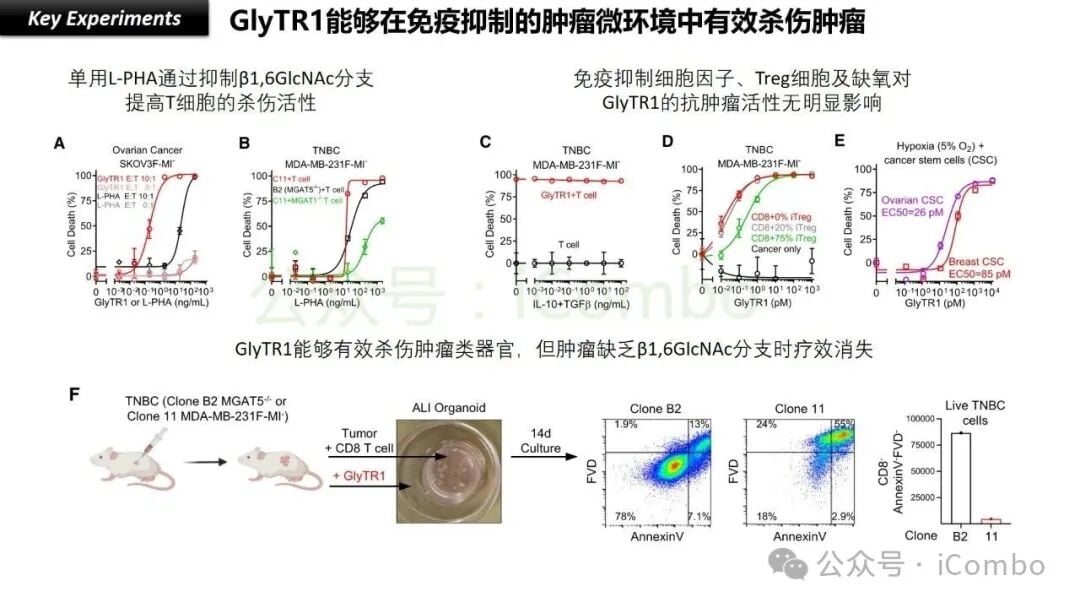
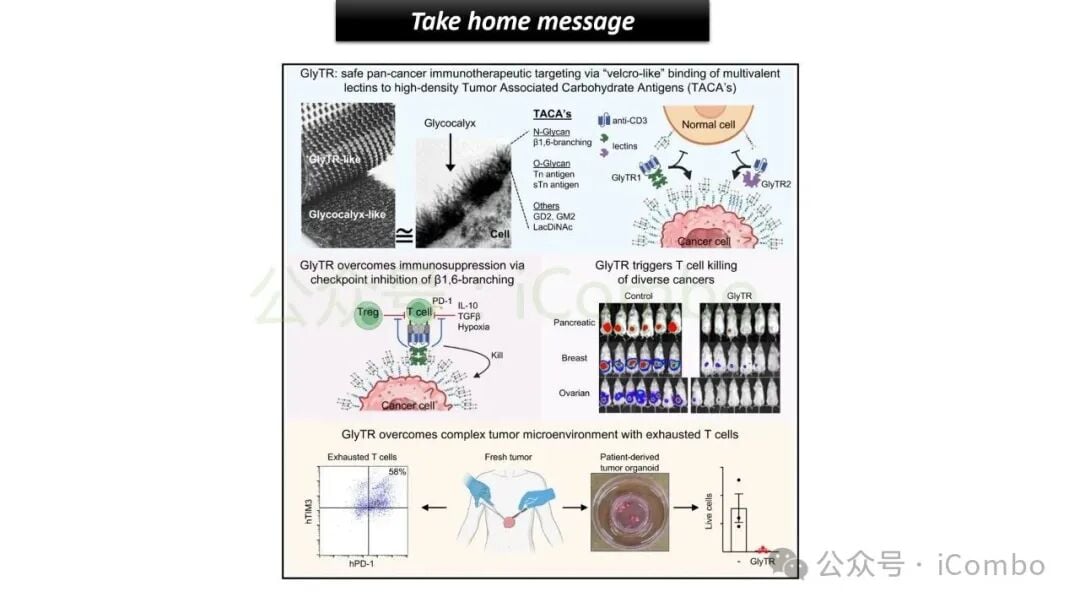
3.3 激活“疲惫”的T细胞:克服免疫抑制微环境
除了精准识别癌细胞,GlyTR还有一个更令人兴奋的能力:它能克服肿瘤的免疫抑制微环境,让那些“疲惫不堪”的T细胞重新恢复活力。
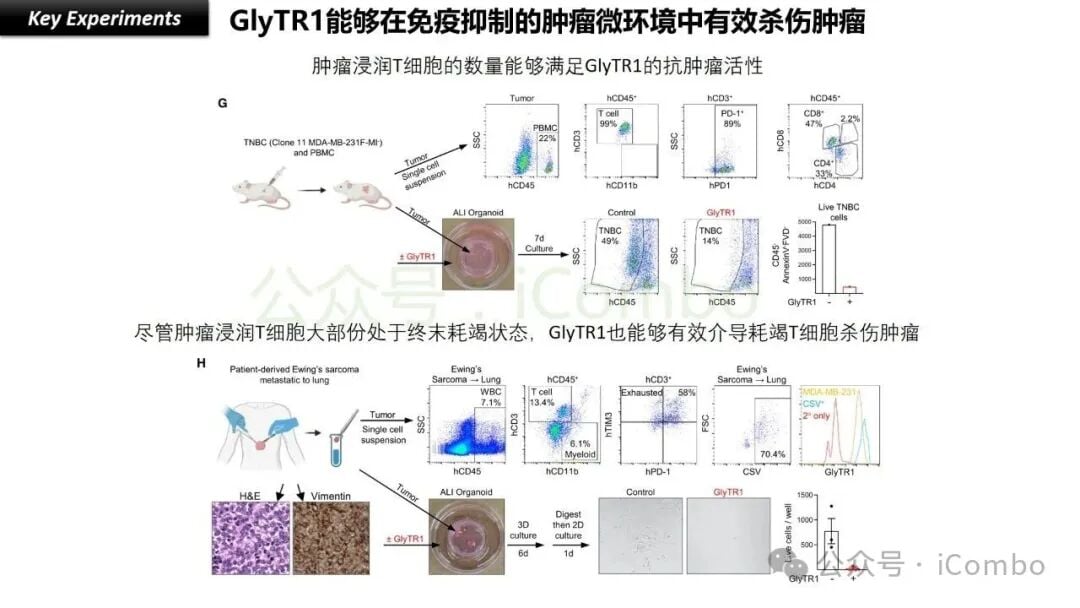
肿瘤的生长和扩散,往往会创建一个对免疫细胞不友好的微环境。在这个环境中,T细胞长期受到抑制,变得“筋疲力尽”(医学上称为“耗竭状态”),无法有效杀伤癌细胞。这也是许多免疫检查点抑制剂(如PD-1/PD-L1抑制剂)面临的挑战之一——部分患者的T细胞已经严重耗竭,即使解除了“刹车”,也无法重新启动“油门”。
研究表明,GlyTR不仅能将T细胞招募到肿瘤细胞旁边,更重要的是,它似乎还能重新激活这些处于耗竭状态的T细胞,让它们恢复杀伤功能。这意味着:
- 突破免疫抑制:GlyTR有望突破肿瘤的“免疫屏障”,即使在肿瘤内部环境恶劣的情况下,也能重新唤醒T细胞的抗癌能力。
- 扩大治疗人群:对于那些因T细胞耗竭而对现有免疫疗法响应不佳的患者,GlyTR可能提供一个全新的治疗选择。
这项多重优势的结合,使得GlyTR不仅仅是一个精准的靶向工具,更是一个能全面提升抗肿瘤免疫反应的革命性分子。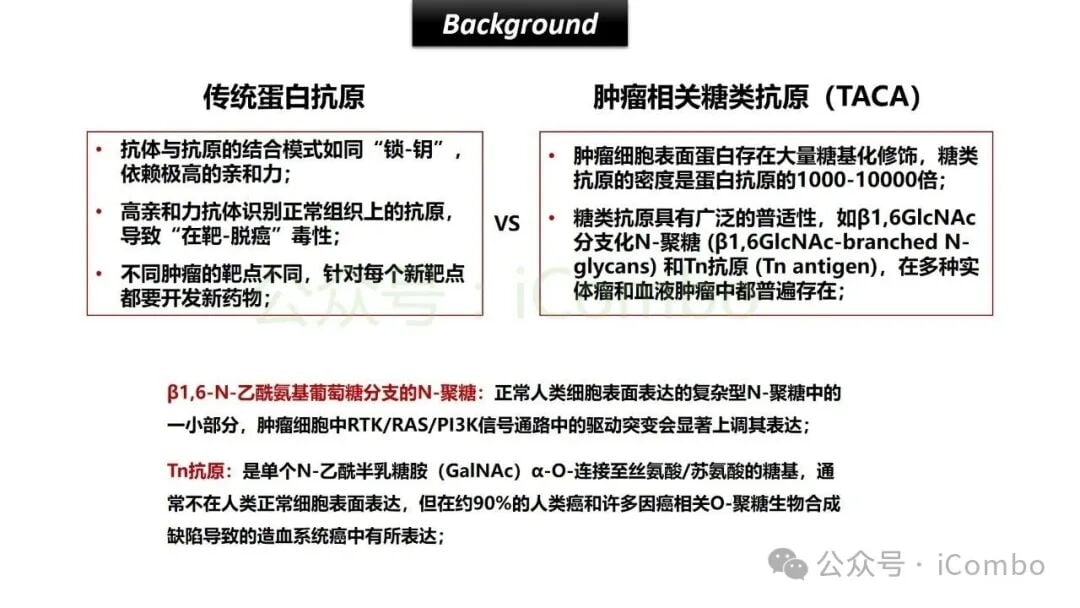




第四章:GlyTR的广阔前景:泛癌种治疗与未来展望
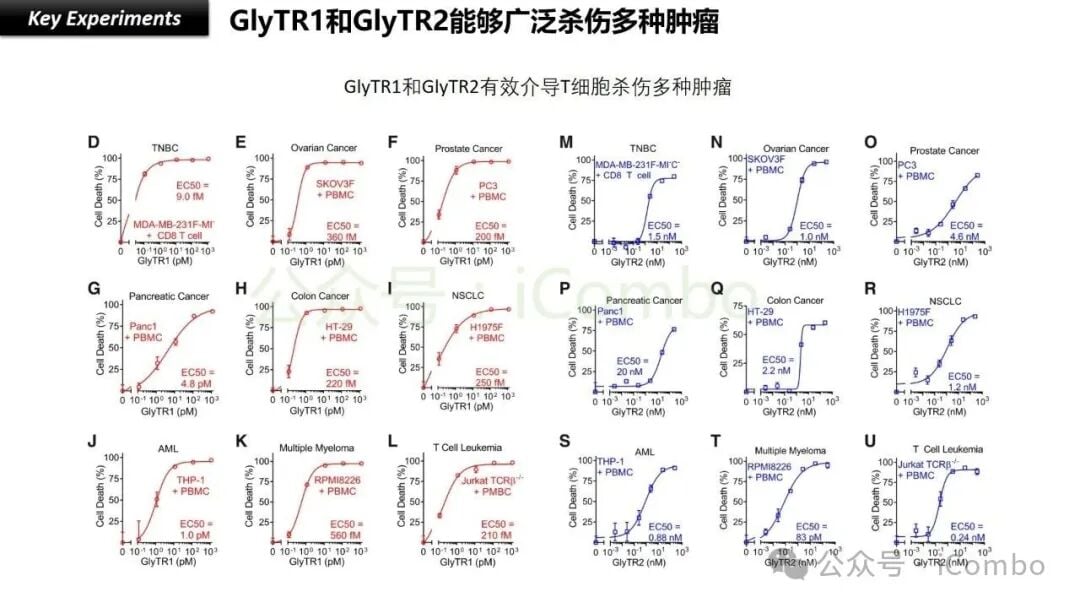
4.1 泛癌种治疗的巨大潜力
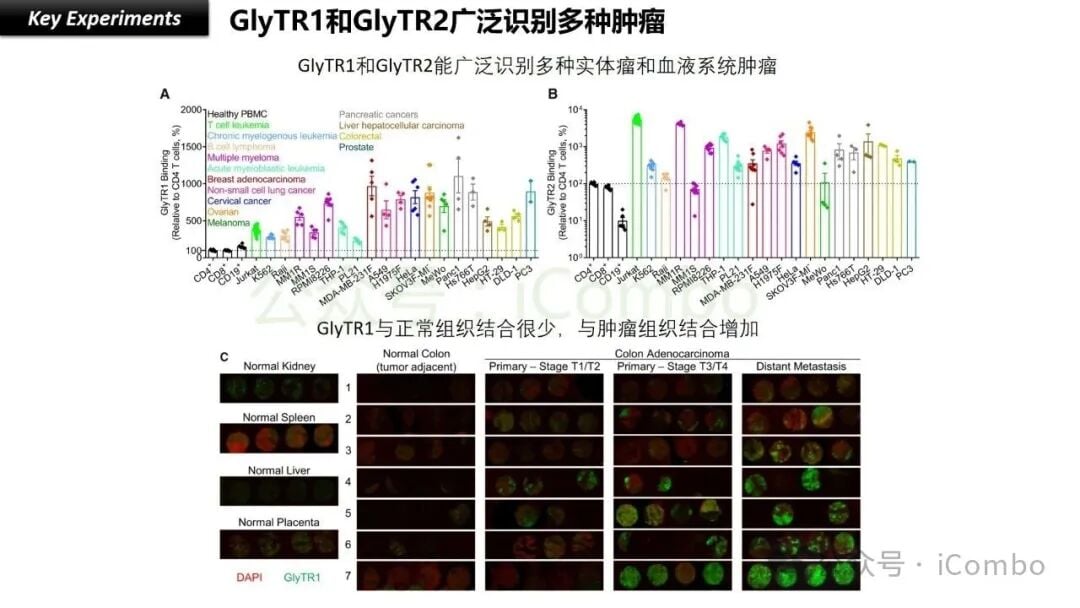
GlyTR的“魔术贴”策略之所以备受瞩目,更在于其泛癌种治疗的巨大潜力。由于肿瘤相关糖抗原(TACAs)在多种实体瘤中普遍高表达,并且其异常糖基化是癌细胞的共同特征,这意味着GlyTR可能不局限于治疗某种特定类型的癌症,而是有望对多种不同的癌症类型都产生治疗效果。这对于患者来说,无疑是一个令人振奋的消息,因为它可能意味着更多患者能从中受益,甚至有望改变未来癌症治疗的格局。
目前,许多创新药的研发都专注于某一特定癌种或特定基因突变类型,而GlyTR这种基于普遍存在的肿瘤特征进行靶向的设计,使其具有更广泛的适用性。如果后续研究能够证实其在多种癌种中的有效性和安全性,那么GlyTR有望成为一种真正的“广谱抗癌利器”。
4.2 更安全、更高效的癌症治疗未来
GlyTR的出现,为癌症治疗带来了前所未有的“精准、安全、高效”的可能性:
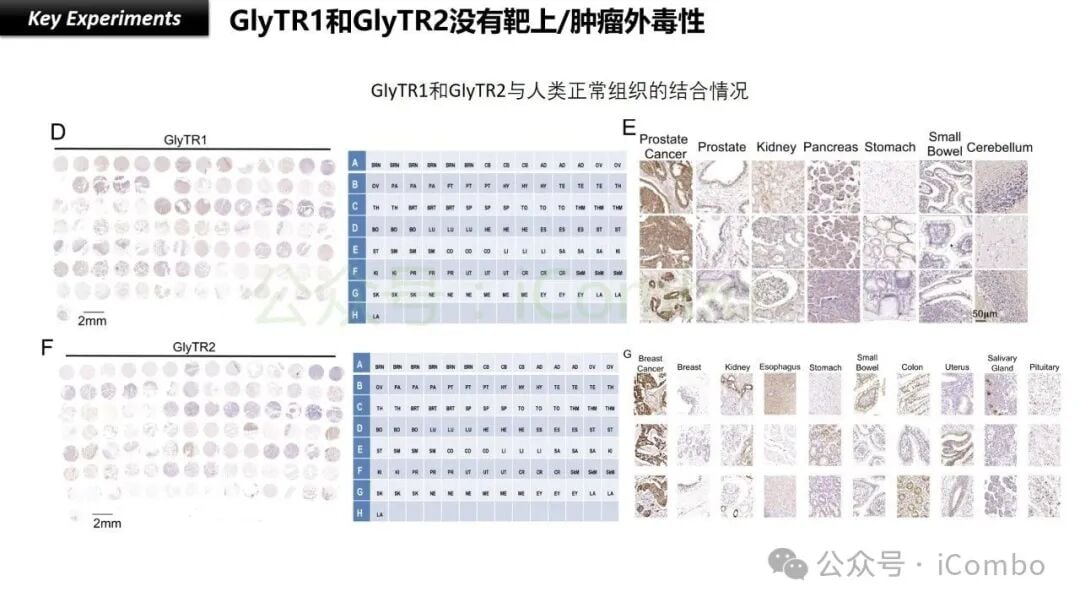
- 安全性提升:通过“密度依赖性”识别机制,GlyTR能够精准区分癌细胞与正常细胞,极大减少“瘤外靶效应”,从而降低治疗带来的毒副作用,提高患者的耐受性和生活质量。
- 疗效增强:不仅能精准靶向,还能有效激活处于耗竭状态的T细胞,有望克服肿瘤的免疫抑制微环境,从而提高治疗的整体疗效,让更多难治性肿瘤患者看到希望。
- 普适性广:泛癌种治疗潜力,意味着它可能适用于更多不同癌症类型、不同基因背景的患者。
这些优势的结合,预示着GlyTR可能引领T细胞免疫治疗进入一个全新的时代,一个更加人性化、更加高效的抗癌时代。
4.3 从研究走向临床:我们还需多久?
尽管GlyTR的研究结果令人鼓舞,这项技术目前仍处于前沿研究阶段,尚未进入临床试验,更未上市成为药物。从实验室的突破到最终惠及患者,通常需要漫长而严谨的研发过程,包括:
- 临床前研究:在细胞和动物模型中进一步验证疗效和安全性。
- I期临床试验:初步在少数患者中评估药物的安全性、剂量和药代动力学。
- II期临床试验:在更多患者中评估药物的有效性和安全性。
- III期临床试验:与现有标准疗法进行对比,大规模验证疗效和安全性。
- 审批上市:获得监管机构批准后才能正式用于临床。
这个过程可能需要数年甚至十几年。因此,我们一方面要对这项科学突破充满信心和期待,另一方面也要保持理性,理解新药研发的复杂性和周期性。MedFind会持续关注GlyTR的后续研究进展,第一时间为您带来最新的消息和解读。
结语:
GlyTR“魔术贴”疗法的诞生,是癌症治疗领域一项里程碑式的突破。它以创新的机制,有望解决困扰T细胞免疫治疗多年的“脱靶毒性”和“T细胞耗竭”难题,为癌症患者带来更加安全、精准、高效的治疗新选择。虽然这项技术距离临床应用尚有时日,但它所展现出的巨大潜力,无疑为无数与癌症抗争的生命点亮了新的希望之光。在未来,MedFind将一如既往地紧密追踪全球最新的抗癌研究与药物进展,为您提供最前沿、最准确的信息。如果您或您的家人正在与癌症搏斗,欢迎随时咨询MedFind,了解最新的治疗方案和药物选择,我们将竭诚为您提供专业的帮助和支持。