对于无数正在与癌症抗争的患者及其家庭而言,“耐药”和“复发”无疑是横亘在希望之路上的两座大山。许多癌症患者在初期治疗效果显著后,肿瘤却像狡猾的敌人,突然变得对药物无动于衷,甚至卷土重来,这不仅让之前的努力付诸东流,更带来巨大的心理和经济压力。每年,全球有数以千万计的生命因癌症而逝去,其中绝大多数实体瘤的死亡,都与这种令人束手无策的耐药性和随之而来的复发转移密切相关。这让科学家们长久以来都在追问:肿瘤为何如此“善变”?我们能否找到它的阿喀琉斯之踵,一劳永逸地解决耐药复发难题?
近日,国际顶级科学期刊《Nature》刊登了一项来自纪念斯隆凯特琳癌症中心等机构的重磅研究,这项研究为我们揭示了癌症耐药与复发背后的一个关键“幕后黑手”——一群被称为“高度可塑性细胞状态”(HPCS)的特殊癌细胞。研究不仅在肺癌小鼠模型中成功锁定了这些“变形军团”,更令人振奋的是,科学家们发现,只要精准清除它们,就能有效遏制肿瘤恶化,防止耐药产生,甚至让已经形成的肿瘤显著缩小。这项里程碑式的发现,为包括肺癌在内的、占所有癌症80%-90%的上皮来源的癌症(即“癌”)开辟了全新的治疗思路,有望从根本上解决困扰已久的耐药与复发难题。MedFind将深入解析这项突破性研究,带您了解癌症治疗的未来走向,并为您的抗癌之路提供最前沿的指引。
癌症耐药与复发:癌友们最深切的痛点
癌症治疗的进展日新月异,靶向治疗和免疫治疗等新疗法为许多患者带来了前所未有的生存希望。然而,一个残酷的现实是,即便最初效果惊人,肿瘤往往会在一段时间后发展出对药物的抵抗力,这就是所谓的“耐药性”。一旦耐药发生,肿瘤会继续生长,甚至转移到身体的其他部位,导致病情恶化,最终走向复发。对于患者而言,这意味着需要不断更换治疗方案,承受更多的副作用,面对更加不确定的未来。
- 耐药的普遍性:无论是化疗还是精准靶向药物,几乎所有的抗癌治疗都面临着耐药的风险。例如,针对EGFR突变的肺癌患者,奥希替尼(点击查看购买渠道与价格)等靶向药初期疗效显著,但多数患者最终仍会因为肿瘤细胞产生新的突变或激活其他信号通路而导致耐药。
- 复发的无情:耐药常常是复发的前兆。一旦肿瘤复发,其恶性程度通常更高,对治疗的反应也更差,给患者带来了身体和心理上的双重打击。
- 现有治疗的困境:目前的策略主要是通过不断研发新的药物,或者尝试多种药物联合使用,以期延缓耐药的发生。但这种“道高一尺魔高一丈”的追赶模式,往往让患者疲惫不堪。我们迫切需要一种能够从根源上解决问题的策略。
那么,肿瘤为何如此“狡猾”,能够一次次地“进化”出耐药机制,逃避药物的追杀呢?答案就藏在肿瘤内部那些极具“可塑性”的细胞中。
揭秘肿瘤的“变形军团”:高度可塑性细胞状态(HPCS)
想象一下,如果把肿瘤比作一个不断扩张的邪恶王国,那么我们过去主要攻击的是它庞大的“常规部队”。但这个王国里,还隐藏着一支数量不多但却极其关键的“特种部队”——它们善于伪装,能随时“变形”改变身份,帮助王国适应各种压力,甚至在受到重创后迅速恢复元气。这就是此次研究发现的“高度可塑性细胞状态”(High-Plasticity Cell State, HPCS)。
HPCS是什么?
在我们的身体里,细胞的“可塑性”原本是一种正常的生理现象。比如,当皮肤受伤时,局部的一些细胞会暂时进入一种“高度可塑”的状态,它们能够快速分化成各种所需细胞类型来修复伤口,这就像是身体自带的“快速修复模式”。这种细胞状态比普通干细胞更“多才多艺”,能够快速响应环境变化。它本是生命体精妙的自我保护和再生机制。
然而,癌细胞却异常“狡猾”,它们“盗用”了这套本该只在组织损伤修复时才激活的程序。研究发现,在肿瘤发展过程中,一小部分癌细胞会“劫持”并进入这种类似损伤修复的HPCS状态。这些HPCS细胞并非肿瘤最初形成所必需,但却是推动肿瘤从良性走向恶性、产生耐药性,乃至发生转移的关键“引擎”。它们虽然数量不多,但却像肿瘤的“战略参谋部”和“进化加速器”,决定着整个肿瘤如何适应治疗压力并持续生存。

HPCS:癌症耐药与复发的“幕后推手”
那么,HPCS具体是如何推动肿瘤恶化和耐药的呢?
- 身份转换:HPCS细胞能够根据环境变化,灵活地改变自身的分子和细胞特征。当肿瘤面临化疗或靶向药的攻击时,大部分癌细胞会死亡,但少数HPCS细胞却能通过“变形”,转换到一种对药物不敏感的状态,从而“躲过一劫”。
- 产生耐药亚群:更重要的是,这些“幸存”的HPCS细胞能够进一步增殖,并产生出对药物具有抵抗力的新型癌细胞。这就导致了肿瘤的耐药性,使得之前的治疗方案失效。
- 促进恶性进展和转移:HPCS不仅与耐药有关,还被发现与肿瘤的侵袭性、转移能力密切相关。它们能够帮助肿瘤细胞逃离原发灶,在身体其他部位建立新的病灶,加速癌症的恶化进程。
理解HPCS的这种“多功能性”和“可塑性”,是破解癌症耐药和复发难题的关键一步。这意味着,仅仅杀死大部分癌细胞是不够的,我们必须找到并剿灭这支“特种部队”,才能真正阻止肿瘤的卷土重来。
纪念斯隆凯特琳的突破性研究:精准锁定与剿灭HPCS
面对HPCS在肿瘤恶化中的核心作用,纪念斯隆凯特琳癌症中心的科学家们开展了一系列创新性研究,旨在不仅要找到这些细胞,更要证明清除它们能够带来显著的治疗效果。他们开发了创新的小鼠肺癌模型,能够特异性地标记、追踪乃至清除HPCS细胞,这种精密的实验设计为我们揭示了HPCS的真面目。
关键发现一:HPCS是肿瘤生长与恶化的“核心发动机”
通过精密的“谱系追踪技术”(想象成给细胞打上“族谱标签”,追踪它们的后代),研究人员亲眼目睹了HPCS细胞在肿瘤内部的“七十二变”:它们不仅能产生早期分化较好的肿瘤细胞,更能衍生出进展期的、恶性程度更高的细胞状态。更重要的是,在已形成的肿瘤中,源自HPCS的细胞比普通肿瘤细胞或其他分化状态的癌细胞生长能力更强,这表明它们是推动肿瘤持续增长和恶化的“核心发动机”。
关键发现二:提前清除HPCS,从源头阻止癌症萌芽
这项研究最令人振奋的发现之一是,如果在肿瘤发生的早期就精准地清除这些高度可塑性细胞,竟然可以从根本上阻止突变细胞发展成癌症。这就像是在邪恶王国刚有萌芽时,就精准消灭了它的领导核心,使其无法组织起有效的“叛乱”。这一发现为癌症的早期干预和预防提供了全新的思路,未来甚至可能针对高危人群开发预防性策略。
关键发现三:清除已形成肿瘤中的HPCS,大幅减瘤并瓦解耐药性
研究人员进一步探索,即使肿瘤已经形成,清除HPCS是否依然有效?他们采用了两种策略:一是使用“自杀基因”技术,让HPCS细胞自行凋亡;二是利用了当下热门的CAR-T细胞技术,设计出能特异性识别并清除HPCS的CAR-T细胞。结果令人鼓舞:当已形成的肿瘤中的HPCS被清除后,肿瘤负荷显著降低,这意味着肿瘤明显缩小。更重要的是,研究发现HPCS细胞会衍生出耐药的细胞状态,而清除HPCS后,肿瘤对化疗和靶向治疗产生耐药的能力被极大抑制。这表明,靶向HPCS有望成为打破肿瘤耐药僵局的“决定性一击”。
HPCS的“阿喀琉斯之踵”:精准打击靶点uPAR蛋白
既然HPCS如此关键,那么如何才能在不伤害正常细胞的前提下,精准地打击它们呢?这项研究找到了一个极具潜力的“阿喀琉斯之踵”——uPAR(尿激酶型纤溶酶原激活物受体)蛋白。
uPAR蛋白:HPCS的“专属标记”
研究团队发现,uPAR蛋白在处于HPCS状态的细胞表面高度富集,而绝大多数正常的健康细胞上却很少出现这种蛋白。这就如同HPCS细胞拥有了一个独特的“身份标识”,为我们提供了精准打击它们的靶点。这种特异性是开发新型抗癌疗法的关键,因为它能最大限度地减少对正常组织的附带损伤。
CAR-T细胞如何利用uPAR精准打击?
研究人员正是利用了uPAR的这一特性,设计了能够识别uPAR蛋白的CAR-T细胞。这些经过基因改造的T细胞就像是“特种兵”,它们能够精准地找到并清除那些带有uPAR标记的HPCS细胞,从而引发强烈的抗肿瘤反应。实验结果再次证明了这种方法的有效性,因为uPAR蛋白只存在于这些具有“修复样程序”的癌细胞中,而非大多数正常的健康细胞。清除它们就相当于切断了肿瘤适应和再生的能力。
HPCS数量与肿瘤进展:晚期癌症更难治的秘密
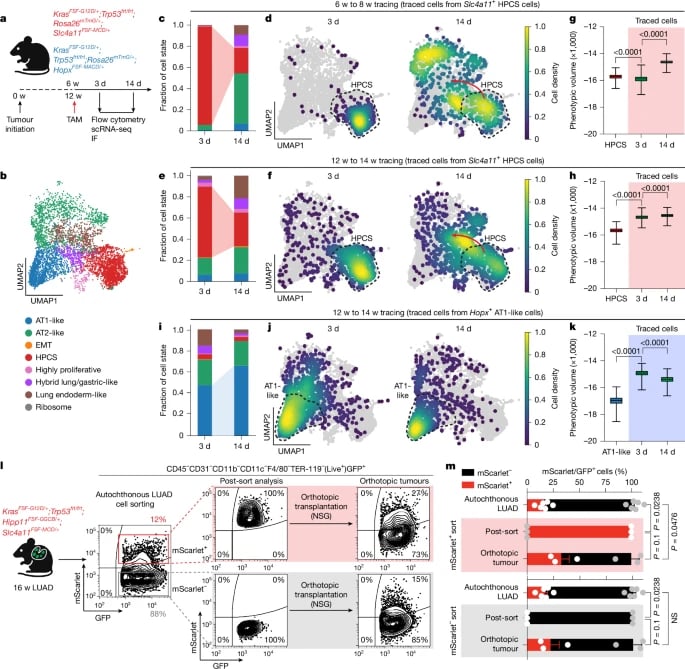
研究还发现,HPCS的数量会随着肿瘤的进展而增加。在癌前病变中,HPCS大约只占3%;而在已形成的肿瘤中,这一比例会上升到约15%;更令人担忧的是,在肿瘤发生转移后,HPCS的数量甚至可以高达30%。这一趋势解释了为何晚期肿瘤往往更难治疗、更容易产生耐药性——因为它们的“变形军团”规模更庞大,适应和抵抗治疗的能力也更强。
澄清重要概念:HPCS与传统“癌症干细胞”有何不同?
在癌症研究领域,长期以来存在“癌症干细胞”(Cancer Stem Cells, CSCs)的概念。传统观点认为,肿瘤中存在一个罕见的、稳定的干细胞样亚群,它们像正常干细胞一样能够自我更新,并持续产生其他类型的癌细胞来维持肿瘤的生长。CSCs被认为是肿瘤的“种子”,具有启动肿瘤、驱动耐药和复发的能力。
然而,这项研究揭示的HPCS则提供了一个新的视角。HPCS并非一个稳定的干细胞亚群,而是一种癌细胞响应局部损伤样信号(例如治疗压力、微环境变化)而获得的“暂时性”高可塑性状态。它更像是正常组织在应对损伤时激活的临时再生程序,而非一个永恒不变的“干细胞库”。癌细胞可以根据需要“进入”或“退出”这种HPCS状态。在这种新的模型中,HPCS更像是帮助肿瘤在不同阶段(从细胞增生到腺瘤,再到侵袭性腺癌)之间切换的“过渡态”或“枢纽”。
这种区别非常重要:如果CSCs是肿瘤的“根”,那么HPCS更像是肿瘤“适应环境的变色龙”和“进化加速器”。靶向CSCs可能需要彻底清除那些具有干细胞特性的细胞,而靶向HPCS则可能意味着干扰肿瘤细胞进入和维持这种高可塑性状态的能力。这项研究为我们提供了更精准、更动态的理解肿瘤异质性和细胞可塑性的框架,也为开发更有效的抗癌策略提供了理论基础。
展望未来:广谱抗癌新策略与MedFind的坚定承诺
这项《Nature》研究的发现,无疑为全球抗癌事业注入了一剂强心针。它将长期以来关于“肿瘤异质性”和“细胞可塑性”的理论猜测,转化为了坚实的实验证据和明确的治疗靶点,为癌症患者带来了前所未有的新希望。
广谱抗癌的巨大潜力
尽管这项研究主要在肺腺癌模型中进行,但科学家们已发现,HPCS样状态普遍存在于其他多种组织的再生上皮和癌中。这意味着,不同癌症可能“不约而同”地劫持了相似的细胞可塑性程序。这一发现为开发针对多种上皮源性癌(如结直肠癌、乳腺癌、胰腺癌等)的广谱新疗法提供了巨大潜力,我们有望找到一个“万能钥匙”来应对多种癌症的耐药和复发问题。
未来治疗策略的多样性
目前,研究人员正在积极探索多种靶向HPCS的策略,包括:
- 小分子药物:寻找能够特异性抑制HPCS细胞功能或诱导其死亡的小分子化合物。
- 抗体偶联药物(ADC):利用抗体精准靶向HPCS表面的uPAR蛋白,并将化疗药物或其他毒素递送到癌细胞内部。
- 新型CAR-T细胞疗法:进一步优化针对uPAR的CAR-T细胞,提高其疗效和安全性。
- 阻断可塑性通路:通过基因疗法或药物,直接破坏维持HPCS状态本身的分子通路,从根本上阻止癌细胞“变形”。
更重要的是,靶向HPCS的策略有望与现有疗法(如化疗、靶向治疗、免疫治疗)形成强大的“组合拳”。通过预先铲除耐药的“火种”,有望让现有治疗的效果更持久、更彻底,显著延长患者的生存期并提高生活质量。对于高危人群,甚至可能开辟癌症预防的新路径。
MedFind:您身边的抗癌专家与希望桥梁
作为由癌症患者家属发起的抗癌信息共享平台,MedFind始终紧密关注全球最前沿的癌症研究进展和药物动态。我们深知,对于身处困境的患者和家属来说,准确、及时、专业的医疗信息是多么宝贵。这项关于HPCS的突破性研究,正是MedFind希望分享给您的重要信息之一,它代表了未来癌症治疗的方向。
MedFind致力于:
- 分享最新抗癌资讯:我们将持续为您解读全球权威机构发布的最新研究成果、临床试验数据和诊疗指南,让您第一时间了解抗癌前沿。
- 提供药物信息与获取渠道:对于国内外已上市或即将上市的创新抗癌药物,MedFind提供详细的药物介绍、适应症、副作用管理建议。一旦HPCS相关的靶向药物进入临床应用,我们将第一时间为您提供合规的海外购药和国际直邮服务,确保您能及时、安全地获取最需要的救命药。
- AI辅助问诊服务:利用人工智能技术,为患者提供个性化的问诊支持,帮助您更好地理解病情,制定治疗策略。
癌症的治疗之路充满挑战,但科学的进步从未停歇。HPCS的发现,让我们对未来充满了信心。MedFind将始终与您并肩作战,为您点亮希望之光,成为您抗癌旅程中最坚实的后盾。
如果您或您的家人正在与癌症抗争,对最新的治疗方案、药物获取有任何疑问,请随时访问MedFind平台,我们的专业团队将竭诚为您服务,共同探索最佳的治疗之路!





