肠道菌群与癌症风险的关联日益受到关注,特别是结直肠癌。最近,一项发表在《科学》期刊上的重磅研究,首次详细揭示了肠道细菌产生的一种毒素——colibactin——如何直接攻击DNA并导致癌症相关突变。这项发现不仅为理解结直肠癌的发生发展提供了全新的视角,也为患者和家属提供了关于疾病预防和早期干预的潜在方向。
肠道“隐形杀手”:Colibactin毒素的致癌机制揭秘
在我们的肠道中,某些特定类型的大肠杆菌(Escherichia coli)能够产生一种名为colibactin的强效毒素。这种细菌产物具有高度不稳定性,但其潜在的致癌能力长期以来一直是科学界关注的焦点。科学家们推测,这种潜伏在肠道的毒素可能导致DNA损伤,进而驱动结直肠癌的发生和进展。然而,由于colibactin分解速度极快,难以获得足够纯化的产物进行深入研究,这使得明确其致癌机制成为一个巨大的挑战。

为了攻克这一难题,由哈佛大学领衔的研究团队巧妙地转换了研究思路。他们不再试图分离和纯化这种不稳定的毒素,而是直接在实验室中,将能够产生colibactin的活细菌与短链DNA片段进行共培养。通过这种创新策略,毒素一旦产生,便能立即作用于旁边的遗传物质,使得研究人员能够有效地捕获并研究其造成的DNA损伤。
独特的DNA双链交联损伤
通过上述策略,研究团队首次清晰地捕捉到了colibactin攻击DNA的独特机制。与许多常见的致癌物通常只损伤DNA双螺旋的一条链不同,colibactin的破坏方式更为极端和彻底——它会在DNA的双链之间创建类似“桥梁”的连接,就像强力胶水一样将两条链紧密粘合在一起,形成DNA交联(DNA cross-linking)。
这种永久性的损伤对细胞来说是巨大的挑战。每次细胞试图复制其基因组时,都需要将DNA双螺旋的两条链解开。然而,colibactin导致的双链交联会成为DNA复制过程中的巨大障碍,阻止细胞正确读取或复制其遗传物质。这种错误的累积最终会导致可能引发癌症的遗传突变。
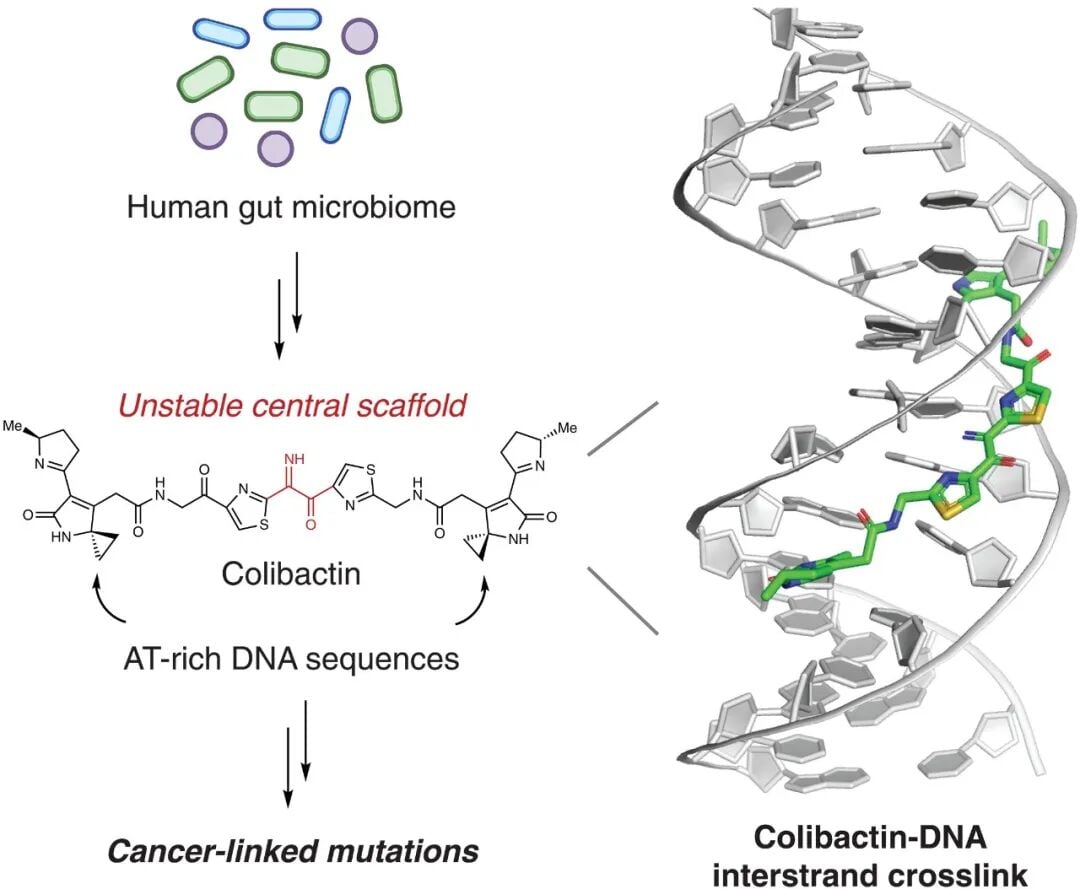
精准打击:Colibactin对DNA序列的选择性偏好
研究进一步发现,colibactin对DNA的攻击并非随机,而是具有高度的选择性。它对富含腺嘌呤(A)和胸腺嘧啶(T)的DNA序列有着强烈的偏好,总是在特定的序列上形成交联。值得注意的是,这种偏好恰好与在结直肠癌患者基因组中观察到的特定突变信号位置高度吻合,这为colibactin在结直肠癌发生中的作用提供了强有力的证据。
为了深入探究这种选择性背后的原因,研究团队转向了结构生物学领域。他们利用核磁共振波谱技术,成功构建了colibactin-DNA交联损伤的结构模型。这一精密的结构模型清晰地揭示了毒素“挑食”的真相:在富含腺嘌呤-胸腺嘧啶的DNA片段中,DNA双螺旋的一侧存在一个带有强烈负电荷的狭窄“凹槽”。而colibactin则拥有一个不稳定、带正电荷的核心区域,其中的特定基团能够完美地嵌入这个“凹槽”并紧密结合,从而实现了对特定DNA序列的精准攻击。
Colibactin机制发现的临床意义与未来展望
这项研究不仅阐明了colibactin导致特定DNA突变的分子基础,更为肠道菌群与癌症风险之间的直接关联提供了关键证据。这一发现具有重要的临床意义:
- 早发性结直肠癌的线索: 研究者指出,与colibactin相关的突变在年轻肿瘤患者中更为常见。这与肠道微生物组中大肠杆菌在生命早期富集的现象相吻合,为理解早发性结直肠癌的环境风险因素提供了宝贵的线索。对于关注癌症风险的患者和家属,了解这些潜在的致病机制有助于提高警惕。
- 新型诊断工具的开发: 对colibactin攻击机制和DNA交联结构的深入认识,有助于未来开发新型诊断工具。这些工具可能用于筛查高风险人群,例如那些肠道中含有产colibactin大肠杆菌的个体,从而实现结直肠癌的早期发现和干预。
- 潜在的治疗与预防策略: 了解colibactin核心区域与DNA结合的机制,也为设计能够中和该毒素的疗法提供了可能。此外,通过改变饮食习惯来减少特定产colibactin大肠杆菌的数量,也可能成为一种有效的癌症预防策略。如果您想了解更多癌症治疗方案和药物信息,可以访问 MedFind 药物信息平台。
这项突破性研究强调了肠道微生物组在癌症发生发展中的关键作用,为我们提供了对抗结直肠癌的新思路。随着对这些机制的进一步理解,未来有望开发出更精准的预防、诊断和治疗方法,从而改善患者的预后。如果您对肠道健康或癌症风险有疑问,可以尝试 AI 辅助问诊服务 获取初步建议。