在癌症治疗领域,靶向疗法和免疫疗法正日益成为对抗恶性肿瘤的关键武器。其中,白细胞介素-7 (IL-7) 及其受体 (IL-7R) 信号通路因其在淋巴细胞发育、免疫稳态调节以及多种疾病(包括癌症)发生发展中的重要作用,正受到广泛关注。本文将深入探讨IL-7/IL-7R的生物学机制,并重点介绍其作为潜在靶点在癌症治疗,特别是白血病等血液肿瘤及实体瘤中的最新临床研究进展,为患者和研究人员提供前沿资讯。
IL-7/IL-7R的生物学基础与广泛表达
IL-7是一种由IL7基因编码的25kDa可溶性分泌蛋白,其受体(IL-7R)则是一个由IL-7Rα和γ链组成的异二聚体复合物。值得注意的是,γ链是多种细胞因子受体(如IL-2、IL-4、IL-9、IL-15和IL-21)的共享组分。IL-7及其受体IL-7R对于T细胞和B细胞的发育、幼稚T细胞的分化与存活,以及记忆T细胞的生成和维持都至关重要。
尽管IL-7 mRNA最初在胸腺中被高水平检测到,但最新研究表明,它在广泛的组织中均有表达。淋巴器官如胸腺和淋巴结(LN)是IL-7 mRNA表达水平最高的部位,同时在肠道、肺、肝脏和皮肤等非淋巴样部位也能检测到其表达。
从细胞来源来看,IL-7主要来源于非造血细胞,包括上皮细胞和内皮细胞。淋巴结中的胸腺上皮细胞(TEC)和成纤维细胞网状细胞(FRC)是重要的IL-7来源。此外,皮肤中的角质形成细胞组成性表达IL-7,肠上皮细胞的IL-7表达可由IFN-γ信号诱导。大脑中的神经元祖细胞也被报道能产生IL-7。
同样,IL-7Rα在整个淋巴系统中广泛表达,涵盖B细胞祖细胞、先天淋巴细胞(ILC)以及T细胞发育和成熟的各个阶段。近期报告还指出,IL-7R在胎儿源性巨噬细胞的发育过程中也有表达。除了造血系统,淋巴管内皮细胞也表达IL-7Rα,并在第三淋巴结构形成期间驱动淋巴管扩张。
IL-7在淋巴系统发育与免疫稳态中的核心作用
IL-7信号传导对整个淋巴系统的发育和维持至关重要,这在IL-7缺陷小鼠模型中得到了充分证实,包括T淋巴细胞、B淋巴细胞和ILC的形成。
IL-7信号被认为是淋巴细胞谱系特异性的关键因素,引导细胞向B淋巴细胞而非T淋巴细胞分化。尽管小鼠的成熟B细胞不表达IL-7R,但从共同淋巴前体(CLP)到祖B细胞,以及随后在骨髓中发育为B细胞,都绝对需要IL-7。而在人类中,IL-7的作用相对不那么关键。
淋巴祖细胞离开骨髓并迁移到胸腺,产生多种淋巴谱系,其发育依赖或受IL-7信号的影响。例如,胸腺NK细胞比传统NK细胞更依赖IL-7。前T祖细胞(双阴性DN细胞)在小鼠中根据CD44和CD25的表达分为四个亚群(DN1-DN4)。从DN2发育到γδT细胞完全依赖于IL-7,IL-7信号通过调节细胞生长基因(如CD98)促进这些DN阶段的增殖和分化。相反,CD4和CD8双阳性(DP)胸腺细胞则不需要IL-7信号,因为这些细胞缺乏功能性IL-7R表达。对于先天淋巴细胞,IL-7对ILC2和ILC3的发育至关重要,IL-7缺陷小鼠完全缺乏这些亚群。
IL-7对免疫稳态的调控
与B细胞不同,IL-7R在幼稚和记忆T细胞中持续表达,IL-7信号对所有T细胞群的长期维持至关重要,它通过调节凋亡的内在途径促进细胞存活。
T细胞激活后,会迅速失去IL-7Rα的表达。外周T细胞中IL-7R表达的维持依赖于Foxo1的活性。而Foxo的活性受到Akt介导的磷酸化的负调节,该磷酸化通过PI3K被上游TCR或IL-2信号激活。这有效地将效应细胞从IL-7依赖的稳态调控中脱离,转而依赖TCR和IL-2信号进行生存和增殖。
此外,在T细胞免疫应答后,大多数效应细胞会发生凋亡,而一些存活下来的成为长期记忆细胞,IL-7信号在这种记忆群体的形成中起着关键作用。在缺乏抗原的情况下,TCR依赖的IL-7Rα表达抑制被逆转,使效应T细胞可以重新表达IL-7Rα。至少在某些情况下,重新表达IL-7Rα的细胞是长期记忆细胞的前体,这表明IL-7可能指引效应器细胞发育为记忆细胞。
此外,越来越多的证据表明,ILC的存活也依赖于IL-7,这也解释了免疫稳态依赖于IL-7的一些特征。
IL-7/IL-7R与疾病:从自身免疫到癌症
IL-7/IL-7R介导的信号促进淋巴发育和体内免疫平衡,其在支持正常免疫方面的作用显而易见。然而,异常的IL-7和IL-7R水平也与免疫病理学相关。IL-7被认为支持自身免疫疾病(如I型糖尿病和多发性硬化症)以及慢性炎症疾病(如类风湿关节炎、强直性脊柱炎和炎症性肠病)中的异常免疫活性。
多项针对多发性硬化症(MS)和原发性干燥综合征(pSS)患者的研究表明,IL-7和IL-7R分别在脑脊液和唇唾液腺中过表达,这些表达水平与疾病的严重程度相关。对自身免疫性疾病的易感性增加与IL-7R基因座的若干单核苷酸多态性有关。据报道,IL7R基因的单倍型可导致可溶性IL-7R水平的上调。然而,IL-7/IL-7R轴的调节如何导致自身免疫性疾病易感性增加的机制在很大程度上仍不清楚。一般认为,IL-7信号的激活促进T细胞的扩增,并增加自身抗原的增殖,从而导致自身免疫的易感性。
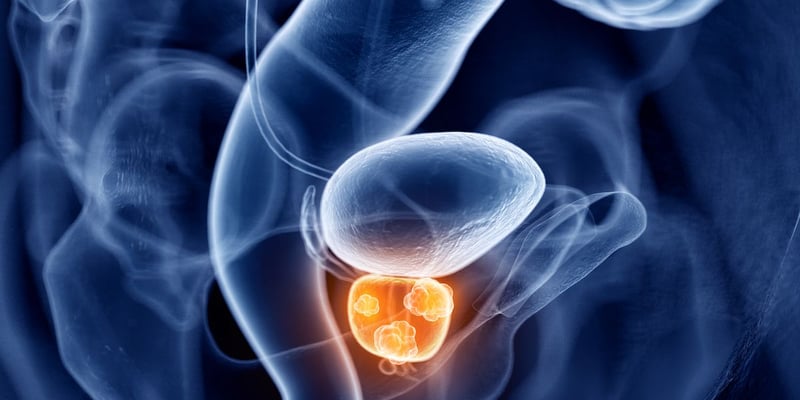
在肿瘤方面,IL-7Rα的过表达与儿童急性B淋巴细胞白血病(B-ALL)的复发密切相关。IL-7Rα基因座已被证明在一小部分BCP-ALL患者中携带功能增益突变,大多数突变与TSLPR上调和配体非依赖性的信号激活同时上调有关。此外,广泛的研究证实了IL-7信号轴参与急性T淋巴细胞白血病(T-ALL)的进展,显示IL-7刺激T-ALL细胞并过表达IL-7Rα。研究发现,T-ALL患者中存在IL-7Rα功能增益突变,该突变导致组成性IL-7非依赖性受体激活,导致IL-7反应增加。考虑到10%的T-ALL患者携带IL-7Rα相关突变,IL-7Rα及其信号通路已成为合理的治疗靶点。除了强有力的证据表明IL-7具有抗肿瘤作用外,一些研究表明,IL-7可能会促进肿瘤进展,例如在非小细胞肺癌中。显然,需要进一步的研究来更好地阐明IL-7在肿瘤进展中的作用。
靶向IL-7/IL-7R通路的临床开发与治疗前景
鉴于IL-7/IL-7R信号与自身免疫、慢性炎症疾病以及癌症的密切关联,针对该通路的靶向治疗在多个层面展开,许多临床试验正在进行和计划中。
在自身免疫性疾病领域,抗IL-7R单克隆抗体能够阻断IL-7信号,从而弱化效应T细胞,同时保留调节性T细胞(Treg)。辉瑞的PF-06342674(RN168)曾在1型糖尿病和多发性硬化患者中进行I期临床试验,但最终因管线调整而终止开发。葛兰素史克的另一种抗IL-7Rα单克隆抗体GSK2618960在多发性硬化症的试验中因未公开原因提前终止,但其在原发性干燥综合征的IIa期研究仍在进行中。OSE的抗IL-7Rα单克隆抗体(OSE-127)正在健康志愿者中进行I期临床试验,旨在对炎症性肠病和干燥综合征患者进行II期评估。
在癌症治疗方面,动物实验表明,IL-7可以诱导T细胞扩增且毒性很小,这预示着IL-7可能对人类具有治疗作用。一项针对淋巴细胞减少型乳腺癌患者的研究表明,化疗前给予IL-7治疗可增加CD4+T细胞;一项针对儿童肉瘤患者的试验将肿瘤疫苗与IL-7结合,证实IL-7可诱导T细胞增加,降低Treg细胞频率,但没有表现出明显的抗癌益处。另一项将IL-7与前列腺癌疫苗Provenge(CITN-03)联合的试验显示,前列腺特异性抗原(PSA)反应性T细胞加倍,这可能预示着患者在研究中获益。
此外,NeoImmune公司的IL-7-Fc融合蛋白在健康受试者中表现出良好的耐受性并显示T细胞增加。其与替莫唑胺(temozolomide)联合治疗胶质母细胞瘤,以及联合阿替利珠单抗(atezolizumab)治疗皮肤癌、黑色素瘤、默克尔细胞癌和皮肤鳞状细胞癌的临床试验正处于1b/2a阶段。IL-7-Fc与帕博利珠单抗(pembrolizumab)联合治疗三阴性乳腺癌的临床也在进行中。最后,IL-7-Fc还将与嵌合抗原受体T细胞疗法(CAR-T)联合用于急性淋巴细胞白血病的试验,这为难治性白血病患者带来了新的希望。
结语
IL-7作为一种重要的细胞因子,其IL-7/IL-7R信号通路在T细胞和B细胞的分化、发育和成熟中扮演着关键角色,是维持适应性免疫和免疫稳态的核心。除了在淋巴细胞发育中的作用外,最新研究表明IL-7/IL-7R也与自身免疫疾病的免疫病理学相关,并且在癌症治疗中展现出巨大的潜力。目前,靶向IL-7/IL-7R通路的多种药物已在自身免疫疾病和癌症患者中进入临床阶段。我们期待这些创新疗法能够带来更多振奋人心的结果,最终使更多患者从中获益,为癌症靶向治疗开辟新的道路。
参考资料:
1.Flip the coin: IL-7 and IL-7R in health and disease,Nature Immunology,2019,20, 1584–1593
2. The Role of Chemokine IL-7 in Tumor and Its Potential Antitumor Immunity. J Interferon Cytokine Res.2022 Jun;42(6):243-250.
3. Modulation of Signaling Mediated by TSLP and IL-7 in Inflammation, Autoimmune Diseases, and Cancer. Front Immunol.2020 Jul 21;11:1557