弥漫性中线胶质瘤(Diffuse Midline Glioma, DMG)是一种侵袭性极强的儿童和青少年脑肿瘤,其治疗面临巨大挑战。这种致命性癌症的典型特征是组蛋白H3的H3K27M突变,该突变会显著降低多梳抑制复合体2(PRC2)介导的H3K27三甲基化(H3K27me3)水平。尽管PRC2在DMG细胞的生长中扮演着关键角色,但其下游的具体分子机制,特别是与多梳抑制复合体1(PRC1)的相互作用,此前仍未完全阐明。
DMG分子机制新发现:CBX4/PCGF4-cPRC1复合体成关键靶点
近日,国际权威期刊《Molecular Cell》发表了一项突破性研究,题为“A specific form of cPRC1 containing CBX4 is coopted to mediate oncogenic gene repression in diffuse midline glioma”。该研究首次揭示,在H3K27M突变的DMG中,一种特定的规范PRC1(cPRC1)复合体——由CBX4和PCGF4组成——是介导癌基因抑制的关键因素。研究发现,H3K27M突变不仅改变了H3K27me3的正常分布,还导致了CBX4-PCGF4-cPRC1复合体在染色质上的结合显著增加,从而进一步加剧了癌基因的抑制作用。这一发现不仅为理解DMG的分子机制提供了全新的视角,也为这种难以治愈的儿童脑癌带来了潜在的靶向治疗新机会。

PRC2功能与DMG细胞生长的关联性研究
研究团队首先利用免疫沉淀结合质谱(IP-MS)技术,深入分析了PRC2的组成,并构建了一个针对PRC2所有11个成员的饱和CRISPR-Cas9文库。结果令人瞩目:只有PRC2的核心酶活性成员,如EZH2、SUZ12和EED,在DMG细胞中被显著耗尽后,细胞生长才受到明显影响。这强有力地证明了PRC2的酶活性对于维持DMG细胞的生存和增殖至关重要。随后的功能恢复实验和体内异种移植实验进一步巩固了EZH2/PRC2功能在DMG发展中的核心地位,为抗癌药研发提供了理论基础。
CBX4和PCGF4:DMG基因抑制的非冗余核心
通过全基因组CRISPR-Cas9筛选实验,研究人员识别出CBX4和PCGF4是DMG细胞中功能上不可或缺的cPRC1成员。尽管它们在cPRC1复合体中的占比不到5%,但其在基因抑制中的作用却至关重要。一系列基因敲除实验进一步证实,只有CBX4的敲除能够显著改变基因表达,而其他CBX家族成员(如CBX2和CBX8)则没有类似效果。这明确指出,CBX4/PCGF4-cPRC1复合体在DMG中发挥着独特的、非冗余的基因抑制功能,使其成为潜在的靶向药研发方向。
H3K27me3分布改变驱动cPRC1结合动态
为深入探究PRC1/2复合体在染色质上的结合动态,研究人员采用了先进的CUT&RUN-Rx技术。结果显示,在H3K27M突变的DMG细胞中,CBX2、CBX4和PCGF4的结合显著增加,而CBX8和PCGF2的结合则有所减少。这种动态变化与H3K27me3的分布密切相关,暗示H3K27me3的改变是导致cPRC1结合动态变化的驱动因素。体外实验也进一步验证了H3K27me3分布的改变对cPRC1结合的直接影响,为理解抗癌药作用机制提供了新的线索。
CBX4中心区域:特异性结合PCGF4的关键
通过精密的CRISPR扫描筛选实验,研究人员发现CBX4的中心区域(氨基酸220-370)对其在DMG细胞中的功能至关重要。该区域的缺失会导致CBX4与PCGF4的结合减少,而与PCGF2和其他PHC亚基的结合增加。这表明CBX4的中心区域是其与PCGF4特异性结合的关键,从而直接影响了cPRC1复合体的组成和功能,为未来开发针对这一特定结合的靶向药提供了精确的靶点。
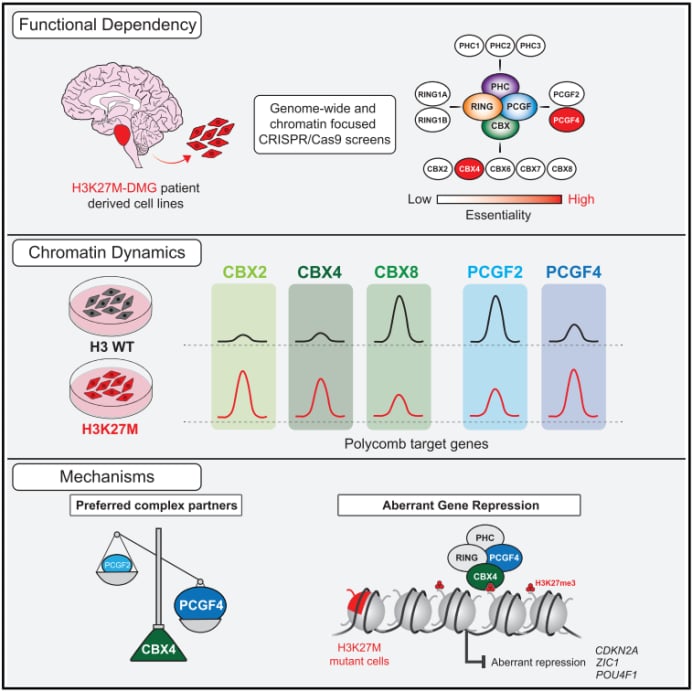
图 本研究模式图
展望与患者支持:靶向治疗新希望
这项研究的发现,不仅为深入理解弥漫性中线胶质瘤的分子机制提供了新的视角,更重要的是,它为开发针对这种致命性儿童脑癌的新型治疗方法提供了潜在的靶点。未来的研究将进一步探索CBX4/PCGF4-cPRC1复合体在其他癌症中的作用,并致力于开发针对这一复合体的特异性抑制剂,以期为DMG患者带来新的希望。
对于面临弥漫性中线胶质瘤等复杂癌症挑战的患者及家属,获取前沿的药物信息和专业的诊疗建议至关重要。MedFind致力于提供全面的抗癌支持,包括最新的药物资讯、诊疗指南,以及便捷的海外靶向药代购服务。如果您正在寻找海外靶向药、抗癌药,或对仿制药有疑问,MedFind的专业团队可以为您提供帮助。通过我们的海外靶向药代购服务,您可以更便捷地获取所需药品。同时,我们的AI问诊服务也能为您提供初步的智能咨询,而药物信息与诊疗指南专区则汇集了丰富的抗癌资讯,助您更好地了解疾病与治疗方案。
原始出处:
A specific form of cPRC1 containing CBX4 is co-opted to mediate oncogenic gene repression in diffuse midline glioma. Mol Cell. 2025 May 14:S1097-2765(25)00405-8. doi: 10.1016/j.molcel.2025.04.026. Epub ahead of print. PMID: 40403727.





