结直肠癌是常见的恶性肿瘤之一,其治疗面临诸多挑战,其中肿瘤细胞逃避免疫系统的监视(即免疫逃逸)是关键因素。了解并阻断癌细胞的免疫逃逸机制,对于提高现有抗癌疗法,特别是靶向免疫治疗的效果至关重要。
结直肠癌与免疫逃逸的挑战
免疫系统本应识别并清除体内的异常细胞,包括癌细胞。然而,肿瘤细胞会发展出多种策略来逃避免疫攻击。程序性细胞死亡配体PD-L1是癌细胞常用的“伪装”手段之一。它与T细胞上的PD-1受体结合,会抑制T细胞的活性,使癌细胞得以存活和增殖。针对PD-1/PD-L1通路的免疫检查点抑制剂(ICIs)已在多种癌症治疗中取得显著成效,但其疗效并非对所有患者都有效,且存在耐药问题。因此,深入研究PD-L1在肿瘤细胞内的调控机制,寻找新的干预靶点,是当前癌症研究的热点。
新研究发现:ID3蛋白的关键作用
近期发表在PNAS杂志上的一项重要研究,由福建医科大学和厦门大学的团队合作完成,揭示了DNA结合蛋白抑制剂ID3在结直肠癌免疫逃逸中的一个此前未被充分认识的关键作用。尽管ID3蛋白通常被认为会抑制某些转录因子的DNA结合能力,但这项研究发现,肿瘤细胞中高表达的ID3,竟然能够增强PD-L1的表达。

ID3如何影响PD-L1表达?
研究团队深入探索了ID3增强PD-L1表达的分子机制。他们发现,ID3蛋白能够与转录因子MYC相互作用,并且令人惊讶的是,它能够“重塑”MYC蛋白的结构,从而显著增强MYC与PD-L1基因启动子的结合亲和力。这种增强的结合导致PD-L1基因的转录活性大大提高,最终使得癌细胞表面PD-L1蛋白增多,更容易逃避免疫细胞(特别是CD8+ T细胞)的攻击。
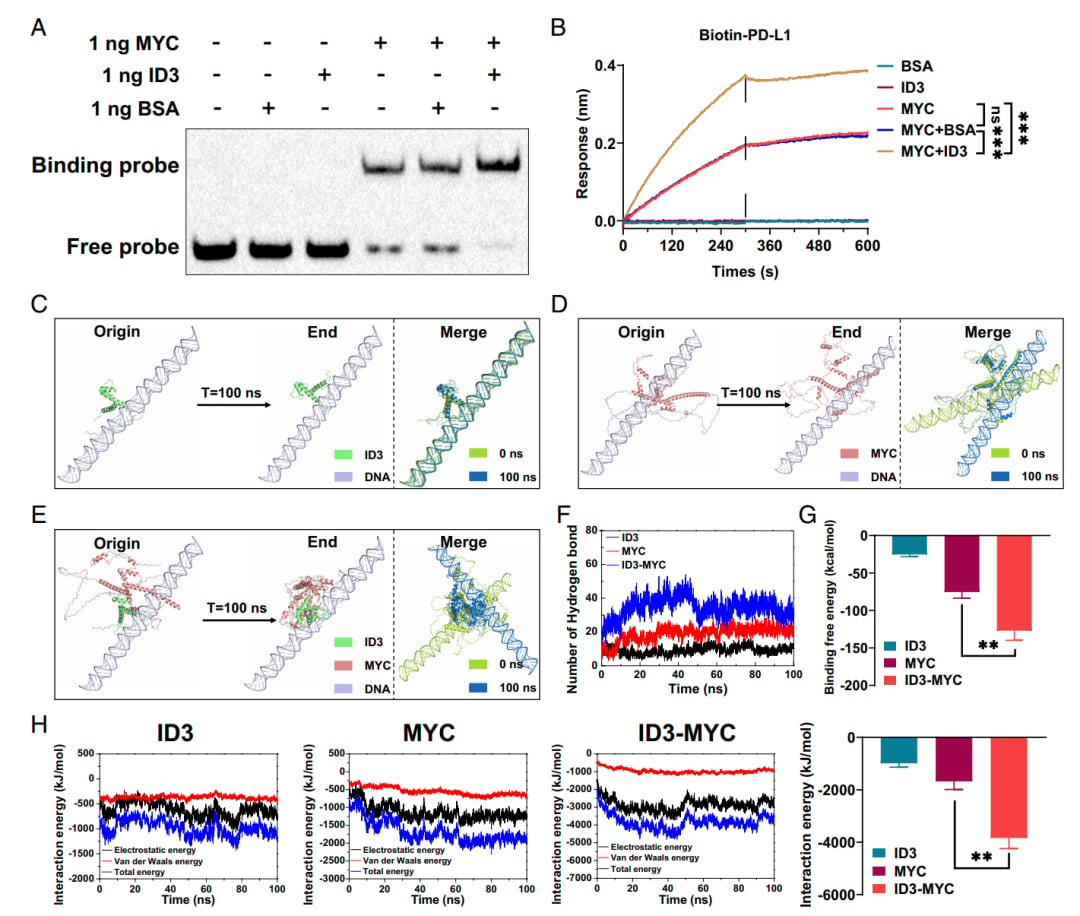
ID3作为潜在治疗靶点
这项研究更令人振奋的是,科学家们在小鼠模型中发现,降低ID3的表达(敲低ID3)能够显著提高PD-L1抗体治疗结直肠癌的效果。这不仅是因为ID3降低后PD-L1表达减少,还因为它能改善肿瘤微环境,增强免疫细胞的活性。这强有力地暗示,靶向抑制ID3蛋白,可能成为未来增强现有抗PD-1/PD-L1免疫治疗疗效的一种新策略。
展望:提升癌症治疗效果
这项研究不仅揭示了ID3在结直肠癌免疫逃逸中的独特作用机制,也为开发新的抗癌药物或联合治疗方案提供了理论基础。未来针对ID3的靶向药物研发,有望克服当前免疫治疗面临的部分耐药问题,为结直肠癌患者带来更好的治疗前景。
对于癌症患者而言,了解最新的研究进展和药物信息至关重要。获取前沿的靶向药、抗癌药信息,探索海外购药途径,或需要专业的AI问诊服务来解读复杂的病情和治疗方案,都可以通过MedFind平台获取帮助。我们致力于为患者提供全面的抗癌资讯、海外靶向药及仿制药代购服务,以及便捷的AI问诊支持,助力患者找到更适合自己的治疗之路。
持续关注癌症研究的最新动态,是患者和家属积极应对疾病的重要一环。希望这项关于ID3和PD-L1的研究,能为未来的结直肠癌治疗带来新的希望。