早筛查不出、结节又分不清怎么办?血浆细胞外囊泡蛋白检测,正在成为癌症早筛领域的重要方向。真正值得患者和家属关心的,不是“技术听起来多先进”,而是它到底能筛哪些癌、准确性如何、能不能替代现有检查、离临床可用还有多远。
为什么癌症早筛这么难
很多癌症在早期几乎没有典型症状,等到出现持续咳嗽、吞咽困难、消瘦、黑便或明显疼痛时,往往已经错过最佳干预窗口。传统筛查手段各有价值,但也各有限制。
- 影像学:适合发现可见病灶,但对极早期微小病灶、良恶性判断存在局限。
- 血清肿瘤标志物:获取方便,但单一指标往往敏感度和特异性有限。
- 内镜或活检:诊断价值高,但属于侵入性检查,不适合所有人群反复筛查。
因此,临床一直希望找到一种更稳定、创伤更小、可重复、还能覆盖多癌种的检测方式。液体活检正是在这个需求下迅速发展,而细胞外囊泡是其中非常受关注的一类载体。
什么是细胞外囊泡,为什么值得关注
细胞外囊泡可以理解为细胞释放到血液等体液中的“微型信息包裹体”。其中的小细胞外囊泡,能够携带蛋白、脂质、核酸等多种分子信息,而且在体液中相对稳定。
这意味着,如果肿瘤细胞释放出的囊泡进入血液,研究者就有机会从一管血中读取与肿瘤相关的信号。相比单一血清标志物,这类信息往往更接近肿瘤本身的生物学状态。
但这条路并不轻松。细胞外囊泡并不只来自肿瘤,正常细胞也会分泌;不同患者、不同癌种之间差异明显;如果缺乏稳定可靠的标志物,再先进的检测平台也很难真正落地。
这项研究解决了哪几个关键问题
这项研究的核心价值,不是简单报告“找到几个蛋白”,而是沿着临床转化路径做了四步验证:
- 先在同源细胞模型中筛出候选标志物。
- 再到真实患者血浆样本中验证多癌种识别能力。
- 进一步开发可并行检测多标志物的微流控-SERS芯片。
- 最后观察术前术后变化,评估这些标志物是否与肿瘤负荷相关。

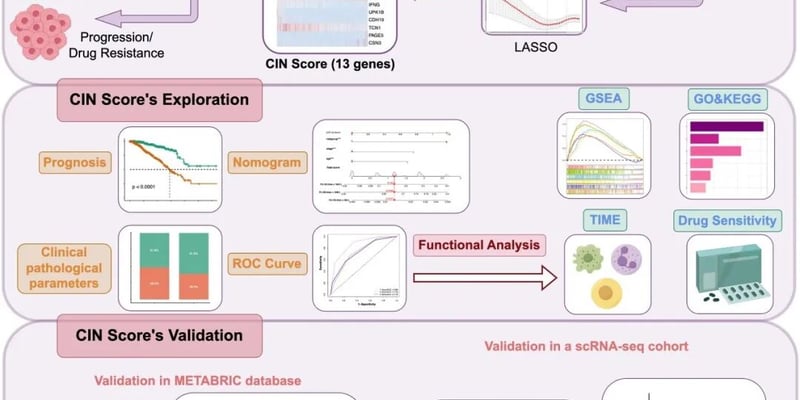
多癌种血浆细胞外囊泡蛋白检测的整体研究路径
核心标志物是怎么筛出来的
研究团队先比较了正常与癌变支气管上皮细胞来源的小细胞外囊泡蛋白组,发现327个差异蛋白,再从中聚焦有潜在临床检测价值的胞外蛋白,最终确定4个核心标志物:THBS1、NID1、PTX3、VCAN。
这一步非常关键。早筛标志物最怕“只在单一模型有效”,而这4个蛋白随后又在22种不同癌细胞系中呈现一致上调趋势,提示它们并非只适用于单一癌种场景。

4个细胞外囊泡蛋白标志物的发现及在多种癌细胞系中的验证
这4个蛋白意味着什么
对患者来说,最重要的不是记住缩写,而是理解它们为什么有机会成为标志物。这些蛋白多数与肿瘤微环境重塑、炎症反应、细胞外基质变化、肿瘤侵袭转移等过程相关。换句话说,它们反映的不是单一突变,而是癌变过程中更广泛的生物学改变,这也解释了其跨癌种检测潜力。
哪些癌种被纳入了临床验证
研究在250例健康人和514例癌症患者的血浆来源小细胞外囊泡中进行了验证。纳入的癌种包括:
- 非小细胞肺癌
- 胶质母细胞瘤
- 结直肠癌
- 前列腺癌
- 黑色素瘤
- 胃癌
- 食管癌
- 小细胞肺癌
结果显示,这4个蛋白在癌症患者中整体显著升高。更重要的是,联合逻辑回归模型在多癌种中的AUC达到0.91-1.00,说明整体区分癌症与健康对照的能力较强。

血浆细胞外囊泡蛋白标志物在多癌种临床样本中的验证结果
AUC 0.91到1.00,患者该怎么理解
AUC是评价检测模型区分能力的常用指标,越接近1,说明模型越能把“有病”和“没病”分开。但患者需要注意两点:
- AUC高,不等于单个患者一定能被准确判断。它反映的是整体统计学性能。
- 筛查场景比病例对照研究更复杂。真实世界中会遇到炎症、良性结节、合并基础病、不同年龄结构等干扰因素。
因此,这组数据说明该方法“很有前景”,但不能直接等同于“已经可以独立替代临床诊断”。
关键数据怎么看更直观
| 研究环节 | 样本或场景 | 核心结果 | 临床意义 |
|---|---|---|---|
| 标志物筛选 | 正常与癌变同源细胞模型 | 发现327个差异蛋白,最终锁定4个核心蛋白 | 建立可检测的候选标志物基础 |
| 细胞系验证 | 22种不同癌细胞系 | 4个蛋白呈一致上调趋势 | 支持跨癌种潜力 |
| 临床验证 | 250例健康人,514例癌症患者 | 联合模型AUC为0.91-1.00 | 提示较强区分能力 |
| 早期分期分析 | 非小细胞肺癌、食管癌、胃癌 | I期检测能力与中晚期接近 | 提示有早筛价值 |
| 筛查应用 | 68例肺结节患者 | 良恶性区分AUC为0.85 | 更接近真实筛查场景 |
I期也能检出,为什么意义大
很多患者真正关心的是:这项技术对“早期癌”有没有用。如果一种方法只能识别晚期肿瘤,对改善总体生存帮助有限。该研究显示,在非小细胞肺癌、食管癌和胃癌中,这组标志物在I期肿瘤中的检测能力与中晚期基本一致。
这意味着它捕捉到的信号,可能在肿瘤体积尚不大时就已出现。对于肺癌、胃癌、食管癌这类“越早发现越能改变结局”的肿瘤,这一点非常关键。

该标志物组合在部分癌种I期肿瘤中的检测表现
微流控-SERS芯片到底先进在哪里
找到标志物只是第一步,能不能把它做成临床可操作的检测平台,决定了技术是否真正有未来。研究团队开发的微流控-SERS芯片,目标就是把多标志物检测做得更高效、更灵敏。
微流控可以理解为在芯片上精准处理微量液体,适合快速、节省样本地完成捕获和反应。SERS则是表面增强拉曼散射技术,能够显著放大检测信号,提高灵敏度,并支持多重标记读取。
该芯片通过非对称电极设计增强纳米混合效应,从而提升小细胞外囊泡的捕获和标记效率。这一步的临床意义在于:如果未来进入常规检测流程,它有望比传统实验室方法更快、更省样本,并具备标准化潜力。

非对称电极设计的微流控-SERS检测芯片
它能用于肺癌和肺结节筛查吗
这是最贴近患者现实的问题。研究先用健康人和已明确诊断的晚期肺癌患者进行检测,结果显示4个蛋白均显著升高,联合分类性能达到AUC=1。这提示同一组标志物在ELISA与SERS两种平台上具有较好一致性。

微流控-SERS平台对健康人与晚期肺癌患者的区分表现
随后,研究把芯片放到了更接近临床真实世界的场景:肺部良恶性结节的区分。在68例肺结节患者中,分类性能达到AUC=0.85。
这组数据尤其值得重视。因为很多“看起来很强”的检测技术,在健康人与确诊癌症患者之间区分很好,一到结节鉴别这种复杂场景就明显下降。AUC=0.85说明它具有一定临床应用前景,但也提示目前仍属于辅助判断工具,而非最终定论工具。

微流控-SERS芯片在肺结节良恶性筛查场景中的表现
术后指标下降,说明了什么
研究还对肺癌患者术前和术后样本做了纵向分析。大多数患者在肿瘤切除后,这4个蛋白的表达水平下降,提示这组小细胞外囊泡蛋白特征与肿瘤负荷存在直接关联。
对未来临床应用来说,这一点有两层意义:
- 一是增强了生物学可信度。它不是偶然相关,而更可能与肿瘤本身有关。
- 二是提示未来可能用于动态监测,例如治疗后趋势观察、复发风险辅助评估等。
但要强调,是否能真正用于复发监测,还需要更大规模、长期随访研究证实。

细胞外囊泡蛋白标志物与肺癌肿瘤负荷的关联验证
这项技术离临床常规应用还有多远
从科研到临床,往往隔着几道门槛。患者在关注新技术时,既要看到希望,也要看清边界。
当前优势
- 血浆样本获取相对方便,适合重复检测。
- 4个蛋白联合检测,比单一标志物更稳。
- 覆盖多癌种,理论上更适合泛癌筛查思路。
- 在I期肿瘤和肺结节场景中已显示实际潜力。
当前局限
- 现阶段仍以研究数据为主,尚不是成熟普及的常规临床项目。
- 不同人群、不同医院、不同实验条件下的稳定性,还需更大规模验证。
- 对炎症、感染、自身免疫病等潜在干扰因素的影响,仍需进一步澄清。
- “能发现异常”不等于“能明确癌种来源”或“直接替代病理诊断”。
患者最关心的几个现实问题
1. 能替代CT、胃镜、肠镜或病理吗
不能。现阶段更合理的定位是辅助筛查、风险分层、辅助判断。如果检测提示高风险,仍需结合低剂量CT、胃镜、肠镜、PET-CT、穿刺活检或手术病理等标准诊断路径。
2. 适合哪些人重点关注
- 有肺癌、胃癌、结直肠癌、食管癌等家族史的人群
- 长期吸烟或有职业暴露史的人群
- 已有肺结节、反复消化道症状但检查结论不明确的人群
- 高龄且存在多种肿瘤风险因素的人群
3. 检测异常是不是就一定得癌症
不是。任何筛查技术都存在假阳性和假阴性问题。真正安全的做法,是让检测结果进入完整的临床决策链,而不是自行下结论。
4. 中国大陆能不能常规做
这类基于细胞外囊泡蛋白的多癌种检测,目前更多仍处于科研转化和临床探索阶段。不同地区、不同机构的可及性差异很大,检测平台、方法学和适用场景也未完全统一。对患者来说,最现实的痛点不是“有没有概念”,而是哪里能做、结果怎么解读、异常后下一步怎么办。
如果家里有人有结节或怀疑肿瘤,下一步更重要
真正影响结局的,往往不是单次检测本身,而是后续决策是否正确。面对肺结节、可疑早癌或复杂检查结果,建议把问题拆开:
- 先确认现有资料是否完整:影像、病理、基因检测、肿瘤标志物是否齐全。
- 再判断当前问题属于筛查、确诊、分期,还是治疗后监测。
- 最后决定下一步是复查、补做检查、手术评估,还是进入系统治疗。
如果已经确诊癌症,接下来的重点就不再只是“查出来没有”,而是分子分型是否明确、标准治疗是否完整、是否还有前沿药物选择。这一步常常决定患者能否抓住真正改变预后的机会。
把早筛信息变成可执行方案
对患者家庭来说,最难的不是看到新研究,而是把复杂信息转成可执行路径:哪些检查值得补、哪些结果需要二次解读、哪些药物在国内外可及性不同、哪些治疗机会不能因为信息差被错过。
如果正面临肺结节鉴别、早癌风险评估、确诊后方案选择,或想了解全球前沿抗癌药物与可及性差异,MedFind可提供更系统的信息支持,包括抗癌资讯检索、治疗方案辅助解读、以及合规渠道下的跨境直邮信息服务。对很多家庭来说,尽早把检查、诊断、用药这三件事理顺,往往比盲目四处求医更能争取时间。
【参考文献】
Lobb RJ, Zhou Q, et al. Early-stage multi-cancer detection through a plasma extracellular vesicle protein signature. Cell Reports Medicine. 2026;S2666-3791(26)00111-4.