肺结节合并肺囊肿,到底是炎症、肺大疱、肺癌,还是罕见病?当影像提示孤立肺结节,同时存在双肺多发囊性病变,单靠CT很难给出答案。对患者和家属来说,真正关键的是:是否需要手术、是否要做ALK融合和FLCN基因检测、会不会遗传、将来是否需要ALK抑制剂治疗。
这类情况最容易被低估。一个肺结节可能被当成炎症性肌纤维母细胞瘤、朗格汉斯细胞组织细胞增生症,甚至普通良性结节;多发肺囊肿可能被简单写成“肺大疱”。但如果背后同时存在ALK阳性组织细胞增生症和伯特-霍格-杜布综合征,漏诊会影响后续随访、家族筛查和肾脏肿瘤风险管理。
肺结节为何会误诊?
ALK阳性组织细胞增生症,英文简称APH,是一种非常罕见的组织细胞肿瘤。它不是常见肺癌,也不是普通炎症结节,而是由组织细胞异常聚集形成的肿瘤性病变。APH可累及肝脏、血液系统、神经系统、骨、皮肤、淋巴结,也可发生在肺部;但仅表现为孤立性肺结节的情况极少见。
误诊的核心原因有三点:
- 影像不典型:肺部APH可表现为单个肺结节,CT上很难与炎症、肉芽肿、炎症性肌纤维母细胞瘤或肺癌完全区分。
- 病理形态复杂:镜下可见泡沫样组织细胞、梭形细胞、多核细胞、图顿巨细胞和少量炎症细胞,容易与其他组织细胞病或间叶源性肿瘤混淆。
- 分子特征少见:APH的核心线索是ALK异常表达或ALK基因重排,但如果没有主动做ALK免疫组化、FISH或二代测序,诊断可能停留在“疑似”阶段。
在肺结节诊断中,如果病理看到梭形细胞并伴炎症背景,临床很容易想到炎症性肌纤维母细胞瘤。尤其当检测到EML4::ALK融合时,误判风险会进一步增加,因为这一融合也可见于部分ALK相关肿瘤。真正决定诊断方向的,是形态学、免疫组化和分子检测的联合判断。
APH的关键诊断证据
APH的诊断不能只看一个指标。较可靠的路径是:先通过病理形态发现组织细胞性病变,再用免疫组化确认组织细胞来源,最后用ALK检测和分子检测锁定诊断。
典型APH的病理表现包括:泡沫样组织细胞聚集、图顿巨细胞、部分梭形细胞、细胞异型性不明显、核分裂象少见。免疫组化通常需要至少两种组织细胞标志物阳性,例如CD68、CD163、CD14、CD4或溶菌酶,同时ALK染色阳性。
| 诊断环节 | 重点看什么 | 对患者意味着什么 |
|---|---|---|
| 影像学 | 肺结节位置、大小、是否伴多发囊肿或肺大疱 | 提示是否需要手术切除、穿刺或密切随访 |
| 病理形态 | 泡沫细胞、梭形细胞、多核细胞、图顿巨细胞 | 判断是否属于组织细胞性病变 |
| 免疫组化 | CD68、CD163、CD4、ALK等阳性;SMA、Desmin等阴性可帮助排除部分疾病 | 决定诊断更偏向APH还是其他肿瘤 |
| FISH检测 | 确认是否存在ALK基因断裂或融合信号 | 为ALK驱动性病变提供直接证据 |
| 二代测序 | 识别EML4::ALK融合、FLCN变异等 | 同时影响诊断、遗传风险评估和后续治疗选择 |
这类病例的时间线往往并不复杂:患者因发热、干咳、胸闷、气促或胸痛就诊,CT发现双肺多发肺大疱或肺囊肿,同时发现一个肺结节。真正改变诊断方向的,是术后病理和分子检测。

肺结节合并肺囊肿的诊断过程,常需要影像、手术病理、免疫组化和基因检测共同完成。
为什么要查ALK融合?
ALK是一类重要的酪氨酸激酶驱动基因。发生ALK重排后,ALK激酶结构域可能被异常激活,进一步启动RAS/RAF-MEK-ERK和PI3K/AKT/mTOR等信号通路,推动细胞增殖和存活。对APH来说,ALK重排是非常关键的诊断线索,也是未来系统治疗可能用到ALK抑制剂的基础。
在已报道的APH病例中,ALK融合伴侣基因并不完全相同,EML4::ALK只是其中一种。值得注意的是,EML4::ALK更为公众熟知的场景是ALK阳性非小细胞肺癌,也可见于某些炎症性肌纤维母细胞瘤。因此,发现EML4::ALK并不等于自动诊断肺癌或IMT,必须结合病理形态和免疫组化。
在实际诊断中,ALK相关检测常见有三类:
- ALK免疫组化:用于判断肿瘤细胞是否表达ALK蛋白,操作相对便捷,常作为筛查手段。
- FISH检测:通过荧光探针观察ALK基因是否发生断裂或重排,是确认ALK重排的重要方法。
- 二代测序:不仅能判断是否存在ALK融合,还能识别具体融合类型,例如EML4::ALK,并同步发现其他有临床意义的变异。
对患者而言,ALK融合检测的价值不只在于“确诊”。如果APH为多系统受累、无法完整切除或后续进展,ALK抑制剂可能成为系统治疗的重要方向。但对于已经完整切除、仅单系统受累且无复发证据的患者,是否立即用药需要非常谨慎,通常要结合病灶范围、症状、术后病理边界、复发风险和多学科意见。
FLCN变异提示什么?
肺部多发囊肿并不总是“肺大疱这么简单”。如果患者存在双肺多发囊性病变,尤其伴有自发性气胸个人史或家族史,应考虑伯特-霍格-杜布综合征,简称BHD综合征。
BHD综合征是一种罕见的常染色体显性遗传病,由FLCN基因胚系突变导致。FLCN编码卵泡蛋白,是一种与肿瘤抑制功能相关的蛋白。BHD最典型的临床表现包括:
- 肺部表现:多发肺囊肿,可伴复发性自发性气胸。
- 皮肤表现:纤维毛囊瘤等皮肤病变,但并非每位患者都会出现典型皮肤表现。
- 肾脏风险:与多种肾脏肿瘤风险增加相关,需要长期监测。
- 遗传特征:常染色体显性遗传,一级亲属可能需要遗传咨询和基因检测。
最容易漏诊的情况,是患者只有肺囊肿或气胸,而没有明显皮肤病变。此时,如果医生没有追问家族气胸史,也没有进行FLCN检测,BHD可能长期被当作普通肺大疱处理。
肺囊肿要查家族史吗?
需要。对肺囊肿患者来说,家族史不是“可有可无”的信息,而是决定是否考虑遗传综合征的重要线索。以下情况尤其建议主动告知医生:
- 本人曾发生不明原因自发性气胸,尤其反复发作。
- 父母、兄弟姐妹、子女中有人反复气胸。
- 家族中有人年轻时出现多发肺囊肿或肺大疱。
- 家族中有人患肾肿瘤,尤其病理类型特殊或双侧、多灶。
- 本人或亲属有面部、颈部、躯干部多发皮肤小丘疹,曾被诊断为纤维毛囊瘤。
如果检测提示FLCN胚系突变,意义不止是给患者本人贴上一个诊断名称。它还会带来三项现实影响:第一,解释肺囊肿和气胸风险;第二,提示需要长期肾脏影像监测;第三,提示直系亲属可能需要遗传咨询。
APH和BHD如何鉴别?
APH和BHD是两个不同层面的疾病。APH是组织细胞肿瘤,核心问题是肺结节或其他器官组织细胞性病变;BHD是遗传综合征,核心问题是肺囊肿、气胸、皮肤病变和肾肿瘤风险。二者可以同时存在,但诊断逻辑不能混在一起。
| 项目 | ALK阳性组织细胞增生症 | BHD综合征 |
|---|---|---|
| 疾病性质 | 罕见组织细胞肿瘤 | 罕见常染色体显性遗传病 |
| 关键基因 | ALK重排或融合,如EML4::ALK | FLCN胚系突变 |
| 肺部表现 | 可表现为孤立或多发肺结节 | 多发肺囊肿,可伴自发性气胸 |
| 关键检测 | 病理、CD68/CD163等免疫组化、ALK免疫组化、FISH、二代测序 | FLCN基因检测、家族史评估、肾脏监测 |
| 治疗重点 | 手术切除;进展或多系统受累时评估系统治疗和ALK抑制剂 | 气胸预防与处理、肾脏肿瘤监测、家族筛查 |
影像、病理和分子检测相互印证时,诊断才更可靠。肺结节和肺囊肿同时出现时,不应只围绕一个疾病解释全部表现。
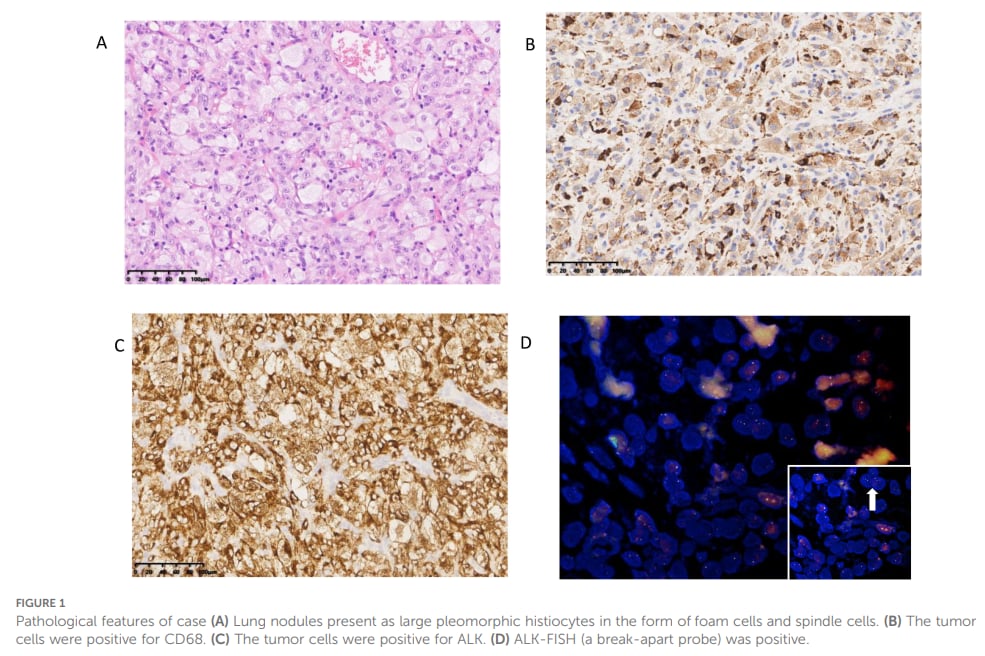
APH的病理诊断依赖泡沫样组织细胞、梭形细胞、图顿巨细胞及ALK相关检测的综合判断。
最容易混淆哪些病?
APH的鉴别诊断很复杂,尤其在肺部罕见发生时,更容易与其他疾病混淆。临床和病理常需重点排除以下疾病:
- 炎症性肌纤维母细胞瘤:也可出现ALK相关异常,且有梭形细胞和炎症背景。鉴别重点包括SMA、Desmin等肌源性标志物。IMT常表达肌源性标志物,而APH更强调CD68、CD163等组织细胞标志物。
- 朗格汉斯细胞组织细胞增生症:肺部可受累,但通常需要结合CD1a、Langerin、S100等标志物判断。
- 幼年性黄色肉芽肿:形态上可与APH相似,关键差异之一是ALK易位或ALK异常表达。
- 罗道病、埃德海姆-切斯特病、网状组织细胞增生症、组织细胞肉瘤:均可能出现组织细胞增生相关病变,需要结合免疫组化、形态和分子检测鉴别。
BHD综合征则需要与其他弥漫性囊性肺疾病区分。例如淋巴管平滑肌瘤病多见于育龄期女性,可与TSC1/2突变相关,HMB-45和SMA可阳性;淋巴细胞性间质性肺炎以多克隆淋巴细胞增殖为特征,也可出现弥漫性囊性肺病变。
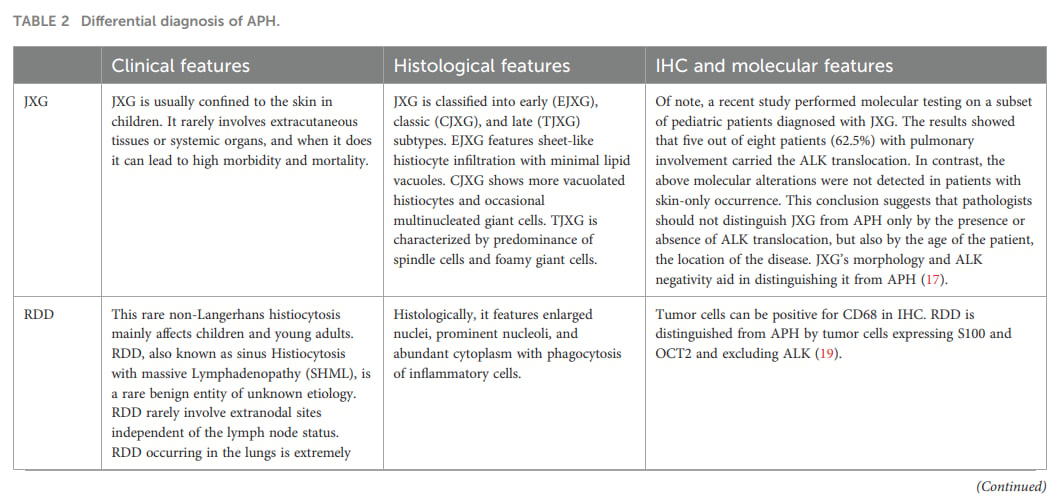
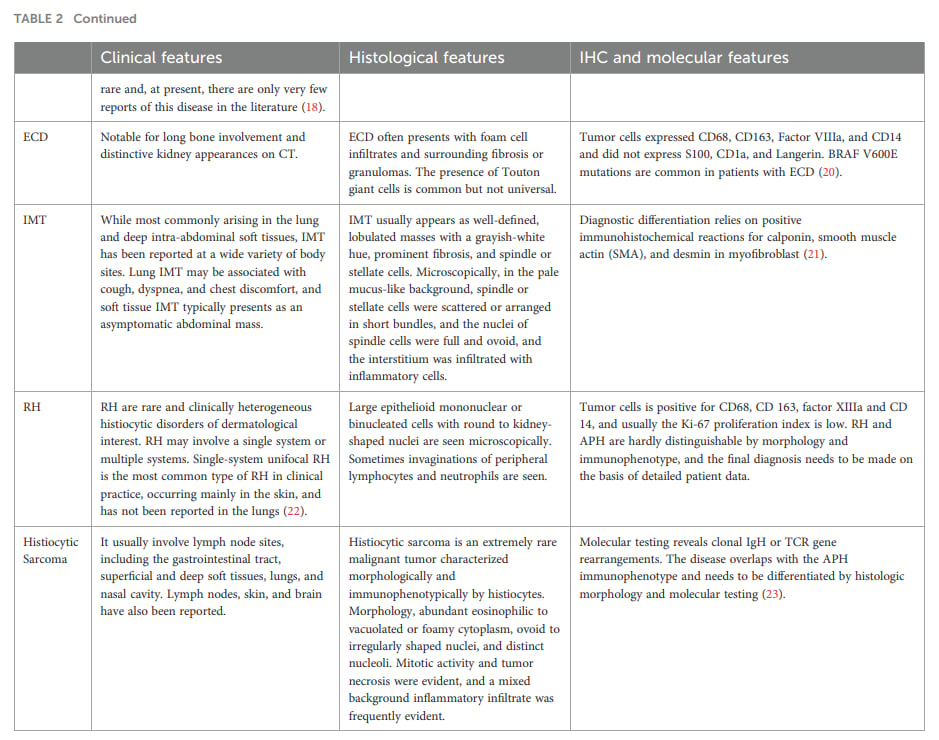
APH的鉴别诊断需要联合病理形态、免疫组化和分子检测,单一指标不足以定论。
治疗一定要用药吗?
不一定。APH的治疗取决于受累范围、能否完整切除、症状严重程度以及是否进展。由于病例极少,目前缺乏统一标准,临床通常采取个体化策略。
| 临床情况 | 常见处理思路 | 患者需要关注 |
|---|---|---|
| 孤立性肺结节,已完整切除 | 术后随访为主,是否追加治疗需个体化评估 | 定期复查胸部影像,关注复发或新发病灶 |
| 单系统受累但切除不完整 | 可能需要多学科讨论,评估局部治疗或系统治疗 | 确认病理边界、残留病灶和ALK状态 |
| 多系统受累 | 可考虑系统治疗,ALK抑制剂是重要潜在选择 | 明确融合类型、药物可及性和副作用管理 |
| 婴幼儿全身性APH | 部分病例支持治疗后可自发缓解,也有病例需系统治疗 | 需在专科团队下严密监测血液系统和肝脏受累 |
既往个案中曾使用支持治疗、化疗、ALK抑制剂,以及地塞米松(Dexamethasone)等药物方案,但由于APH总体病例数量不足,不能简单把个案经验当成标准治疗。对患者来说,最重要的是先把诊断做准,再决定是否需要药物。
如果存在BHD综合征,目前肺囊肿本身没有成熟的特异性逆转治疗。mTOR抑制剂能否预防囊肿形成仍不明确,临床管理重点是气胸风险评估、避免高危诱因、发生气胸时及时处理,以及肾脏肿瘤筛查。
ALK抑制剂何时考虑?
ALK抑制剂并不是所有APH患者的“标配”。它更可能用于无法手术、术后进展、多器官受累或病灶造成明显功能损害的患者。对于仅有一个肺结节且已切除干净的患者,术后观察可能是合理选择。
需要强调的是,ALK抑制剂的选择不能只看“ALK阳性”四个字。不同疾病、不同融合类型、既往治疗史、脑部受累情况、药物可及性和不良反应风险都会影响方案。患者不应自行购药或照搬肺癌治疗经验,而应由熟悉罕见肿瘤和分子诊疗的医生进行评估。
如果医生建议使用ALK抑制剂,患者通常需要提前了解:
- 检测报告是否明确写明ALK融合或重排,融合伴侣是否清楚。
- 病灶是否可测量,是否有基线影像用于疗效评估。
- 是否存在中枢神经系统、肝脏、骨髓等重要器官受累。
- 用药前肝肾功能、心电图、用药相互作用是否已评估。
- 目标药物在当地是否获批、是否可及、费用和后续复查如何安排。
术后随访查什么?
对于APH合并BHD综合征的患者,随访应分成两条线:一条线看APH是否复发或进展,另一条线看BHD相关风险,尤其是气胸和肾脏肿瘤。
| 随访目标 | 建议关注项目 | 原因 |
|---|---|---|
| APH复发风险 | 胸部CT、症状变化、必要时全身评估 | 肺结节切除后仍需观察是否新发病灶 |
| ALK相关治疗准备 | 保存病理切片、基因检测报告、影像资料 | 若进展,可快速评估靶向治疗可能性 |
| BHD气胸风险 | 胸闷、胸痛、突发气短;必要时急诊影像 | 多发肺囊肿患者发生自发性气胸风险增加 |
| BHD肾脏风险 | 肾脏超声、CT或MRI等影像监测 | BHD与多种肾脏肿瘤相关 |
| 家族风险 | 遗传咨询、一级亲属FLCN检测 | 常染色体显性遗传,亲属可能携带同一变异 |
随访频率应由主管医生根据病灶状态、手术结果、家族史和基因检测结果制定。对于BHD患者,肾脏监测不应被忽视,因为肺部症状往往更明显,但真正影响长期风险的还包括肾脏肿瘤。
居家如何降低风险?
APH本身没有特定饮食可以“消除病灶”,BHD相关肺囊肿也不能靠保健品逆转。居家管理的核心是识别危险信号、减少气胸诱因、按时复查和保存完整资料。
- 警惕气胸信号:突发胸痛、胸闷、气短、呼吸困难,尤其是一侧胸痛伴活动后加重,应及时就医。
- 避免吸烟:吸烟会增加肺部损伤风险,对肺囊肿患者尤其不利。
- 谨慎高压环境:潜水、高海拔快速变化、无专业评估的剧烈压力变化活动,可能增加气胸风险。
- 保存关键资料:病理报告、免疫组化结果、FISH报告、二代测序报告、手术记录、CT影像原始文件都应长期保存。
- 家属同步评估:若确认为FLCN胚系突变,直系亲属不应只等症状出现后再检查。
- 心理管理:罕见病最折磨人的地方是不确定性。把诊断、随访和用药问题逐项拆解,比反复搜索碎片信息更重要。
患者最该问医生什么?
面对罕见肺结节和遗传综合征,患者问对问题,往往能显著减少误诊和延误。复诊时建议带着以下清单:
- 我的肺结节最终诊断是否明确为APH?依据是哪些病理和免疫组化指标?
- ALK检测做的是免疫组化、FISH还是二代测序?是否确认具体融合类型?
- 病灶是否完整切除?切缘情况如何?是否需要追加治疗?
- 目前是否有多系统受累证据?是否需要脑部、骨、肝脾或血液系统评估?
- 肺囊肿是否符合BHD综合征?FLCN变异是否为胚系突变?
- 是否需要肾脏肿瘤筛查?用超声、CT还是MRI?多久复查一次?
- 父母、兄弟姐妹、子女是否需要遗传咨询或FLCN检测?
- 如果未来复发或进展,是否有ALK抑制剂等治疗选择?当地能否获得?
药物可及性怎么规划?
罕见肿瘤患者常遇到一个现实问题:诊断结果提示存在明确靶点,但对应药物的适应症、获批地区、购买路径、用药经验和费用并不完全匹配。尤其APH这类极罕见疾病,ALK抑制剂的使用更多依赖病例经验和专家判断,不等同于常见肺癌的标准流程。
因此,药物规划应遵循三个原则:
- 先确认诊断:没有充分病理和分子证据,不应贸然启动靶向治疗。
- 再确认获益场景:完整切除且无复发的患者,可能不需要立即用药;进展、多系统受累或不可切除时,才更需要讨论系统治疗。
- 最后确认可及路径:不同国家和地区药物上市、适应症、处方要求和供应稳定性不同,患者需要提前了解正规渠道。
MedFind长期关注全球抗癌药物、罕见肿瘤治疗和分子诊疗信息。对于已经拿到ALK融合、FLCN变异或复杂病理报告的患者,MedFind可协助梳理报告重点、准备问诊问题、对照国际药物信息,并在符合合规要求和医生处方前提下,提供抗癌药品跨境直邮信息支持。对罕见病患者而言,少走一步弯路,往往就是争取一次更准确治疗机会。
关键结论
肺结节合并多发肺囊肿,不能只按常见病处理。孤立肺结节可能是罕见的ALK阳性组织细胞增生症,多发肺囊肿可能提示BHD综合征。准确诊断依赖病理形态、免疫组化、FISH和二代测序的综合判断。
如果报告中出现EML4::ALK融合,应进一步确认疾病类型,而不是直接套用肺癌或炎症性肌纤维母细胞瘤的诊疗逻辑。如果存在FLCN胚系突变,应同步考虑气胸风险、肾脏肿瘤监测和家族遗传筛查。
罕见病并不等于无路可走。真正的分水岭,是能否及时完成正确检测、找到理解分子报告的医生,并提前规划随访和药物可及性。MedFind希望帮助患者把复杂报告变成清晰行动:哪些要复查,哪些要问诊,哪些药物值得了解,哪些路径可以提前准备。
参考文献
Yang S, Bai Z, Zhao Q, Wang Y and Xi Y (2025) A case of pulmonary ALK-positive histiocytosis combined with Birt-Hogg-Dubé syndrome carrying an EML4::ALK gene fusion: a case report and literature review. Front. Immunol. 15:1501217. doi: 10.3389/fimmu.2024.1501217