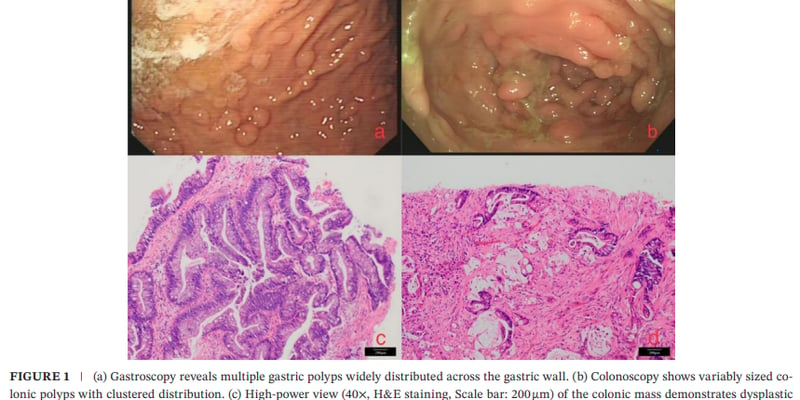
切片太少、标志物太多,罕见肿瘤病理诊断到底该先保分型,还是先看肿瘤微环境?这正是很多患者和家属容易忽视、却直接影响后续治疗判断的关键环节。对于弥漫大B细胞淋巴瘤,尤其是原发性中枢神经系统弥漫大B细胞淋巴瘤这类少见场景,病理不仅要回答“是不是肿瘤、属于哪一型”,还要尽量看清细胞周围的免疫环境,才能为后续治疗策略提供更完整的信息。
为什么罕见肿瘤更怕“切片不够用”?
罕见肿瘤的难点,不只是“少见”,更在于可用于检测的组织样本往往有限。一张病理切片既可能要做常规形态学判断,也可能要做多个免疫标志物检测,甚至还要进一步评估肿瘤微环境。如果每个指标都单独消耗一张切片,现实中很快就会遇到样本不足的问题。
这会带来三个直接后果:
- 诊断分型信息不完整:关键标志物做不全,病理结论可能只能停留在“倾向性判断”。
- 微环境评估难开展:当切片优先用于诊断时,留给研究免疫细胞分布和空间关系的样本就更少。
- 重复取材风险增加:某些部位活检本身就有创伤和风险,能否在已有切片上尽量获得更多信息,临床意义很大。
对于患者来说,病理诊断并不是“走流程”的一环,而是决定后续是否需要进一步基因检测、是否考虑靶向治疗、免疫治疗或临床研究的重要起点。
Dumi技术解决了什么核心问题?
这项研究提出的核心工具,是一种双模式微流控免疫染色装置Dumi。它试图解决的不是单一检测灵敏度问题,而是更贴近临床现实的难题:如何在极少量切片上,同时兼顾多标志物筛查和肿瘤微环境评估。
这套装置具备两种可切换的工作模式:
- 多通道模式:可在同一张切片的不同区域并行检测多种标志物。
- 全腔室模式:可覆盖组织区域进行整张切片染色,并支持循环多重免疫荧光成像。
简单理解,多通道模式更像是在有限样本中尽量“筛全指标”,全腔室模式更像是在同类样本上进一步“看清空间关系”。这种思路的价值,在于让病理分型与微环境研究不再完全割裂。

Dumi装置结构、工作流程及双染色模式示意图。
双模式切换,临床上意味着什么?
病理科最看重的不只是“技术先进”,还包括是否兼容现有临床流程。这项技术的设计重点之一,就是在标准病理切片基础上完成操作,而不是完全脱离现有病理体系另起一套平台。
多通道模式的价值
研究中,多通道模式通过16条彼此隔离的平行微通道,在同一张切片不同区域并行检测多种标志物。对于需要多个免疫表型支持诊断的肿瘤,这种方式能明显提高信息获取效率。
从临床思维看,它特别适合以下场景:
- 组织量有限,无法支持多轮常规免疫组化。
- 需要尽快完成初步分型判断。
- 不同标志物需要在同一病例上进行横向比较。
全腔室模式的价值
当需要进一步分析肿瘤微环境时,全腔室模式可形成覆盖组织区域的统一染色腔室,结合循环多重免疫荧光成像,对整张切片进行更系统的观察。它的重点不只是“看到阳性细胞”,而是进一步分析不同细胞群在空间上的相邻、聚集和分布关系。
这对于理解肿瘤细胞与免疫细胞之间的相互作用具有潜在价值,也为后续探索生物标志物与治疗反应之间的关系提供了方法学基础。
效率提升体现在哪些环节?
研究显示,在优化流速与孵育时间后,传统超过1小时的抗体孵育过程可缩短至10分钟量级。对于病理检测流程来说,这种效率提升并不只是“快一些”,而是可能带来多个层面的改善。
| 比较维度 | 传统流程 | Dumi相关流程特点 |
|---|---|---|
| 抗体孵育时间 | 通常超过1小时 | 缩短至10分钟量级 |
| 切片消耗 | 多指标常需多张切片 | 可在1至2张标准病理切片上完成更多任务 |
| 标志物检测方式 | 多为顺序开展 | 支持区域化并行检测 |
| 微环境评估 | 常需额外样本与额外流程 | 可衔接全切片多重免疫荧光成像 |
| 资源消耗 | 试剂和人工投入较高 | 试剂消耗与时间成本有下降空间 |
对患者最现实的意义包括:
- 减少样本浪费:特别适合活检组织珍贵、重复取材困难的情况。
- 缩短等待时间:病理结果越快明确,后续治疗越容易尽早推进。
- 为后续精准治疗留出空间:当切片用得更省,后续基因检测或补充检测的机会更多。

全腔室模式与传统IHC的性能对比。
对弥漫大B细胞淋巴瘤有什么启发?
研究团队在4例弥漫大B细胞淋巴瘤病例中验证了该技术的诊断应用潜力,其中包括1例原发性中枢神经系统弥漫大B细胞淋巴瘤。这里最值得关注的,不是样本量本身,而是研究路径:先用多通道模式获得诊断相关的多标志物表达信息,再利用同一样本的剩余切片开展全腔室循环多重免疫荧光成像,构建细胞水平的肿瘤微环境图谱。
这种“先分型、再看微环境”的衔接方式,对淋巴瘤尤其有现实意义。因为淋巴系统肿瘤的诊断往往高度依赖免疫表型,而不同肿瘤细胞亚群与周围免疫细胞、基质成分之间的关系,也可能影响疾病行为和后续研究方向。
研究进一步观察到,由特定诊断标志物定义的肿瘤细胞亚群,与其原位微环境组成之间存在关联。这说明病理标志物不只是“贴标签”,还可能成为理解肿瘤空间生态的重要入口。

诊断生物标志物与肿瘤微环境的联合分析。
这项技术离患者治疗还有多远?
这是很多患者最关心的问题。需要明确的是,这项工作属于病理检测与研究方法学层面的进展,重点是提升有限样本中的信息获取能力,并不等同于一种已经普遍进入临床的标准治疗方案。
现阶段更合理的理解是:
- 它为罕见肿瘤和疑难病理场景提供了更高效的检测思路。
- 它有助于把诊断标志物检测与肿瘤微环境分析整合到更连贯的流程中。
- 它为后续开展更大样本验证、标准化流程建设和临床转化打下基础。
因此,患者不必把它理解成“马上就能替代现有病理流程”,但可以把它看作一个非常重要的方向:未来病理不只是给出肿瘤名称,更可能同时给出更丰富的空间生物学信息,帮助医生做出更细的治疗决策。
病理结果出来后,患者最该关注什么?
很多家庭只盯着“是不是癌症”,却忽视了病理报告中真正影响方案选择的内容。尤其在淋巴瘤和罕见肿瘤中,下面这些问题很值得追问:
- 病理分型是否已经明确?
如果报告提示“倾向”“考虑”而非明确诊断,往往意味着还需要更多免疫标志物或分子检测支持。
- 切片和蜡块是否足够继续检测?
如果样本很少,后续基因检测、补充免疫组化、复核会受到限制。
- 是否需要会诊或复核病理?
对于罕见肿瘤、疑难病例和重要治疗决策前,病理复核非常关键。
- 是否需要进一步做分子检测?
病理是治疗起点,但很多靶向治疗和部分创新治疗仍依赖更深入的分子分型。
- 微环境信息是否会影响后续研究型治疗选择?
在部分前沿研究或临床试验中,肿瘤微环境特征可能成为重要参考。
样本有限时,如何尽量避免“检测走弯路”?
对患者和家属来说,最实用的不是记住技术名词,而是避免在样本珍贵时做出低效决策。可以重点把握以下几点:
- 先明确检测优先级:先满足确诊与分型,再规划补充检测与分子检测。
- 尽量集中在有经验的病理团队完成评估:尤其是罕见肿瘤,经验差异会直接影响切片使用效率。
- 保留原始病理资料:包括HE片、免疫组化结果、蜡块信息、病理报告全文。
- 重要节点及时复核:诊断不确定、治疗效果差或方案变化前,复核病理很有必要。
- 同步关注全球诊疗进展:病理分型越清晰,越有机会匹配到更合适的药物、指南和临床研究信息。
为什么前沿病理信息同样影响用药机会?
很多患者以为“药物选择”只看基因检测,其实并不完整。真实临床中,病理诊断、免疫表型、分子特征、肿瘤微环境往往是连在一起的。病理做得越精准,后续治疗路径越清晰。
比如在淋巴瘤、脑部少见肿瘤或其他罕见实体瘤中,病理分型错误或信息缺失,可能导致:
- 错过本应优先考虑的标准治疗;
- 错过后续分子检测窗口;
- 无法及时识别可尝试的前沿药物或临床研究方向;
- 在跨地区、跨医院求医时重复检查,耽误治疗时间。
这也是为什么越来越多患者开始重视“从病理出发的全流程决策”——先把诊断做准,再去谈药物、方案和可及性,成功率更高。
面对罕见肿瘤,下一步怎么走更稳?
如果正面临罕见肿瘤或疑难病理,最需要的往往不是零散信息,而是把病理、指南、药物和就医路径串起来。当病理分型复杂、样本有限、治疗选择不清时,患者最怕的是信息断层:知道病名,却不知道接下来该查什么、问什么、争取什么。
MedFind持续追踪全球抗癌资讯、病理分型进展、前沿药物与诊疗指南,帮助患者和家属更快理解报告背后的治疗含义。如果已经拿到病理结果,却仍不清楚后续方案重点,可借助辅助问诊梳理检测优先级、药物方向和就医决策;如果明确了治疗目标、却面临海外新药可及性问题,也可进一步了解跨境直邮服务,尽量减少因信息与渠道差异造成的等待。
对抗癌症,第一步不是盲目找药,而是把诊断做深、把信息看全、把每一张珍贵切片用到极致。
【参考文献】
Zhang Yu, Shi Bing, Huang Zhenli, et al. Dual-mode microfluidic immunostaining device for diagnostic biomarkers detection and tumor microenvironment evaluation. Science Advances. 2026-01-16.