CAR-T对血液肿瘤很强,但到了实体瘤就“冲不进去、打不久、很快累”怎么办?围绕“能不能用一种更简单的方式让CAR-T更有劲”,研究者把目光投向肝脏产生的酮体β-羟基丁酸(β-hydroxybutyrate, BHB):它是否能像“高效燃料”一样,给CAR-T续航、减少耗竭、提升肿瘤控制?本文用患者听得懂的方式,讲清BHB与CAR-T增强的证据、关键机制(BDH1、线粒体、TCA循环、ATP、耗竭基因)、生酮饮食与BHB补充的边界,以及在临床试验尚在推进阶段,患者如何更安全地参与前沿治疗决策。
1. 一句话抓住重点:BHB可能是CAR-T的“加油站”
这项发表于《Cell》的研究核心结论是:在小鼠肿瘤模型里,BHB能提升CAR-T细胞的代谢适应性与抗肿瘤活性,表现为CAR-T扩增更好、肿瘤控制更强。更重要的是,研究提示BHB的作用主要是“帮免疫细胞更能打”,而不是直接杀肿瘤。
对很多患者家庭而言,这个方向的吸引力在于:相较于再做一次复杂的基因工程改造,代谢干预听起来更“轻”、更容易整合进治疗流程。但也必须强调:目前的关键证据来自动物与机制实验,临床效果与安全性仍需要严格的临床试验验证,不能把它当成已经证实可替代标准治疗的方案。
2. 研究做了什么:从“生酮饮食有效”追到“BHB是关键差异”
研究团队先问了一个很现实的问题:饮食结构会不会影响CAR-T疗效?他们在小鼠中测试了6种饮食(包括高纤维、高蛋白、西式饮食、生酮饮食等)。结果是:只有生酮饮食在CAR-T治疗后显示出一致的肿瘤控制改善。
接着他们去找“为什么只有生酮饮食有效”。通过代谢差异分析,发现生酮饮食组的小鼠BHB水平明显更高,提示BHB可能是这套饮食产生免疫增强效应的关键代谢物。

为什么不直接推荐“所有人都去生酮”?
原研究也明确提到:生酮饮食对癌症患者并不友好,原因包括宏量营养素比例要求极严格、潜在营养缺乏风险、以及肿瘤相关食欲不振等。很多患者在化疗、放疗、靶向或免疫治疗期间,本就存在体重下降、低白蛋白、贫血等问题,此时盲目生酮可能带来额外风险。
所以研究者进一步追问:如果不做整套生酮饮食,单独补充BHB能不能获得类似收益?
3. 单独补充BHB:在多种肿瘤模型里“只在CAR-T存在时才更好”
研究在多种小鼠肿瘤模型中观察到:补充BHB后,CAR-T细胞扩增更好、肿瘤杀伤更强,包括淋巴瘤、白血病模型,甚至还包括一个耐药性胰腺癌模型。
特别关键的一点是:只有在使用CAR-T时,BHB带来的改善才明显;如果没有工程化T细胞治疗,单独给BHB几乎没有影响。这种结果支持一个更“靠谱”的解释:BHB不是“神奇抗癌药”,它更像是给CAR-T提供了更适合的能量与状态管理,让CAR-T在肿瘤微环境的高压与消耗战里更耐打。
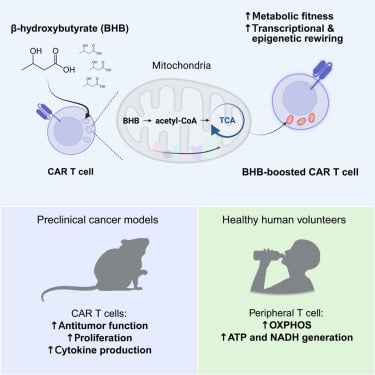
4. BHB为什么能“点燃”CAR-T:把机制翻译成患者能理解的话
很多免疫治疗失败,失败的不一定是“武器不够锋利”,而是“电量不够、系统过热、续航崩溃”。肿瘤微环境常常缺氧、缺营养、酸性强,还会用各种信号让T细胞进入耗竭(可以理解为“越打越乏,最后按不动扳机”)。这项研究提供了三个层面的机制证据。
4.1 代谢层面:BHB进入线粒体“发电站”,接入TCA循环
研究用稳定同位素示踪追踪BHB去向,发现CAR-T可以快速利用BHB,并把它整合进三羧酸循环(TCA循环)。如果把细胞比作一座工厂:TCA循环就像核心的“发电车间”,为线粒体提供持续发电的原料。
进一步实验显示,接触BHB的CAR-T细胞耗氧更多、产生更多ATP(细胞通用的能量货币)。对患者来说,这意味着:在“能量更紧张”的肿瘤环境里,这些CAR-T可能更能维持作战强度和存活。
4.2 基因表达层面:激活与杀伤基因更多,耗竭相关基因更少
研究用单细胞RNA测序看到:BHB处理过的CAR-T细胞更倾向表达与激活、肿瘤杀伤相关的基因,同时更少表达与耗竭相关的基因。简单说就是:不仅“更有电”,还更像“处在战斗模式”,而不是“躺平模式”。
4.3 染色质层面:让关键DNA区域更“可访问”,利于维持战斗状态
研究还使用ATAC-seq、CUT&RUN等技术(可理解为“查看哪些基因开关更容易被打开”),发现BHB让一些关键区域对CAR-T更开放,从而帮助它们更好地表达与能量、健康状态、抗肿瘤功能相关的基因程序。这提示BHB不只是短暂“补能”,还可能参与了“作战系统的配置优化”。
4.4 关键验证:敲掉BDH1后,BHB优势消失
研究用CRISPR敲除了BDH1(一种把BHB转化为可用能量的关键酶)。结果是:没有BDH1,CAR-T细胞不再因BHB而改善。这一步非常重要,它证明BHB带来的增强依赖于被细胞真正代谢利用,而不是“只是发出某种信号”。
5. 这对“实体瘤CAR-T难题”意味着什么?
实体瘤CAR-T面临的核心挑战通常包括:肿瘤微环境抑制、营养竞争、缺氧酸化、浸润不足、抗原异质性等。BHB这类代谢干预,理论上最可能改善的是其中的“代谢压力与耗竭”这一块:让CAR-T在恶劣环境里更能活、更能持续工作。
但也要把预期放到正确位置:代谢加油不等于解决所有障碍。例如肿瘤抗原选择、CAR结构设计、细胞制备质量、浸润能力、以及与放疗/化疗/免疫检查点抑制剂的联合策略,仍然是实体瘤CAR-T成败的决定因素。BHB更像是可能的“增强模块”,而不是“单点翻盘”。
6. 患者最关心的3个问题:能不能用?怎么用?安全吗?
6.1 现在就能把BHB当成“抗癌补剂”吗?
不建议。原因很直接:目前核心证据来自动物与机制研究,临床数据尚在积累阶段。研究提到针对大型B细胞淋巴瘤的BHB补充剂临床试验已经启动,这意味着它正在走向“人体证据”验证,但在结果公布前,任何把BHB补充等同于“已证实有效抗癌治疗”的说法都不严谨。
6.2 如果正在做CAR-T,是否可以自行生酮或自行补充BHB?
务必先与CAR-T团队沟通,尤其是以下人群更要谨慎:存在明显消瘦或营养不良、糖代谢异常、肝肾功能异常、严重恶心呕吐或腹泻、正在使用激素或有严重感染风险的患者。CAR-T治疗期间还可能出现细胞因子释放综合征(CRS)和神经毒性(ICANS),任何饮食或补充剂干预都不应在脱离团队监测的情况下进行。
更现实的做法是:把BHB作为“可讨论的联合策略”带到门诊,询问是否有正在招募的临床试验、是否可在研究框架下接受补充剂、以及是否有明确的监测方案(电解质、肝肾功能、体重、营养指标等)。
6.3 如果医生同意尝试,居家管理要盯哪些风险信号?
即便是在研究框架内,患者与家属也应学会“守住安全底线”。以下为通用的风险提示(不替代个体化医嘱):
- 营养与体重:出现体重快速下降、乏力明显、进食量显著减少时,优先保证总热量与蛋白质摄入,避免为了“控碳/生酮”而加速恶病质。
- 消化道反应:持续腹泻、呕吐可能导致脱水与电解质紊乱,应及时就医评估补液与化验。
- 代谢与电解质:头晕心悸、肌肉抽搐、意识改变等需要警惕电解质异常;糖尿病患者更要关注血糖波动与酮体相关风险,所有调整必须由医生指导。
- 感染与发热:CAR-T后发热需要与团队快速沟通,不能用“饮食调整”替代规范评估。
饮食方面,如果不能安全生酮,很多患者更需要的是“稳住营养、减少波动”:少量多餐、优先优质蛋白(鱼禽蛋奶豆)、能量密度足够的主食与脂肪搭配、保证水分与电解质,必要时使用肿瘤营养补充剂并由营养师评估。
7. 读懂这项研究对你有什么直接价值:如何把“前沿信息”变成“可行动的问题清单”
对患者家庭而言,这类研究最有价值的地方不是“立刻照做”,而是帮助你在就诊时提出更专业、更关键的问题,避免错过可能的试验机会:
- 我的疾病类型与分期,是否有CAR-T适应证或可入组的实体瘤CAR-T研究?
- 我的治疗目标是桥接移植、复发难治挽救,还是争取长期缓解?是否需要联合策略?
- 是否有围绕代谢干预(如BHB)、饮食方案或免疫代谢调控的临床试验在招募?入组标准是什么?
- 如果参与试验,需要监测哪些指标,出现哪些症状必须立刻联系团队?
- 我目前的营养状态是否允许进行饮食结构调整?是否需要营养科共同管理?
8. MedFind能提供什么:把“可能有效”变成“更可及、更可控”
当你看到“BHB增强CAR-T”这类前沿信息,最难的往往不是理解概念,而是把它转化成安全可行的下一步。MedFind建议你优先做两件事:
- 辅助问诊与方案解读:把病理/基因检测、既往治疗史、当前用药与不良反应整理后,我们可以协助你把问题聚焦到“是否适合CAR-T或相关临床试验”“是否需要联合治疗”“营养与代谢干预如何安全评估与监测”等关键决策点,避免在信息洪流里走弯路。
- 跨境直邮的用药可及性支持:若在规范诊疗路径中确有需要用到境外已上市、国内暂未充分可及的相关支持用药或方案环节(以主治医生处方与当地法规为前提),我们可帮助你更高效地了解合规获取路径、时间成本与风险控制,让治疗节奏不被“信息差”拖慢。
如果你愿意,把你的诊断(肿瘤类型、分期)、既往治疗、是否计划CAR-T、以及目前最困扰的症状或副作用发来,我们会优先帮你把“能做什么、先做什么、哪些不能做”列成清单,让每一步更确定。
【参考文献】
Shan Liu et al, β-Hydroxybutyrate Enhances the Metabolic Fitness of CAR T Cells in Cancer, Cell (2026). DOI: 10.1016/j.cell.2026.02.004.

![转移性去势抵抗性前列腺癌治疗新进展:镥[177Lu]特昔维匹肽联合帕博利珠单抗疗效与副作用全解析 3 转移性去势抵抗性前列腺癌治疗新进展:镥[177Lu]特昔维匹肽联合帕博利珠单抗疗效与副作用全解析](https://medfind.link/wp-content/uploads/2026/05/b5eabf912ca30af172ff43ee330147e8.jpg)