“IDH1突变的星形细胞瘤,为什么还会检出KIAA1549::BRAF融合?是不是检测错了、还是病理分型要改?”很多患者家属拿到二代测序(NGS)报告时最焦虑的就是这类“看起来互相矛盾”的结果。本文以一例31岁成人中枢神经系统WHO 4级弥漫性星形细胞瘤为线索,讲清IDH1 p.R132L突变与KIAA1549::BRAF融合为什么可能共存、全面分子检测为何必要、这些结果如何影响治疗路径(手术/放化疗/靶向药物策略),以及正在接受替莫唑胺(泰道, Temozolomide)期间更可操作的居家管理要点。
一、先把核心结论说清楚:为什么这例“少见但重要”
在传统认知里,IDH突变更常见于成人弥漫性胶质瘤(如IDH突变型星形细胞瘤、少突胶质细胞瘤),而KIAA1549::BRAF融合更常见于儿童的毛细胞性星形细胞瘤(WHO 1级)及弥漫性软脑膜胶质神经元肿瘤(DLGNT)。因此很多医生与患者会默认它们“互斥”。
但这例病例提示:在成人、甚至在WHO 4级星形细胞瘤中,也可能出现IDH1突变(p.R132L)与KIAA1549::BRAF融合同时存在。意义在于:
- 诊断层面:不能只凭单一分子标志下结论,整合病理形态、免疫组化与NGS才更可靠。
- 治疗层面:这是典型的“双通路驱动”思路——一条是IDH突变导致的代谢异常(2HG升高),另一条是BRAF融合导致的MAPK通路持续激活。未来制定方案时,可能需要考虑“多模式”或“多靶点”策略。
- 患者沟通层面:当报告出现“少见共存”时,更需要复核检测质量与方法学,并寻找有经验的神经肿瘤团队做解读与决策。
二、病例信息速读:从症状到治疗路径
1)就诊原因与影像学
患者男,31岁,以两次癫痫发作伴意识丧失就诊。MRI显示双侧额叶、双侧大脑半球存在T2/FLAIR高信号浸润性占位病变,并累及胼胝体;病灶伴水肿、周边浸润,且可见强化与中心坏死。功能磁共振提示病灶邻近运动功能区,为手术风险评估提供依据。
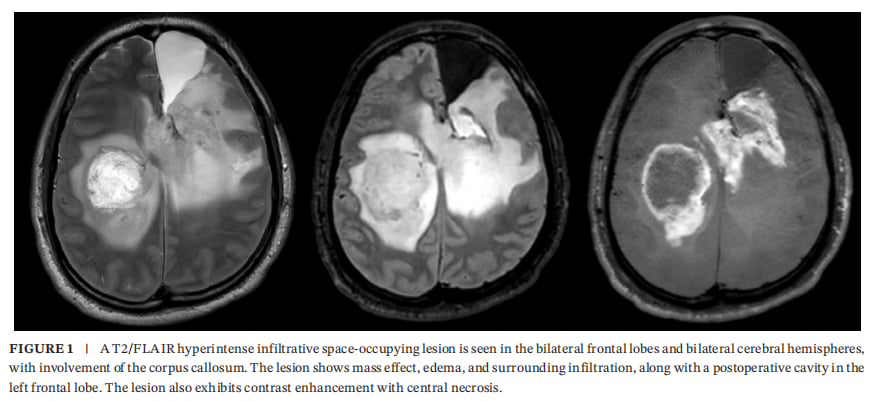
双侧额叶及双侧大脑半球可见T2/FLAIR高信号浸润性占位性病变,累及胼胝体
2)手术与放化疗
患者接受开颅手术,术者实现肿瘤全切除(GTR)。术后放疗总剂量59.4 Gy,分33次完成;同时进行替莫唑胺同步化疗,之后继续辅助治疗,目前已完成11个周期,计划追加第12周期。
对患者家属而言,这里有一个非常关键的现实点:即使后续出现靶向治疗机会,手术+放疗+替莫唑胺仍然是WHO 4级弥漫性星形细胞瘤的基础治疗框架之一;靶向通常是在“分子结果提示可获益”且“时机合适(复发/进展、或临床试验)”时作为增强策略。
三、病理与免疫组化:为什么被诊断为WHO 4级星形细胞瘤
组织学显示弥漫浸润性胶质肿瘤,中至高细胞密度,核分裂活性高,并出现微血管(内皮)增殖与坏死等高等级特征。免疫组化提示GFAP与OLIG2阳性,ATRX表达缺失,p53弥漫阳性,Ki-67增殖指数高(最高增殖区域25%–30%)。这些信息共同支持高等级星形细胞瘤的诊断框架。
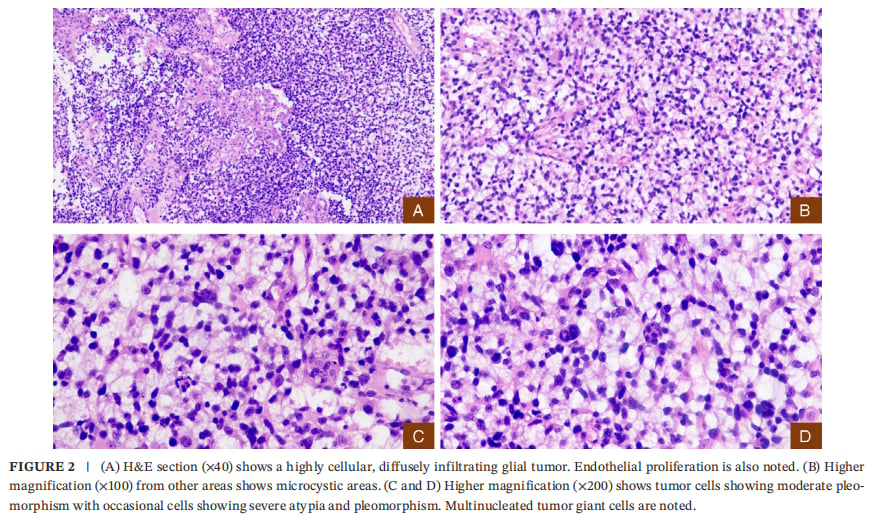
H&E切片显示弥漫浸润、高度细胞化与微囊样区域,部分可见多核肿瘤巨细胞
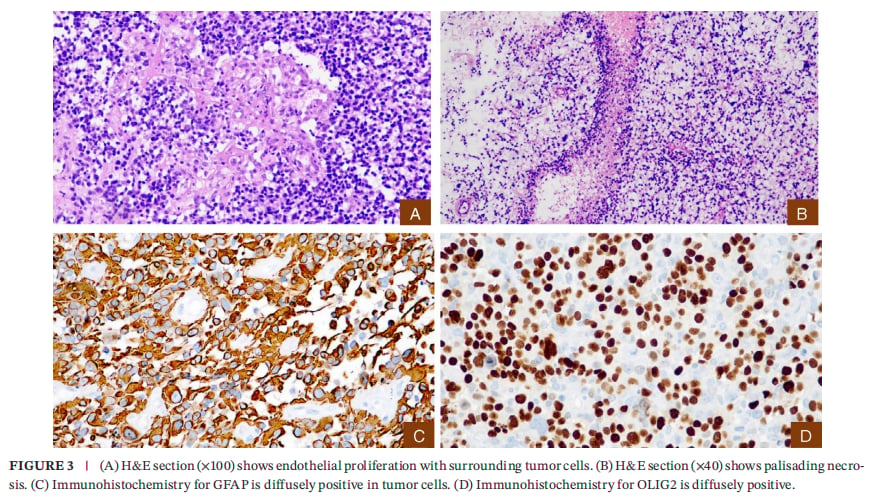
可见内皮细胞增殖、栅栏样坏死;GFAP与OLIG2免疫组化弥漫阳性
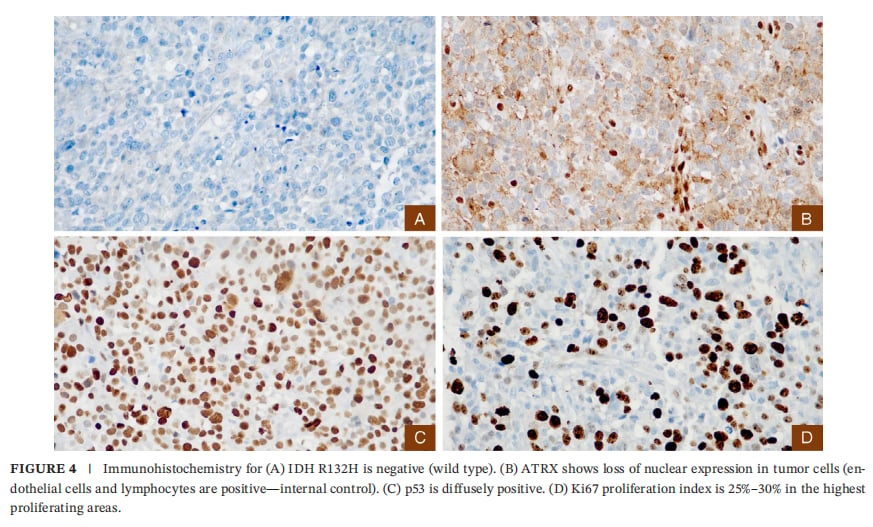
免疫组化提示ATRX缺失、p53弥漫阳性、Ki-67较高;IDH R132H抗体为阴性
需要特别解释的一点是:免疫组化里“IDH R132H阴性”并不等于“没有IDH突变”。因为常用的IDH1 R132H抗体只识别最常见的R132H替换;像本例的IDH1 p.R132L属于“非R132H型”,免疫组化可能显示阴性,必须靠分子检测(NGS或测序)确认。
四、NGS结果怎么读:哪些改变“真的影响治疗”
这例病例的NGS质量控制良好(平均覆盖深度4091×等),并在报告中排除了VAF低于5%的变异及良性/可能良性变异,以增强临床相关性。最终检出几类重点改变:
- IDH1 p.R132L突变(VAF 27%):关键致癌驱动。
- TP53突变(2个变异,VAF 53%与43%):提示抑癌通路受损。
- CDKN2A缺失:进一步推动细胞周期失控与增殖。
- KIAA1549::BRAF融合:检出1443条比对读长,并经FISH验证,提示功能获得性改变,可激活MAPK通路。
把这些信息“翻译成人话”,可以理解为:肿瘤像一辆失控的车,IDH1突变让燃料系统变成“产生有毒废气(2HG)”的模式,TP53与CDKN2A的损伤让刹车失灵,而KIAA1549::BRAF融合相当于油门卡死在高转速,让MAPK通路持续加速。单靠一种手段往往不够,因此才会强调多学科与多模式治疗。
用表格快速抓重点
| 检测发现 | 代表什么 | 对患者最直接的意义 |
|---|---|---|
| IDH1 p.R132L | IDH突变型弥漫性胶质瘤关键驱动,导致2HG升高 | 提示可能存在IDH抑制剂治疗思路(多用于复发/进展或临床试验场景),也提醒免疫组化R132H阴性不能排除IDH突变 |
| KIAA1549::BRAF融合 | MAPK通路持续激活(常见于儿童低级别胶质瘤) | 提示未来可能考虑MAPK通路相关靶向策略(如MEK抑制剂方向),但在成人高等级胶质瘤中的最佳用法仍需更多证据支持 |
| TP53突变、ATRX缺失 | IDH突变型星形细胞瘤常见伴随事件 | 为整合诊断提供支持 |
| CDKN2A缺失 | 细胞周期调控受损,促进增殖 | 提示生物学行为可能更“凶”,更需要规范随访与治疗强度评估 |
五、验证实验:为什么说“不是巧合或误检”
为了避免“NGS假阳性”的争议,研究者做了两类验证:
- Sanger测序验证IDH1 p.R132L:色谱图显示c.395G>T杂合替换的重叠峰。
- FISH验证KIAA1549::BRAF融合:按判读标准,本例约40%的肿瘤细胞出现融合信号模式,支持融合真实存在。
 T杂合峰提示真实突变” style=”display: block; margin: 15px auto; max-width: 100%; border-radius: 8px”>
T杂合峰提示真实突变” style=”display: block; margin: 15px auto; max-width: 100%; border-radius: 8px”>
Sanger测序提示IDH1第4外显子132位点存在c.395G>T杂合替换
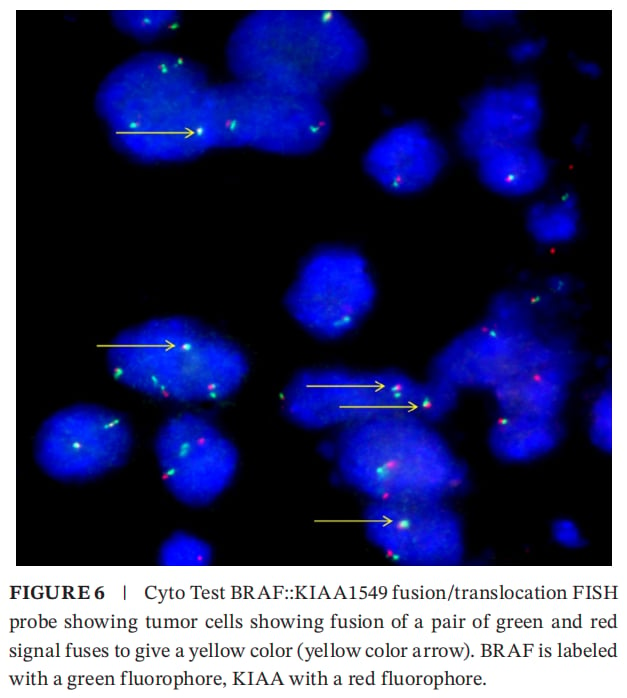
FISH显示部分肿瘤细胞出现红绿融合的黄色信号,支持KIAA1549::BRAF融合存在
六、机制科普:两条通路各在“帮肿瘤做什么”
1)IDH突变:把细胞“代谢废物”变成致癌信号
正常IDH像“工厂里的标准机器”,把异柠檬酸加工成α-酮戊二酸。突变后机器“改装”,反而把α-酮戊二酸加工成2HG。2HG可以理解为一种“会干扰细胞开关系统的错误信号分子”,其积累与胶质瘤发生发展相关。
这也是为什么会出现针对IDH突变的抑制剂:目标不是“杀死所有细胞”,而是尽量让这台“改装机器”停下来,降低2HG,推动肿瘤细胞向更正常的分化方向走。
2)KIAA1549::BRAF融合:让MAPK通路“常开不关”
BRAF本身是信号通路中的“中继放大器”。当发生KIAA1549::BRAF融合后,关键的自我抑制结构域缺失,相当于中继放大器的“限流阀”坏了,导致MAPK通路持续被激活,细胞不断接到“增殖、存活”的指令。
因此,在携带BRAF相关异常(包括融合或特定突变)的胶质瘤中,临床会探索MAPK通路靶向药物(例如MEK抑制剂方向)。但请注意:不同类型的BRAF异常对不同靶向药敏感性并不完全相同,治疗决策应由神经肿瘤专科结合分子类型、分级、既往治疗与药物可及性共同判断。
七、治疗意义:患者最关心的3个问题
问题1:现在正在用替莫唑胺,还需要做什么“加项”吗?
在已完成手术、放疗并进行替莫唑胺辅助治疗的背景下,通常最重要的是:
- 按计划完成治疗与复查:包括MRI随访(常见为每2–3个月一次,具体遵医嘱),监测是否复发/进展。
- 保留完整检测与病理材料:病理切片、蜡块、NGS原始报告与必要时的原始数据(如FASTQ/BAM可选)便于二次解读或复检。
- 提前做“复发预案”:包括临床试验筛选、靶向治疗可行性评估、跨院MDT会诊准备等。
这类“双驱动”并不意味着立刻要在标准治疗之外自行加药,更不建议在未明确获益证据时盲目叠加靶向药,以免毒性叠加、影响放化疗完成率或掩盖影像评估。
问题2:IDH靶向药能不能用?
证据层面:报道提到IDH突变(包括R132L)对IDH抑制剂敏感,能够降低2HG并促进分化,并且相关I期研究显示可实现疾病稳定且安全性特征良好。
药物层面:词典收录的IDH抑制剂为艾伏尼布(拓舒沃, Ivosidenib)。需要坦诚说明的是:不同国家/地区对其适应症与可及性存在差异;即便可获得,也通常需要神经肿瘤医生结合“是否复发/是否有临床试验/既往治疗线数/影像与症状”等综合决定是否使用。
问题3:BRAF融合提示一定要用MEK抑制剂吗?
不一定。现有证据更多来自BRAF异常的儿童低级别胶质瘤,MEK1/2抑制剂司美替尼在相关研究中显示出疗效,并在进行与标准化疗对比的III期研究。
但把这些证据“平移”到成人WHO 4级弥漫性星形细胞瘤,需要更谨慎:肿瘤分级更高、生物学更复杂、既往治疗更强、药物穿透血脑屏障与耐药机制也不同。更合理的做法是:将该融合作为潜在治疗线索,在复发/进展或临床试验评估时,与IDH通路一起纳入方案设计。
八、替莫唑胺期间的居家管理:把副作用“提前拦住”
替莫唑胺是许多胶质瘤患者长期需要面对的口服化疗药,副作用并非人人都重,但一旦出现,往往影响生活质量与疗程完成。以下为常见可操作建议(请以主治医嘱为准):
1)血象监测与感染预防
- 为什么要查血常规:替莫唑胺可能导致白细胞/中性粒细胞或血小板下降,增加感染和出血风险。
- 居家怎么做:出现发热(如≥38℃)、咽痛明显、口腔溃疡加重、皮下瘀点增多或鼻出血反复,应尽快联系医生复查血象。
- 日常预防:人群密集处佩戴口罩、勤洗手、避免生食与不洁饮食;口腔护理可用温盐水漱口,减少黏膜损伤。
2)恶心呕吐与食欲下降
- 用药节奏:许多患者在睡前服用、并按医嘱联合止吐药,可减轻白天不适。
- 饮食策略:少量多餐;优先“高蛋白、易消化”食物(鸡蛋、鱼、豆腐、酸奶等);恶心明显时先保证能量与水分,再追求“吃得完美”。
- 警惕脱水:持续呕吐、尿量明显减少或头晕乏力,需尽快就医。
3)疲乏与认知压力
- 把疲乏当成症状管理:固定作息、午间短时休息、轻度活动(散步、拉伸)往往比“完全躺着”更能改善疲乏。
- 记录关键指标:睡眠时长、体重、情绪、癫痫发作情况、止吐药使用次数,能帮助医生更快调整方案。
4)癫痫管理提示
本例以癫痫发作为首发症状。居家需注意:按时服用抗癫痫药、避免熬夜饮酒、家中准备侧卧位防护与发作记录。若发作频率增加、出现新发神经功能缺损(言语、肢体无力、视野改变等),应尽快复诊并复查影像。
九、为什么我们反复强调“全面分子检测”
这例病例之所以能被识别出来,靠的不是某一个单项检测,而是“整合诊断”链条:
- 影像与临床提示弥漫浸润性肿瘤;
- 病理与免疫组化提示高等级星形细胞瘤特征;
- 因为IDH R132H免疫组化阴性但形态学可疑,进一步做NGS;
- NGS发现IDH1 p.R132L,并发现罕见KIAA1549::BRAF融合;
- 再用Sanger与FISH分别验证,确保结果可靠。
对现实中的患者家庭而言,全面分子检测带来的价值是:不仅帮助“分对型”,还可能为复发时的靶向药、临床试验、以及跨中心会诊提供可落地的证据链。
十、下一步你可以怎么做:把信息变成行动
如果你或家人正面对“IDH突变+其他罕见融合/突变”的胶质瘤报告,建议按以下顺序行动:
- 第一步:把资料收齐:手术记录、放疗方案、替莫唑胺剂量与周期、MRI原片与报告、病理报告、免疫组化面板、NGS报告(包含检测方法、覆盖深度、VAF、融合证据)。
- 第二步:做一次高质量解读:尤其是当出现“互斥事件共存”、或免疫组化与NGS不一致时,优先寻求神经肿瘤MDT或有经验的病理/分子肿瘤团队复核。
- 第三步:为后续治疗预留选择:在疾病稳定期就开始了解可及药物与临床试验,避免真正进展时“临时抱佛脚”。
在MedFind,我们更理解患者家属面对复杂分子报告时的无助感。你可以使用我们的AI辅助问诊与治疗方案解读服务,把病理与NGS报告关键点“翻译成可决策的信息”;当医生建议使用海外已上市的前沿药物、而你又受限于获取渠道时,也可以进一步了解我们的抗癌药品跨境直邮服务,以合规、可追溯的方式提升药物可及性。无论你处在初诊、治疗中还是复发评估阶段,最重要的是:让每一次检测结果都能真正服务于下一步治疗选择。
【参考文献】
Das S, Ahlawat S, Nathany S, Gupta RK, Sharma N, Shaikh S, Patir R, Sharma SK. Coexistence of IDH1 Mutation and KIAA1549::BRAF Fusion in a Diffuse Glioma: A Case Report With Clinical, Radiological, and Pathological Correlation. Neuropathology. 2025 Oct;45(5):e70027. doi: 10.1111/neup.70027. PMID: 40968574.

![转移性去势抵抗性前列腺癌治疗新进展:镥[177Lu]特昔维匹肽联合帕博利珠单抗疗效与副作用全解析 7 转移性去势抵抗性前列腺癌治疗新进展:镥[177Lu]特昔维匹肽联合帕博利珠单抗疗效与副作用全解析](https://medfind.link/wp-content/uploads/2026/05/b5eabf912ca30af172ff43ee330147e8.jpg)