很多结直肠癌患者和家属最难接受的,并不是“做完手术、化疗就结束了吗”,而是“明明治疗很积极,为什么还是可能复发”。复发背后常见的一个关键原因,是肿瘤学会了“躲开免疫系统的巡逻”——也就是免疫逃逸。近期一项发表在《Cancer Research》的研究提出:肿瘤细胞里一种叫METTL3的蛋白,可能被某种“化学开关”调到更隐蔽的模式,从而关闭免疫警报,让肿瘤更容易在治疗后卷土重来。本文将用尽量通俗的方式讲清:这个机制是什么、它和常用化疗药5-氟尿嘧啶有什么关联、对免疫治疗(免疫检查点抑制剂)可能意味着什么,以及患者能做哪些更有把握的下一步。
一、结直肠癌复发:为什么“清干净了”还会回来?
结直肠癌(CRC)是全球常见恶性肿瘤之一。对很多患者来说,根治性手术+基于5-氟尿嘧啶的辅助化疗,是非常标准、也确实能显著降低复发风险的策略。但临床现实仍然是:即便完成根治性治疗,仍有一部分患者会在后续面临复发风险;晚期患者(Ⅳ期)复发或进展风险更高,整体预后也更棘手。
从机制上看,复发并不只是“残留了几颗肿瘤细胞”这么简单。更重要的是:肿瘤细胞与免疫微环境之间会持续博弈。如果肿瘤能把周围环境改造成“免疫抑制型”,即使体内还有免疫细胞,也可能识别不到、打不过,最终导致复发或转移。
因此,现代肿瘤治疗越来越重视两件事:
- 肿瘤本身有什么“开关”在驱动它变得更狡猾;
- 免疫系统为什么没有及时拉响警报,以及能不能把警报重新打开。
二、先把概念讲明白:METTL3、m6A与“表观遗传”到底是什么?
很多患者会在文章里看到“表观遗传”“甲基化”“m⁶A”等词,听起来非常遥远。你可以把它们理解为:不改变DNA“文字内容”,但通过添加或去除“标点符号/荧光标记”,来影响细胞读不读、怎么读这些文字。
1)表观遗传:像“系统设置”
同一个人的不同细胞(肝细胞、肠上皮细胞、免疫细胞),DNA序列几乎一样,但功能完全不同,就是因为细胞对基因的“开关设置”不同。肿瘤细胞会利用这些设置,让自己更能生长、转移,并学会逃避免疫。
常见的表观遗传调控包括:DNA甲基化、组蛋白修饰、以及RNA层面的修饰。
2)m6A:RNA上的“可拆卸标签”
m⁶A是一种发生在RNA上的化学修饰。RNA可以理解为“基因信息的快递单”,决定细胞生产哪些蛋白、生产多少、持续多久。m⁶A就像贴在快递单上的“处理标签”,会影响这张快递单是被保留、被加速使用,还是被更快丢弃。
METTL3是m⁶A修饰体系中非常核心的“写入者”之一,负责把m⁶A标签写到RNA上。肿瘤细胞一旦利用这套体系,就可能在不改变DNA的情况下,迅速改写自己的生存策略。
三、研究核心发现:METTL3的K513“二甲基化”,可能让肿瘤更会躲
这项研究聚焦在一个非常具体但重要的点:METTL3蛋白在赖氨酸513(K513)位点的二甲基化。可以把它看作METTL3身上的一个“功能开关”。
研究给出的主要链条是:
- SETD1A催化METTL3在K513位点发生甲基化(更具体为二甲基化)。
- 这种修饰让METTL3与S-腺苷甲硫氨酸(SAM)的结合亲和力增强。SAM可以理解为甲基化反应常用的“甲基供体燃料”。
- 结果是:METTL3更容易推动RNA上的m⁶A沉积(贴更多“处理标签”)。
为什么这会影响免疫?关键在于:研究认为这会抑制内源性逆转录元件相关转录本的表达,并进一步导致I型干扰素反应受损,最终帮助肿瘤实现免疫逃逸。
你可以把“内源性逆转录元件”理解为:人体基因组里一些远古病毒样的“遗迹”。当它们被表达出来时,免疫系统常常会把这种信号当成“病毒入侵”,从而拉响警报,启动I型干扰素等先天免疫反应。而肿瘤如果能让这些信号更安静,免疫系统就更不容易发现异常。

四、它和化疗药5-氟尿嘧啶有什么关系?
研究还提到:氟尿嘧啶诱导了E2F4/SETD1A/METTL3调控轴。其中E2F4通过自我调节激活SETD1A,进而驱动METTL3甲基化。
这里需要非常谨慎地解读:
- 这并不等于“5-氟尿嘧啶会导致复发”或“不能用5-氟尿嘧啶”。5-氟尿嘧啶仍然是结直肠癌治疗的重要基石之一。
- 更合理的理解是:在某些情境或某些肿瘤生物学背景下,肿瘤细胞可能会通过这条轴,形成一种“对免疫更不友好”的适应性改变。
- 这类发现的价值,往往在于为后续的联合治疗提供线索:如何在不牺牲化疗收益的前提下,减少肿瘤的免疫逃逸。
五、对免疫治疗的启发:为什么“联合”可能更关键?
很多患者会搜索“结直肠癌免疫治疗有效吗”。现实是:结直肠癌并非所有人都对免疫检查点抑制剂(ICB)敏感,尤其是一些免疫“冷肿瘤”。但对于特定分子分型人群(例如临床上常讨论的某些高突变负荷/特定修复缺陷类型),免疫治疗可以带来非常显著的获益。
这项研究的启发在于:如果肿瘤通过METTL3相关机制“关掉免疫警报”,那么单用ICB可能不够。研究显示:通过药理学抑制E2F4或基因层面敲除METTL3甲基化,联合ICB,可显著抑制肿瘤生长。
对患者的通俗意义是:
- ICB更像是“松开免疫刹车”,让免疫细胞敢打。
- 但如果肿瘤把“报警器”和“探照灯”都关了,免疫细胞可能“找不到目标”。
- 因此未来可能需要“先把警报打开/把肿瘤变热”,再配合ICB松刹车,形成更强的组合拳。

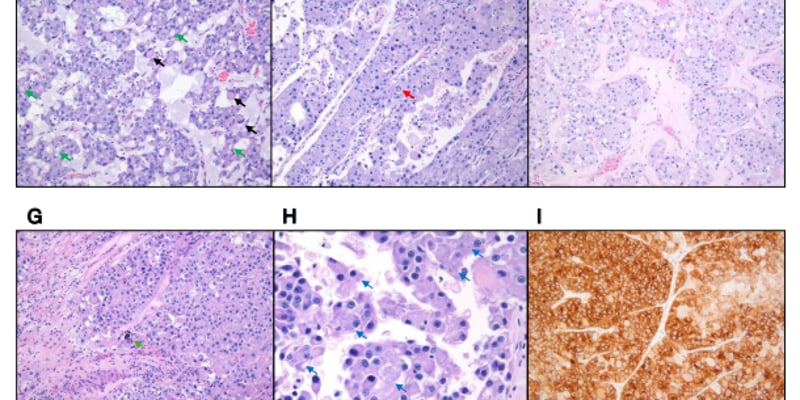
METTL3赖氨酸甲基化与结直肠癌进展和复发相关
六、这些靶点现在能用药吗?患者要避免哪些误区?
很多家属看到“E2F4抑制”“METTL3甲基化靶向”“SETD1A”会立刻问:有没有现成药?能不能马上用?
就目前公开信息和临床常规而言,这些更偏向机制研究与潜在药物研发方向,距离成为结直肠癌标准治疗的“成熟药物方案”,通常还需要:
- 明确可成药的抑制剂或干预方式;
- 动物实验以外的人体安全性与有效性数据;
- 不同分型结直肠癌的获益人群筛选(生物标志物);
- 与现有治疗(化疗、靶向、ICB)的最佳联用顺序与剂量探索。
务必避免的误区:
- 把“实验研究发现”直接等同于“临床已经证明有效”。
- 自行寻找所谓“METTL3抑制剂”“表观遗传特效药”进行非正规用药。
- 因为看到某条机制就否定标准治疗(例如擅自停用医生建议的化疗方案)。
更稳妥的做法,是把这些信息转化为“与医生讨论的高质量问题”,例如:
- 我的肿瘤分型是否可能从免疫治疗中获益?是否做过MSI/MMR等相关检测?
- 如果考虑免疫治疗或临床试验,是否需要更全面的分子检测来筛选人群?
- 我目前的治疗顺序里,是否存在“先让肿瘤变热再上ICB”的策略空间?
七、治疗之外:复发焦虑期,患者最该做的3件事
机制再前沿,落实到生活里,患者最需要的是“我今天能做什么”。以下建议不替代医生诊疗,但对大多数结直肠癌患者更具可操作性。
1)把随访做成“早发现”的保险
复发并非一夜之间发生。规律随访的价值在于:一旦出现复发或转移,往往还能争取到更多治疗选择。建议把随访计划(时间、项目、地点、检查报告归档)做成清单,并固定家属共同管理。
2)化疗常见副作用的居家处理要具体
以5-氟尿嘧啶相关治疗为例,患者常见困扰包括乏力、食欲下降、口腔黏膜不适、腹泻、手足皮肤问题等。居家可以把握几个原则:
- 腹泻:优先补液与电解质;记录次数与性状;若出现发热、血便、明显脱水或持续加重,应尽快就医,避免延误感染或严重肠炎。
- 口腔黏膜不适:餐后温和漱口,避免辛辣酒精;选择软烂食物;疼痛明显影响进食时及时与医生沟通(可能需要局部用药或营养支持)。
- 饮食:少量多餐、优先高蛋白(鱼、蛋、豆制品、瘦肉)+易消化碳水;腹泻期减少高脂和高纤维刺激食物。
- 警惕信号:持续高热、无法进食饮水、尿量明显减少、意识改变、胸闷气促等,属于需要立即就医的危险信号。
3)把“复发恐惧”转化为可执行计划
复发焦虑很常见。有效的方法不是强迫自己不想,而是把担忧拆成行动:
- 把所有病理、影像、用药、基因检测报告按时间线整理;
- 准备二次会诊的问题清单(治疗目标、替代方案、临床试验机会、预期不良反应与处理);
- 建立支持系统:固定一位家属做信息管理员,减少患者反复搜索带来的焦虑。
八、如果你想追上前沿:哪些信息最值得补齐?
这类“肿瘤如何关闭免疫警报”的研究,最终要服务于精准分层与联合治疗。对患者来说,最关键的不是背下每个分子名,而是明确自己是否有机会进入更匹配的方案。
你可以优先补齐的信息包括:
- 完整病理与分期(肿瘤位置、分化程度、淋巴结情况等)。
- 关键分子检测(是否做过与免疫治疗选择相关的检测项目,由主治医生结合病情决定)。
- 既往用药史与不良反应史(决定后续联合方案耐受性)。
- 是否有临床试验机会(尤其是表观遗传调控、免疫联合等方向)。
九、MedFind能为你做什么:把“看不懂的前沿”变成“走得通的方案”
对结直肠癌患者家庭来说,信息差往往就是时间差。很多新机制、新药物、新联用思路,短期内未必立刻进入本地常规路径,但你依然可以提前做好准备:理解方向、筛选适合人群、评估可及性与风险。
MedFind的价值在于:
- AI辅助问诊与治疗方案解读:把病理、分期、既往治疗与报告整合,帮助你形成更清晰的就医提问清单与治疗理解框架,减少“听不懂、问不到点”的挫败。
- 前沿药物与治疗信息梳理:持续跟踪全球研究进展,帮助你判断哪些属于机制阶段、哪些已进入临床试验或指南讨论。
- 抗癌药品跨境直邮:当医生评估后确有合规用药需求时,提供更可及的获取路径支持(以医生建议与当地法规为前提)。
如果你愿意迈出下一步,建议先做两件小事:第一,把现有检查与治疗资料按时间线整理齐;第二,列出你最关心的3个问题(复发风险、下一步治疗选择、免疫治疗/临床试验机会)。当信息变得结构化,选择就会变得更清晰。
参考信息:METTL3 Methylation Induces Decay of Endogenous Retroelement Transcripts to Promote Tumor Immune Evasion. Cancer Research. DOI:10.1158/0008-5472.CAN-25-2893