当“肺腺癌”这三个字被宣判时,无数患者和家庭的内心都会经历一场剧烈的震荡。肺癌,特别是肺腺癌(LUAD),长期以来都是全球癌症相关死亡的首要原因,它的隐匿性、侵袭性以及治疗后的复发与转移,让无数人深感无力。尽管医学科技飞速发展,但癌症的“狡猾”之处,往往在于它的肿瘤内异质性(ITH)——同一肿瘤内癌细胞的“千变万化”,这使得单一疗法难以一劳永逸。面对这样的困境,我们比以往任何时候都更渴望找到突破性的研究,为早期患者带来根治的希望,为晚期患者提供更有效的选择。
今天,我们将深度解读一项来自中国科学院上海营养与健康研究所和上海长征医院团队的重磅研究。这项发表在国际顶尖期刊《Science Advances》上的发现,不仅系统性地揭示了早期肺腺癌中肿瘤异质性的形成机制,更重要的是,它鉴定出了两个能“重编程”癌细胞、抑制肿瘤进展的关键“开关”:Krüppel样因子4(KLF4)和Jun二聚化蛋白2(JDP2)。这项研究为我们理解早期肺腺癌的复杂性打开了一扇窗,也为未来的精准治疗指明了新的方向。
肺腺癌:隐匿的威胁与多变的敌人
肺腺癌(LUAD)是肺癌中最常见的组织学亚型,约占所有非小细胞肺癌的40%。它通常起源于肺部的腺体细胞,可以在肺的任何部位生长,但更常见于肺的外部区域。与其他类型的肺癌相比,肺腺癌在早期可能没有明显症状,这使得早期诊断充满挑战。然而,一旦确诊,其面临的最大威胁之一就是肿瘤内异质性(ITH)。
肿瘤内异质性(ITH)——癌症治疗的“变脸术”
想象一下,您正在与一群敌人作战,但这些敌人并非铁板一块,它们有的高大威猛,有的身形敏捷,有的擅长远程攻击,有的则精通伪装。当您研发出一种武器专门对付高大威猛的敌人时,那些敏捷或擅长伪装的敌人却得以幸存,并可能迅速繁衍壮大,最终导致您的战役失败。这就是肿瘤内异质性(ITH)在癌症治疗中的真实写照。
ITH指的是在同一个肿瘤内部,癌细胞在基因、表型和行为上存在显著差异。这些差异可能源于:
- 基因突变: 癌细胞在分裂过程中不断积累新的基因突变,产生具有不同基因型的亚克隆。
- 细胞可塑性: 肿瘤细胞能够根据微环境信号,动态地改变其表型和功能状态,就像“变色龙”一样。
- 细胞分化状态: 肿瘤细胞可能重新获得干细胞样特性,并通过自我更新和分化形成不同的细胞谱系。
ITH的存在,是导致肿瘤转移、治疗耐药和疾病复发的关键因素,它极大地增加了癌症治疗的复杂性。在临床上,这意味着针对肿瘤某一特定特征的药物,可能无法有效杀灭所有癌细胞,从而留下“漏网之鱼”,导致治疗失败。尽管ITH在晚期癌症中已得到广泛研究,但其在早期癌症中的起源和作用机制,以及如何有效干预,此前仍是未解之谜。
突破性发现:一个能“重编程”癌细胞的“抑制性过渡状态”
中国科学院上海营养与健康研究所王跃祥研究员和上海长征医院唐华教授团队的研究,正是聚焦于早期肺腺癌(LUAD)的肿瘤内异质性(ITH),并取得了令人振奋的突破。
创新技术:单细胞与空间转录组学
为了深入揭示早期肺腺癌的奥秘,研究团队采用了最前沿的技术手段——单细胞及空间转录组学分析。这两种技术结合起来,就像拥有了一台超高分辨率的“生物显微镜”,不仅能以前所未有的精度逐个分析肿瘤中的每一个细胞(单细胞),还能在保留细胞原始空间位置信息的同时,分析基因表达情况(空间转录组学)。通过对14例早期磨玻璃结节样肺腺癌(LUAD)患者、共计103,375个细胞的详细分析,研究人员系统性地定义了肿瘤状态,并首次证实了在早期肺腺癌中,转录层面的ITH普遍存在。

早期肺腺癌的单细胞及空间转录组学分析
细胞可塑性:肿瘤细胞的“变形金刚”能力
研究发现,在早期肺癌的ITH形成中,上皮可塑性扮演了关键角色。什么是上皮可塑性?简单来说,就是上皮细胞(包括肿瘤细胞)能够改变其原有的分化状态,向低分化状态转变(变得更像“原始”细胞,更具侵略性),或者进行“转分化”(从一种细胞类型转变为另一种细胞类型)。这种能力就像“变形金刚”,让肿瘤细胞得以适应各种环境压力,逃避治疗。
更重要的是,研究团队在肺泡II型(AT2)细胞向肺泡I型(AT1)细胞转分化过程中,发现了一个独特的“过渡状态”。肺泡II型细胞被认为是肺腺癌的起源细胞。令人惊喜的是,在这个特定的过渡状态中,肿瘤抑制通路和基因竟然被激活了!这意味着,癌细胞在向更具侵略性的方向演变过程中,会短暂地经过一个“脆弱期”或“抑制期”,在这个时期内,它们体内的“刹车系统”被重新启动,提示着肿瘤细胞可能遵循着某种正常的发育约束。
两大“关键调控员”:KLF4与JDP2的奇迹
这个“抑制性过渡状态”的发现,犹如在迷雾中点亮了一盏明灯。如何利用它来对抗癌症呢?研究团队通过整合多项高通量数据(scRNA-seq、CUT&Tag及批量RNA-seq),深入挖掘,最终鉴定出了两个能将肺腺癌(LUAD)细胞“重编程”到这个有益的过渡状态,并抑制其进展的关键转录因子——Krüppel样因子4(KLF4)和Jun二聚化蛋白2(JDP2)。
转录因子,可以理解为细胞中的“总指挥”或“开关”,它们能够结合到基因的特定区域,从而调节基因的表达,决定细胞是“听话”还是“叛逆”。这项研究激动人心的发现是:
- 过表达KLF4和JDP2:在晚期肺腺癌细胞中,如果人为地增加这两个因子的表达,癌细胞就能被“逆转”到那个具有肿瘤抑制活性的过渡表型。
- 驱动细胞分化:它们能促使癌细胞向正常的AT1谱系分化,使其回归到更接近正常细胞的状态。
- 抑制肿瘤增殖:最终,这种“重编程”导致肿瘤细胞的增殖能力被显著抑制。
这就像找到了控制癌细胞“变身”的关键密码。如果我们能够精确地调控KLF4和JDP2的活性,就有可能将癌细胞从“恶性”状态扭转回来,进入一个“良性”或至少是“抑制性”的过渡状态,从而减缓甚至阻止肿瘤的生长和恶化。
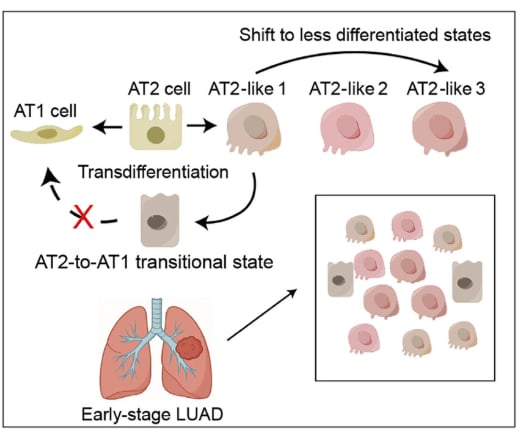
KLF4和JDP2介导肺腺癌重编程及进展抑制机制模式图(图片源自《Science Advances》)
这项研究对肺癌患者意味着什么?
这项突破性研究的意义远不止于科学发现本身,它为肺腺癌的治疗带来了革命性的新视角和无限可能:
-
早期干预的新策略
- 研究首次系统性地定义了早期肺腺癌(LUAD)的肿瘤内异质性(ITH)图谱,并揭示了细胞谱系发育是ITH的关键贡献因素。这意味着,我们对早期癌症的认识不再局限于表面的大小和浸润程度,而是深入到细胞内部的“基因指令”层面。理解ITH的形成机制,为在疾病早期阶段就进行干预提供了理论基础。未来,针对早期病变中这些“开关”的检测和调控,可能成为阻止肿瘤进展的关键。
-
靶向上皮可塑性的精准疗法
- 鉴定了KLF4和JDP2这两个关键转录因子,为开发靶向上皮可塑性的新疗法提供了明确的靶点。传统的靶向治疗通常针对癌细胞的某个异常基因突变或蛋白表达,但当癌细胞“变脸”时,这些疗法就会失效。而通过调控KLF4和JDP2,我们有望“命令”癌细胞改变其分化状态,使其变得不再那么“恶性”,甚至重新激活自身的肿瘤抑制通路。这是一种全新的、从源头“改造”癌细胞的治疗思路,有望克服由ITH带来的治疗耐药问题,实现更持久的疗效。
-
重塑肿瘤微环境的可能
- 研究不仅关注肿瘤细胞本身,还暗示了细胞分化状态的改变可能影响其与周围微环境的互动。如果能将癌细胞“重编程”到抑制性过渡状态,它可能不再是微环境中的“破坏者”,而是“和平共处者”,从而抑制肿瘤的生长和转移。未来,将这种细胞重编程策略与免疫疗法或其他靶向疗法结合,有望产生协同效应。
-
个体化治疗的未来
- 由于每个患者的肿瘤都具有独特的异质性特征,这项研究强调了未来治疗需要更加个性化。通过对患者肿瘤进行单细胞层面的精准分析,识别其细胞分化状态和KLF4/JDP2的表达情况,医生可以为患者量身定制最合适的“重编程”治疗方案。
这项研究为肺癌,特别是早期肺腺癌的治疗带来了革命性的希望。它告诉我们,即使是最顽固的癌症,也可能有其“软肋”,关键在于我们能否找到并精准打击。从“杀灭”癌细胞到“改造”癌细胞,这无疑是抗癌策略的一次重大飞跃。
MedFind:点亮抗癌之路的灯塔
每一次突破性的医学研究,都承载着无数患者对生的渴望。但对于身处信息鸿沟中的患者和家属而言,如何及时了解这些前沿进展,并将其转化为实际的治疗方案,往往是巨大的挑战。MedFind,正是为了打破这种信息壁垒而生,致力于成为您抗癌路上的“信息导航员”和“希望传递者”。
这项关于KLF4和JDP2的重磅发现,正是我们MedFind平台所关注的核心内容之一。我们深知,当一项新的研究成果发布时,患者最关心的是:“这对我意味着什么?我能从中受益吗?如何才能获得这些最新的治疗机会?”
MedFind为您提供:
- 全球抗癌资讯深度解读: 我们将晦涩难懂的医学文献,精准转化为您能看懂、信得过的“救命指南”,确保您第一时间掌握全球最前沿的抗癌进展,如同这篇对肺腺癌重编程研究的深度剖析。
- AI辅助问诊与治疗方案解读: 面对日新月异的治疗方案和复杂的医学术语,我们的AI工具能帮助您理解自身病情,评估潜在的新疗法,并解读这项“重编程”研究未来可能带来的治疗策略,为您提供个性化的参考建议。
- 抗癌药品跨境直邮服务: 尽管KLF4和JDP2相关的疗法尚处于研发阶段,但历史经验告诉我们,突破性的研究最终会催生新的靶向药物。MedFind致力于汇聚全球已获批上市的创新抗癌药物信息,并通过合规的跨境直邮服务,让您有机会更早地接触到全球最新、最有效的治疗选择。我们相信,对最新科研的了解,是为未来做好准备的第一步。
癌症的道路充满挑战,但医学的进步从未停止。每一次突破,都为我们带来新的希望。MedFind将始终与您并肩,为您汇聚全球抗癌智慧,消除信息“边界”与“时差”,让每一位患者都能有机会触及生命的曙光。
参考文献
Yuexiang Wang et al. Epithelial plasticity shapes intratumoral heterogeneity and cell lineages in early-stage lung cancer. Science Advances, 2026-03-06. DOI: 10.1126/sciadv.ady8546

![转移性去势抵抗性前列腺癌治疗新进展:镥[177Lu]特昔维匹肽联合帕博利珠单抗疗效与副作用全解析 3 转移性去势抵抗性前列腺癌治疗新进展:镥[177Lu]特昔维匹肽联合帕博利珠单抗疗效与副作用全解析](https://medfind.link/wp-content/uploads/2026/05/b5eabf912ca30af172ff43ee330147e8.jpg)