对于许多晚期癌症患者及家属而言,“CAR-T细胞疗法”这个词或许并不陌生。这种被誉为“抗癌神药”的技术在白血病、淋巴瘤等血液肿瘤领域创造了无数生命奇迹。然而,当面对胃癌、结直肠癌、肺癌等实体瘤时,CAR-T疗法的表现却一直差强人意。肿瘤内部复杂的环境、缺乏精准靶点、药物难以进入病灶,像是一道道“防火墙”挡住了免疫细胞的进攻。近日,浙江大学医学院附属第一医院方维佳教授团队的一项研究为这一困局带来了曙光。
Nature Cancer重磅发布:让CAR-T细胞学会“智能作战”
2026年2月27日,国际顶级学术期刊《Nature Cancer》(影响因子高达28.5)在线发表了一项突破性研究。由浙江大学方维佳教授、重庆精准生物技术有限公司钱程教授及杨智教授共同主导的1期临床试验显示,一种名为PC13(癌胚抗原靶向CAR-T细胞)的新型疗法,在治疗晚期CEA阳性实体瘤中展现出了令人振奋的安全性和初步疗效。

为什么实体瘤治疗这么难?
在血液肿瘤中,肿瘤细胞散布在血液里,CAR-T细胞能轻松找到并“消灭”它们。但实体瘤不同,它像一个设防森严的堡垒,内部存在严重的缺氧(Hypoxia)、酸性代谢物堆积以及免疫抑制屏障。这些因素不仅限制了T细胞的浸润,还会让进入其中的免疫细胞迅速“耗竭”。此外,许多肿瘤靶点在正常组织中也有少量表达,如果CAR-T细胞敌我不分,就会产生严重的副作用。
PC13:自带“缺氧传感器”的精准导弹
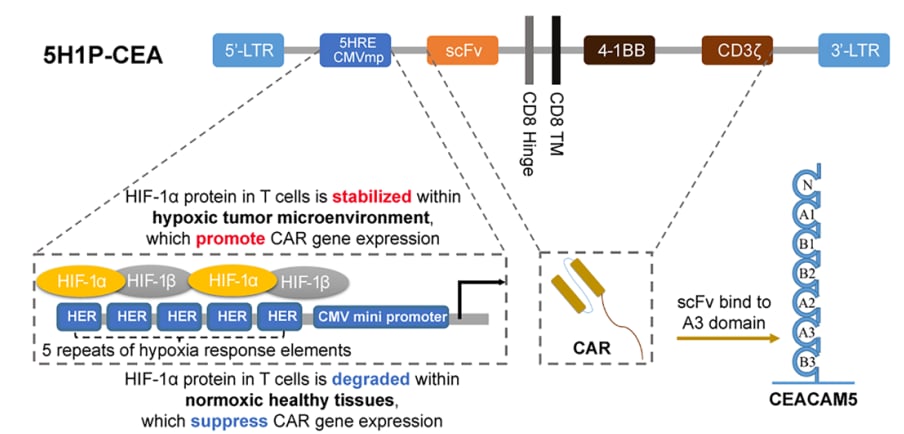
为了解决上述痛点,研究团队对PC13进行了智能化改造。其核心秘密在于引入了“缺氧响应元件(HRE)”组成的启动子。
- 在健康组织中(常氧状态):PC13中的CAR基因处于“休眠”状态,HIF-1α蛋白迅速降解,免疫细胞不会被激活,从而最大程度保护了正常器官。
- 进入肿瘤组织后(低氧环境):缺氧触发了“开关”,HIF-1α稳定并激活CAR表达。此时,PC13迅速苏醒,释放强大的杀伤力。
这种“在体内循环时静止,在肿瘤局部触发”的设计,不仅降低了脱靶毒性,还避免了T细胞在抵达战场前无谓的消耗。在MedFind平台上,不少患者及家属对此类前沿技术表现出高度关注,这正是因为它精准切中了传统化疗“伤敌一千,自损八百”的痛点。
CEA(癌胚抗原):定位肿瘤的精准坐标
癌胚抗原(CEA)是临床上非常常用的肿瘤标志物。它在结直肠癌、胃癌和肺癌中高度表达。正常情况下,它仅存在于肠道粘膜的特定位置,但在癌变后,它会遍布整个细胞表面。PC13正是针对这一特征,实现了对癌细胞的精准定位。
突破给药屏障:腹腔与静脉的双重围剿
对于许多消化道肿瘤患者来说,“腹膜转移”是治疗的难点,因为血液中的药物很难穿过血液-腹膜屏障。本研究采用了一个极具创新性的策略:腹腔输注。
研究人员将PC13直接灌注入腹腔,使免疫细胞能“面对面”地杀伤腹腔内的转移病灶。令人惊喜的是,研究发现这些局部激活的细胞并没有局限在腹腔,它们可以通过淋巴或血液循环重新进入全身,实现“局部打击、全身响应”的效果。这种双路径给药策略,为那些存在严重腹水的晚期患者提供了全新的思路。
临床数据解读:安全可控,初见成效
在1期临床试验中,参与者多为经过多线治疗失败(重度预处理)的CEA阳性实体瘤患者。结果显示:
- 安全性:PC13展示了可控制的毒性。对于患者最担心的细胞释放综合征(CRS),在精准的剂量调控下处于安全范围。
- 疗效趋势:强劲的CAR-T细胞扩增与延长的无进展生存期(PFS)表现出正相关。PFS即患者在治疗后肿瘤不进展的时间,这直接关系到患者的生活质量和生存尊严。
- 受益人群:癌胚抗原的表达水平和转移部位是决定治疗效果的关键。这意味着,通过MedFind提供的辅助问诊与治疗方案解读,患者可以更精准地匹配适合自己的前沿临床研究。
结语:从“强力攻击”到“智能调控”
这项研究标志着实体瘤CAR-T疗法正迈向一个新阶段。不再是单纯增加细胞的“火力”,而是赋予其识别环境的“智慧”。虽然这目前仍处于临床研究阶段,但它为晚期复发难治性实体瘤打开了一扇窗。对于正身处迷茫中的患者及家属,保持对前沿资讯的关注,了解最新的药物机制与临床招募信息,或许就是通往康复的关键一步。
参考文献
方维佳, 钱程, 杨智, et al. Hypoxia-responsive CEA-targeted CAR T cells in CEA-positive solid tumors through intraperitoneal or intravenous infusion: a phase 1 trial. Nature Cancer. 2026.