近年来,免疫治疗的兴起为非小细胞肺癌(NSCLC)患者带来了新的希望。其中,PD-L1表达水平是评估患者是否适合接受免疫检查点抑制剂(ICI)治疗的关键生物标志物。然而,在可切除的早期NSCLC中,PD-L1的预测价值仍存在不确定性,尤其是在不同检测方法和肿瘤内部差异(即肿瘤内异质性,简称ITH)的影响下,问题变得更为复杂。对于正在寻求最佳治疗方案的患者及家属而言,理解这些复杂性至关重要。本文将基于一项大规模的最新研究,深入探讨EGFR突变状态如何影响PD-L1的检测结果和肿瘤内异质性,以及这些发现对围手术期免疫治疗决策的深远意义。
非小细胞肺癌(NSCLC)免疫治疗新进展与PD-L1的挑战
免疫检查点抑制剂(ICI)的问世,彻底改变了晚期非小细胞肺癌的治疗格局。如今,其应用已从辅助治疗、新辅助治疗进一步拓展至围手术期治疗,为早期可切除的NSCLC患者带来了治愈的可能。在临床实践中,免疫组织化学(IHC)检测PD-L1表达水平是筛选适合PD-(L)1抑制剂治疗人群的公认指标。PD-L1表达水平越高,患者从免疫治疗中获益的可能性越大。
然而,在早期可切除的NSCLC中,PD-L1作为生物标志物的预测价值尚不明确。例如,IMpower010试验(主要采用SP142检测,部分采用SP263检测)和PEARLS/KEYNOTE-091试验(采用22C3检测)在PD-L1肿瘤比例评分(TPS)≥50%的亚组患者中,研究结局出现了矛盾。这不仅凸显了单一生物标志物检测方法的局限性,也表明不同围手术期试验采用不同的PD-L1抗体检测方法,可能进一步加剧了结果解读的复杂性。
此外,肿瘤内异质性(ITH)是影响PD-L1检测准确性的另一个关键因素。这意味着肿瘤内部不同区域的PD-L1表达水平可能不一致。临床实践中,通常仅从一个肿瘤区域采集组织进行检测,如果该区域的PD-L1表达不能代表整个肿瘤,就可能导致治疗决策的偏差。尤其是在EGFR突变型NSCLC患者中,ICI治疗效果通常不佳,但某些试验的亚组分析又提示部分PD-L1阳性的EGFR突变型患者或能从辅助ICI治疗中获益,这使得PD-L1检测的准确性及对ITH的理解变得尤为重要。
正是在这样的背景下,本文将详细解读一项迄今为止规模最大的研究。该研究旨在深入分析EGFR突变状态对三种不同PD-L1抗体检测结果一致性的影响,评估不同EGFR突变状态下PD-L1 ITH的发生率和预测因素,并探究其对患者生存结局的预后意义,为患者和临床医生提供更精准的决策依据。
深入剖析:不同PD-L1检测方法(SP263、22C3、SP142)的“默契度”
研究方法概览:如何确保检测精准性?
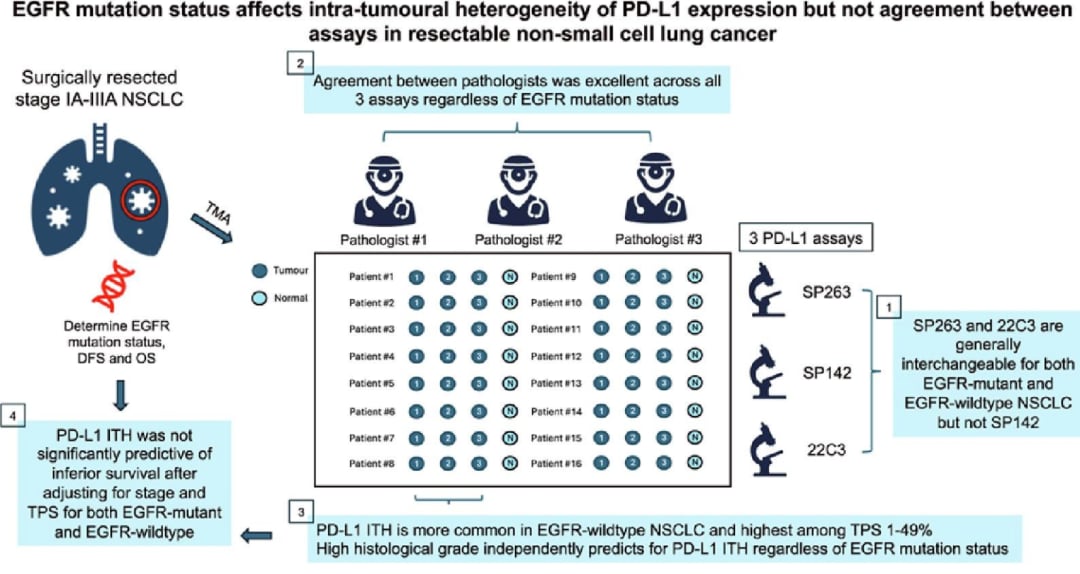
为了全面评估PD-L1检测的复杂性,研究人员精心设计了一项大规模研究。他们纳入了561例可切除的IA-IIIA期非小细胞肺癌(NSCLC)患者,并从每位患者的手术切除标本中,在三个不同的肿瘤区域获取组织穿刺样本,以及一个正常组织样本。这些样本被用于构建组织微阵列(TMA),以确保在标准化条件下进行批量检测。
研究中采用了三种临床上常用的PD-L1抗体/检测方法进行免疫组织化学(IHC)染色,分别是SP263、SP142和22C3。这些检测方法都经过了优化和验证,并设置了阳性和阴性对照,以确保结果的可靠性。随后,由3名对患者临床信息不知情的肺癌病理专家,独立对每个肿瘤穿刺样本的PD-L1肿瘤比例评分(TPS)进行评估。TPS定义为出现部分或完整细胞膜染色的肿瘤细胞占总肿瘤细胞的百分比。
为了更好地贴合临床实践,研究将TPS评分分为三个主要区间:<1%、1%-49%和≥50%。当同一患者的三个肿瘤穿刺组织中,至少有2/3的样本TPS评分在这三个区间内存在不一致时,即被定义为存在PD-L1肿瘤内异质性(ITH)。研究人员通过科恩卡帕检验来评估不同检测方法之间以及不同病理医生之间的一致性,并通过Kaplan-Meier法分析了ITH对患者生存结局的影响。
关键发现一:SP263与22C3高度“合拍”,SP142表现欠佳
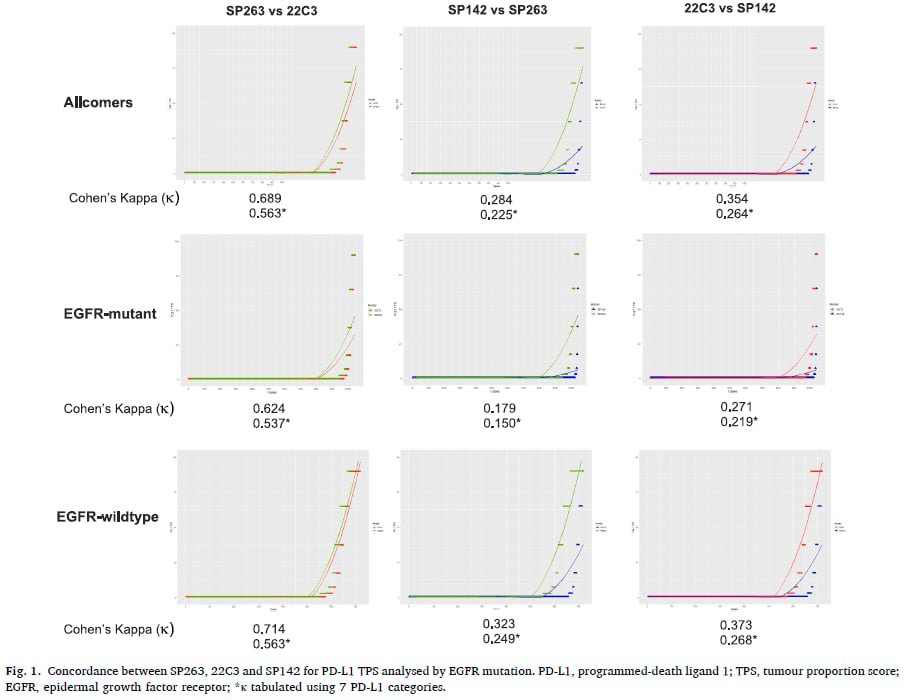
这项研究的一个核心发现,在于对比了三种PD-L1抗体检测方法(SP263、22C3和SP142)之间的一致性。结果显示:
- 在所有患者中,SP263与22C3之间的一致性最高,Kappa值达到了0.689,这表示两者具有中等偏强的一致性。
- 其次是22C3与SP142,Kappa值为0.354,一致性表现一般。
- 而SP263与SP142之间的一致性最低,Kappa值仅为0.284,属于微弱一致。
更重要的是,这种一致性趋势在EGFR突变型和EGFR野生型患者中保持一致,没有明显差异。这意味着无论患者是否携带EGFR突变,SP263和22C3在PD-L1检测结果上都具有较高的可互换性,而SP142与前两者相比,则显得“格格不入”。这一发现对于临床医生选择PD-L1检测方法具有重要的指导意义。
此外,研究还评估了不同病理医生之间的一致性。结果令人欣慰:3名病理医生对同一样本的检测一致性接近完全一致,中位科恩Kappa值达到1(范围0.992-1)。这表明,尽管PD-L1评分是一个主观性较强的任务,但经过专业培训的病理专家之间,对PD-L1表达的判断是高度统一的,观察者之间的差异非常小,进一步保证了研究结果的可靠性。
肿瘤内异质性(ITH):为何有些肿瘤PD-L1表达“变脸”?
关键发现二:EGFR野生型肿瘤PD-L1异质性更高
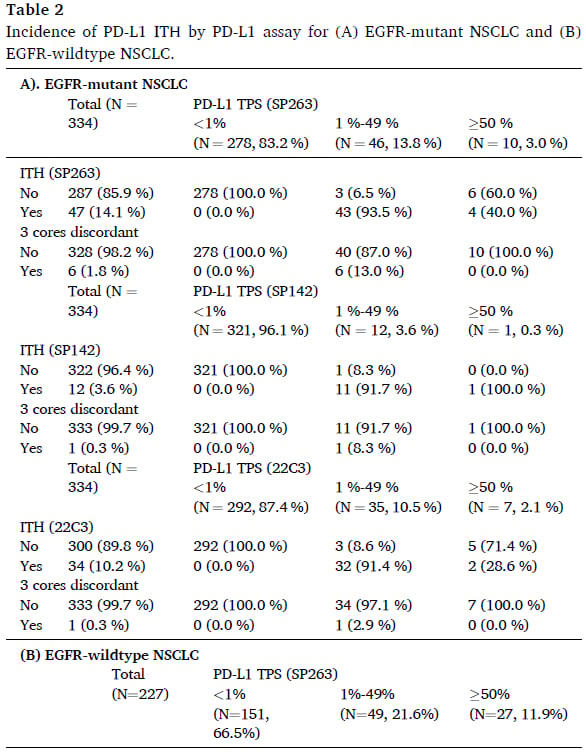
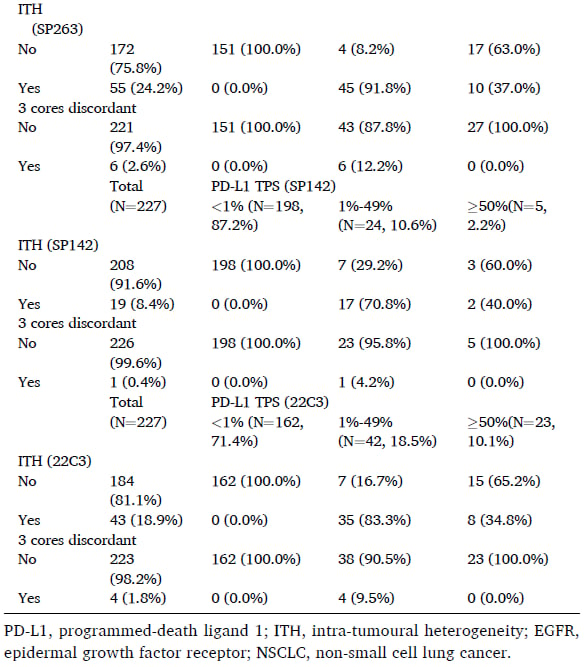
肿瘤内异质性(ITH)是影响PD-L1检测准确性的一个重要因素,它指的是同一肿瘤内部不同区域的PD-L1表达水平可能存在差异。这项研究对此进行了深入分析,并发现:
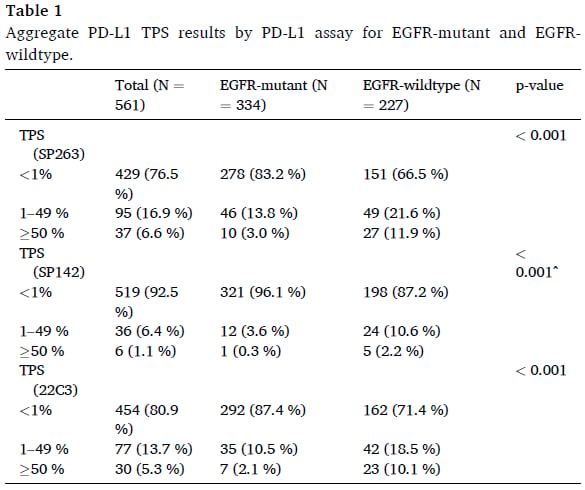
- 在对PD-L1阳性检出敏感性最高的SP263检测方法下,EGFR野生型患者的PD-L1 ITH发生率为24.2%,显著高于EGFR突变型患者的14.1%(p=0.002)。这意味着,对于EGFR野生型NSCLC患者,单次活检的PD-L1检测结果更可能存在偏差,因为它无法完全反映整个肿瘤的真实PD-L1表达状态。
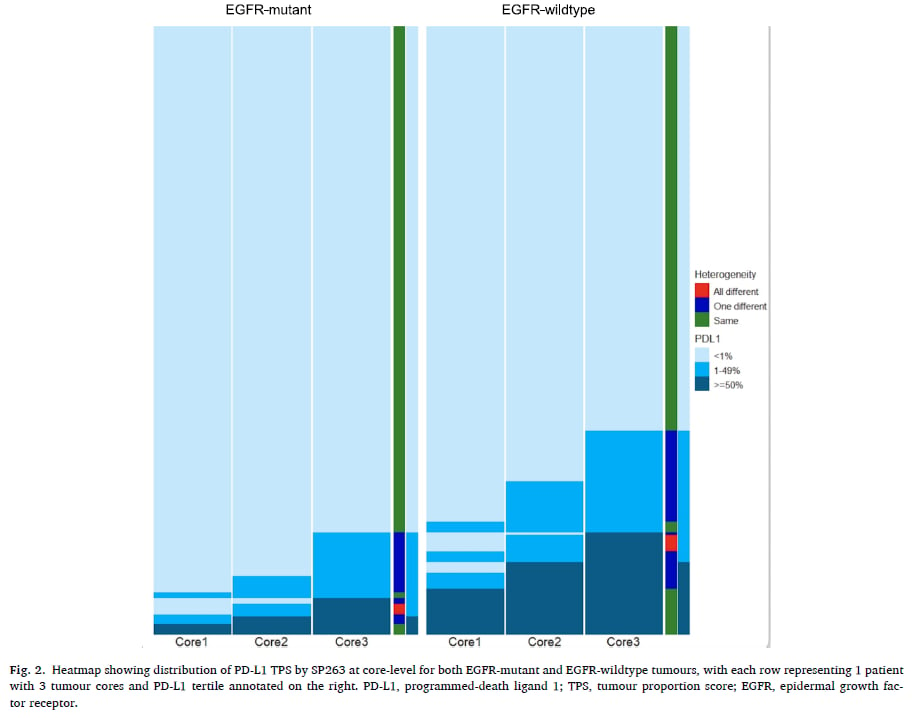
- PD-L1 ITH的发生率在不同的TPS评分区间也存在显著差异:在TPS 1%-49%的肿瘤中,ITH的发生率最高,高达92.6%。这意味着几乎所有PD-L1表达处于中等水平的肿瘤,其内部都可能存在异质性,有些区域PD-L1表达很低(<1%),有些区域则很高(≥50%)。相比之下,TPS≥50%区间的ITH发生率为37.8%,而TPS<1%区间的ITH发生率为0%。
这些数据具有非常重要的临床意义。因为在实际诊疗中,为了降低成本和病理医生的工作量,通常只会采集一个肿瘤穿刺组织进行PD-L1评分。然而,如果肿瘤存在严重的异质性,特别是PD-L1表达介于1%-49%之间的肿瘤,单次活检的结果很可能无法准确代表整个肿瘤的PD-L1状态,从而可能导致医生在围手术期免疫治疗推荐上的误判。
谁是PD-L1异质性的“幕后推手”?
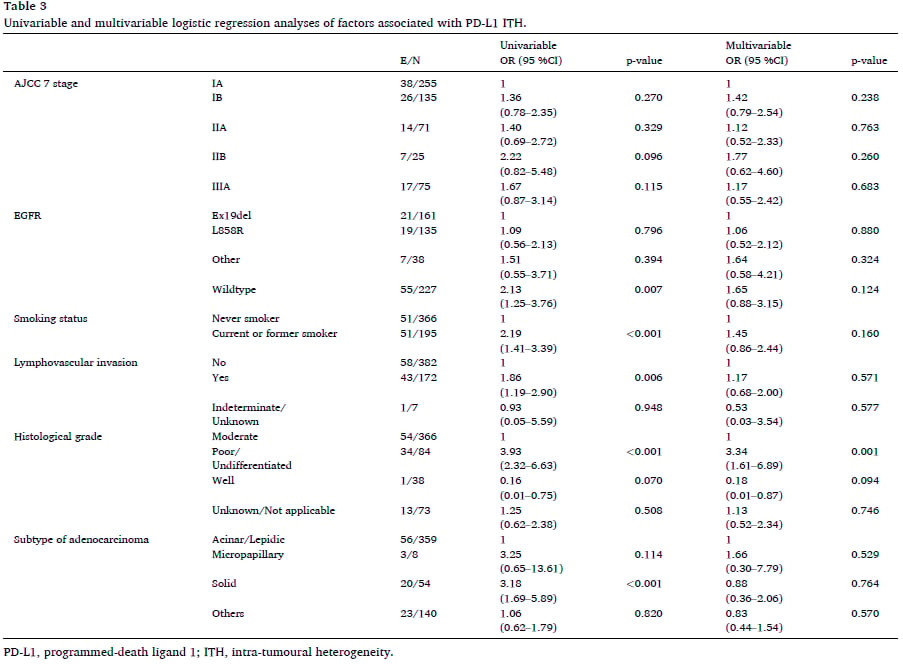
为了探究哪些因素会影响PD-L1的肿瘤内异质性(ITH),研究人员进行了详细的单因素和多因素逻辑回归分析。他们发现:
- 在单因素分析中,EGFR野生型、有吸烟史、存在淋巴管血管侵犯、低分化/未分化肿瘤以及实性腺癌亚型都与PD-L1 ITH显著相关。这表明这些因素可能在一定程度上预示着肿瘤内部PD-L1表达的不均一性。
- 然而,在更严格的多因素分析中,当校正了其他相关因素后,研究显示**组织学高级别(即低分化/未分化肿瘤)是PD-L1 ITH唯一的独立预测因素**。这意味着,如果一个肿瘤的组织学分级较高,其PD-L1表达出现异质性的风险就越大。
这一发现对于病理医生在选择肿瘤活检区域时具有重要的指导意义。对于那些组织学分级较高的肿瘤,病理医生需要更加谨慎,考虑进行多区域活检,以确保PD-L1检测结果能够更准确地反映肿瘤的整体状态,从而为后续的治疗决策提供更可靠的依据。
PD-L1异质性对患者生存结局的影响
这项研究还深入分析了PD-L1肿瘤内异质性(ITH)对患者长期生存结局(包括无复发生存期DFS和总生存期OS)的影响。初步分析结果显示:
- PD-L1 TPS<1%的患者,其DFS和OS均显著优于PD-L1 TPS≥1%的患者。例如,2年DFS分别为79.7%和59.2%,5年DFS分别为64.4%和42.6%;5年OS分别为81.8%和58.5%。这再次强调了PD-L1表达水平对NSCLC患者预后的重要影响。
- 在未经校正的分析中,存在PD-L1 ITH的患者,无论是EGFR突变型还是野生型,其DFS和OS都显著更差。这似乎表明PD-L1异质性与不良预后相关。
然而,当研究人员进一步校正了肿瘤分期、PD-L1 TPS评分和辅助治疗等已知的重要预后因素后,结果发生了变化:**PD-L1 ITH本身与患者的DFS和OS均无显著关联。**这提示我们,虽然PD-L1 ITH可能与一些不良的临床病理特征(如组织学高级别)相关联,但它本身可能不是一个独立的预后因素。PD-L1 TPS评分和肿瘤分期等才是影响患者生存结局的更主要和独立的因素。
此外,研究者还探索性地分析了PD-L1 ITH相关肿瘤微环境的免疫细胞构成。通过多重免疫组织化学检测,对比了PD-L1 TPS评分一致与不一致的肿瘤样本。结果显示,PD-L1表达高的肿瘤(TPS 80%-100%)通常含有更多的CD8+T细胞和CD8+CD39+双阳性T细胞,这些都是抗肿瘤免疫应答的重要组成部分。但令人意外的是,对比PD-L1 TPS评分一致和不一致的肿瘤,并未发现免疫细胞群体构成存在明显差异。这可能意味着PD-L1的异质性更多地体现在肿瘤细胞本身的表达上,而不是免疫细胞的分布差异。
本研究的临床意义与未来展望:MedFind如何助您应对挑战?
这项大规模、多区域活检的研究,为非小细胞肺癌(NSCLC)患者的PD-L1检测和免疫治疗决策提供了宝贵的见解。核心结论包括:
- **PD-L1检测方法选择:** 无论患者的EGFR突变状态如何,SP263和22C3两种PD-L1检测方法的评分结果具有较强的可互换性,而SP142与前两者的一致性较低。这意味着在临床实践中,对于PD-L1检测,选择SP263或22C3可能获得更可靠且一致的结果。
- **EGFR突变与PD-L1异质性:** EGFR野生型肿瘤的PD-L1肿瘤内异质性(ITH)发生率显著高于EGFR突变型肿瘤。这提示医生在评估EGFR野生型患者时,需要对PD-L1检测结果更加谨慎。
- **警惕PD-L1“灰色地带”:** 最值得关注的是,高达92.6%的TPS 1%-49%(即PD-L1表达处于中等水平)的肿瘤存在ITH,其中大部分的相邻穿刺组织PD-L1评分甚至低于1%。这意味着,仅依靠一次单点活检来评估这类患者的PD-L1状态,很可能无法准确反映肿瘤的真实情况,从而影响免疫治疗的决策。
- **PD-L1异质性的预测因素:** 研究明确指出,组织学高级别(低分化/未分化肿瘤)是PD-L1 ITH唯一的独立预测因素。对于这类肿瘤,医生应特别注意其PD-L1检测结果可能存在的异质性。
这些发现对于指导临床医生选择最具代表性的肿瘤穿刺组织进行检测,从而影响新辅助或辅助免疫检查点抑制剂(ICI)治疗的推荐决策,具有深远的意义。鉴于目前临床实践中通常仅采集一个肿瘤区域的组织进行PD-L1评分,这项研究强调了在特定情况下(如组织学高级别或PD-L1 TPS 1%-49%的肿瘤)进行多区域活检的必要性,以提高PD-L1评分的准确性,确保患者能接受最恰当的治疗。
作为癌症患者和家属,面对这些复杂的医学信息和不断更新的治疗方案,往往感到迷茫和焦虑。MedFind致力于为癌症患者提供最新、最权威的抗癌资讯、药物信息和诊疗指南。我们深知精准检测对治疗选择的重要性,因此会持续关注前沿研究,为您解读复杂的医学证据,帮助您更好地理解自己的病情和治疗选项。
尽管本研究具有重要价值,但也存在一些局限性,如单中心、主要针对亚裔华人患者群体,且未评估所有已知的PD-L1抗体。未来的研究将需要更大规模、更多样化的患者群体,并评估其他致癌驱动基因突变对PD-L1检测的影响,以进一步优化PD-L1 TPS评分的准确性,尤其是在可切除NSCLC围手术期治疗策略日益增多,且医保报销政策可能与PD-L1 TPS评分挂钩的背景下。
总之,精准的PD-L1检测是制定有效免疫治疗方案的关键。MedFind将始终与您同行,提供可靠的抗癌资讯,协助您了解国内外最新药物信息,包括跨境购药渠道,并提供AI辅助问诊服务,助您在抗癌征途中做出最明智的决策。
参考文献:
Saw, Stephanie P L et al. “EGFR mutation status affects intra-tumoural heterogeneity of PD-L1 expression but not agreement between assays in resectable non-small cell lung cancer.” Lung cancer (Amsterdam, Netherlands) vol. 202 (2025): 108463. doi:10.1016/j.lungcan.2025.108463