9月22日,第一三共株和阿斯利康官宣:Datopotamab Deruxtecan(Dato-DXd,Trop2 ADC)的乳腺癌III期临床试验达到主要终点之一的PFS(无进展生存期),总生存(OS)的双主要终点数据尚不成熟,试验将按计划继续进行OS的评估。
Dato-DXd一种独特靶向TROP2的DXd抗体-药物偶联物(ADC)。
出处:https://www.astrazeneca.com/media-centre/press-releases/2023/dato-dxd-improved-pfs-in-breast-cancer.html
TROPION-Breast01 III期临床试验中,Dato-DXd对激素受体阳性(HR+)、人表皮生长因子受体2阴性(HER2-)与低表达乳腺癌患者,后线治疗PFS显示统计学意义获益。
TROPION-Breast01 研究是一项全球性、随机、多中心、开放标签的3期临床试验,评估datopotamab deruxtecan与研究者选择的单药化疗(伊瑞布林、卡培他滨、吉西他滨等)在无法手术或转移性HR-阳性、HER2低或阴性(IHC 0、IHC 1+或IHC 2+/ISH-)的乳腺癌患者中的安全性和有效性,这些患者先前已进展或不适合接受内分泌治疗。

TROPION-Breast01 研究双主要终点是经盲法独立中心评价(BICR)评估的PFS和OS。关键的次要终点包括客观缓解率、缓解持续时间、研究者评估的PFS、疾病控制率和首次后续治疗的时间。TROPION-Breast01在亚洲、欧洲、北美、南美和非洲等招募了700多名患者。
2、科伦药业 子公司科伦博泰生物 注射用SKB264相关试验已达主要研究终点:
8月14日,SKB264(MK-2870)是一款靶向人滋养层细胞表面抗原2(TROP2)的新型抗体药物偶联物(ADC),目前研究用于治疗晚期实体瘤,包括TNBC、非小细胞肺癌(NSCLC)及HR+/HER2-乳腺癌(HR+/HER2-BC),科伦博泰生物拥有其自主知识产权。
该试验是SKB264(MK-2870)在中国的首个注册Ⅲ期研究。
SKB264(MK-2870)就治疗局部晚期或转移性TNBC于2022年7月获中国药监局药审中心授予突破性疗法认定。
注射用SKB264对比标准化疗方案,用于既往经二线及以上标准治疗的不可手术切除的局部晚期、复发或转移性三阴性乳腺癌(TNBC)患者的随机、对照、开放性、多中心Ⅲ期临床试验已达到主要研究终点,即独立审查委员会(IRC)评估的无进展生存期(PFS)。
在预先设定的期中分析中,与接受标准化疗的对照组相比,SKB264(MK-2870)在无进展生存期方面有统计学上的显著改善。
因此,根据期中分析结果,科伦博泰生物计划就提交SKB264(MK-2870)的新药申请(NDA)事宜与中国国家药品监督管理局(“中国药监局”)药品评审中心(“药审中心”)进行沟通。
关于Trop2:
TROP2(滋养层细胞表面抗原 2)是一种跨膜糖蛋白,广泛表达于多种实体瘤(包括NSCLC,虽然TROP2在所有肺癌亚型中均发生表达,但在腺癌(64%)和鳞状细胞癌(75%)(NSCLC的最常见形式)中表达最高。
目前尚无TROP2靶向疗法获批用于治疗NSCLC。
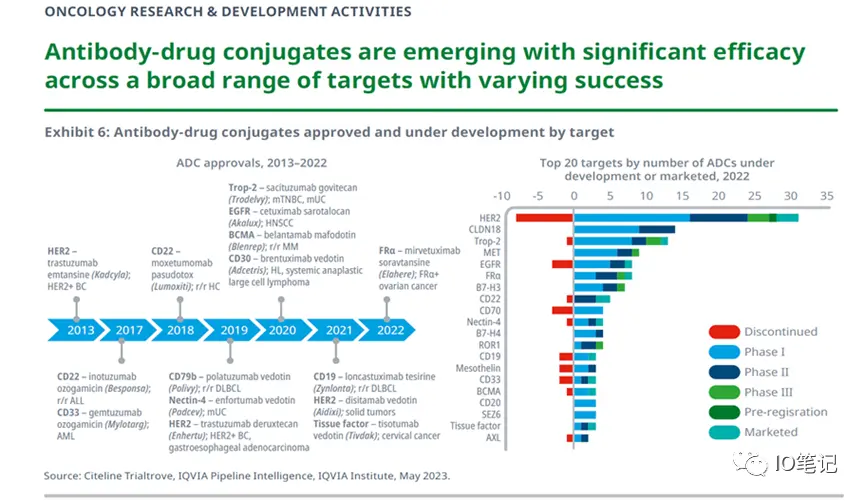
目前HER2、Trop2等ADC药物研发火热。
详见:明日之星?Trop2-ADC还是HER2-ADC?(上篇)(盘点53)
出处:IQVIA Institute, May 2023.侵删!
附:
戈沙妥珠单抗(拓达维,TROP2 ADC)
近日,注射用戈沙妥珠单抗(拓达维,TROP2 ADC)陆续登陆全国各大药店,规格180mg/瓶:8400.00元(仅供参考,具体以医院价格为准,该药为处方药,请在医师处方下合理使用)。
国内适应症为:既往至少接受过2种系统治疗(其中至少一种治疗针对转移性疾病)的不可切除的局部晚期或转移性三阴性乳腺癌成人患者。
戈沙妥珠单抗(英文名:Trodelvy(sacituzumab govitecan-hziy))是一款靶向Trop-2的同类首创抗体偶联药物(ADC)。
2020年首个TROP2 ADC 戈沙妥珠单抗Trodelvy (sacituzumab govitecan)被FDA加速批准批准用于治疗晚期三阴性乳腺癌。后续尿路上皮癌FDA亦获批适应症。2022年6月7日,国家药品监督管理局(NMPA)正式批准云顶新耀戈沙妥珠单抗(拓达维®)用于治疗既往接受过至少两种系统治疗(其中至少一种为针对转移性疾病的治疗)的不可切除的局部晚期或转移性三阴性乳腺癌成人患者。
FDA获批为乳腺癌、尿路上皮癌两个适应症;

出处: FDA 说明书 https://www.accessdata.fda.gov/drugsatfda_docs/label/2023/761115s035lbl.pdf
剂量为:10mg/Kg;21天为一周期;
TROP2在许多实体肿瘤中都过表达,包括乳腺癌,子宫颈癌,结肠直肠癌,食道癌,肺癌,非霍奇金淋巴瘤,慢性淋巴细胞性淋巴瘤,口腔鳞状细胞癌,卵巢癌,胰腺癌,前列腺癌,胃癌等,确实是一个泛癌种过表达的潜在分子。
在许多肿瘤细胞中,Trop2的表达上调,但在正常组织中,Trop2的表达仍然很低,甚至不表达(Wang, Day, Dong, Weintraub, & Michel, 2008)。研究发现,Trop2在调节肿瘤细胞的自我更新、增殖和转化中起着至关重要的作用(Stoyanova et al., 2012)。另外,肿瘤的发展程度与Trop2的表达水平相关,可作为临床检测肿瘤恶性程度的标志物。
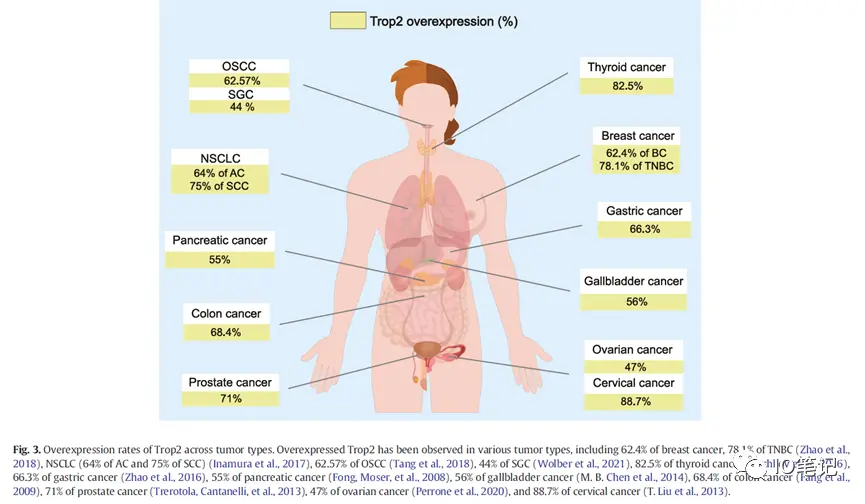
图3所示。Trop2在肿瘤类型中的过表达率。过表达Trop2已经观察到在不同肿瘤类型,其中包括62.4%的乳腺癌,TNBC(三阴性乳腺癌)的78.1%,非小细胞肺癌(腺癌75%;鳞状细胞癌的64%), 62.57%的OSCC, 82.5%的甲状腺癌, 66.3%的胃癌, 55%的胰腺癌, 56%的胆囊癌症,68.4%的结肠癌,前列腺癌71%,卵巢癌47%,宫颈癌88.7%。
出处如下:

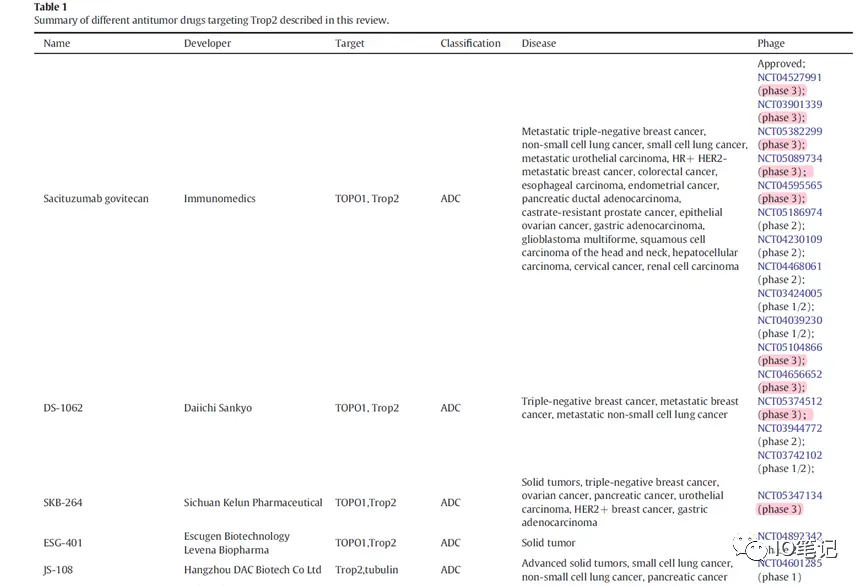
当前针对TROP2药物开发主要集中在ADC药物方向,既有戈沙妥珠单抗Trodelvy (sacituzumab govitecan)FDA获批,也有辉瑞、百奥泰的ADC药物折戟。
临床试验已终止的TROP2 ADC药物;

TROP2相关的ADC新药研发布局(红色标记为3期研发布局);
主要是戈沙妥珠单抗Trodelvy (sacituzumab govitecan)、第一三共&AZ合作的DS-1062、科伦制药的SKB-264等
备注:
Dato-DXd是由阿斯利康和第一三共合作开发的一款TROP2 ADC。
Dato-DXd (Datopotamab deruxtecan; 研发代号DS-1062)是第一三共肿瘤领域管线中的三款核心 DXd 抗体偶联药物(ADC)之一。
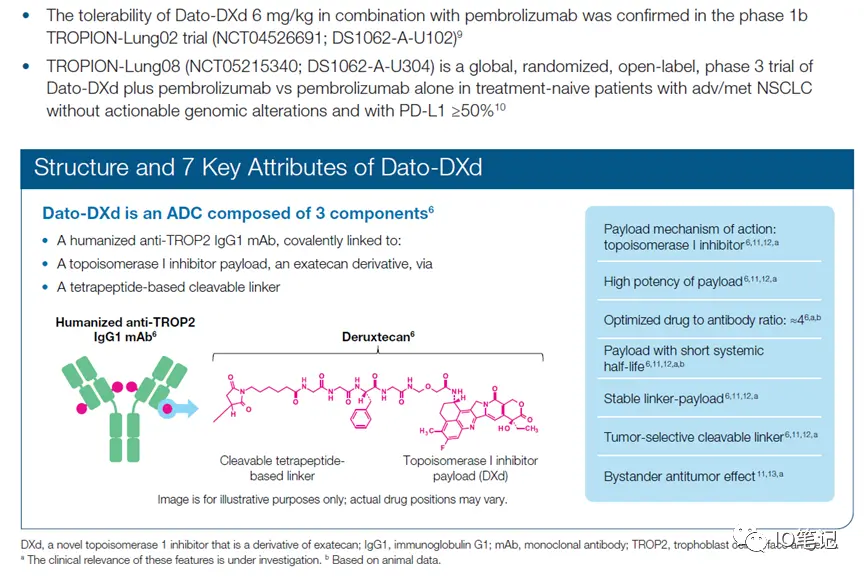
Dato-DXd采用第一三共专有的 DXd ADC 技术设计,由人源化抗 TROP2IgG13单克隆抗体、拓扑异构酶1抑制剂(喜树碱类衍生物)和可裂解的四肽连接子组成,药物抗体比(DAR)为4。
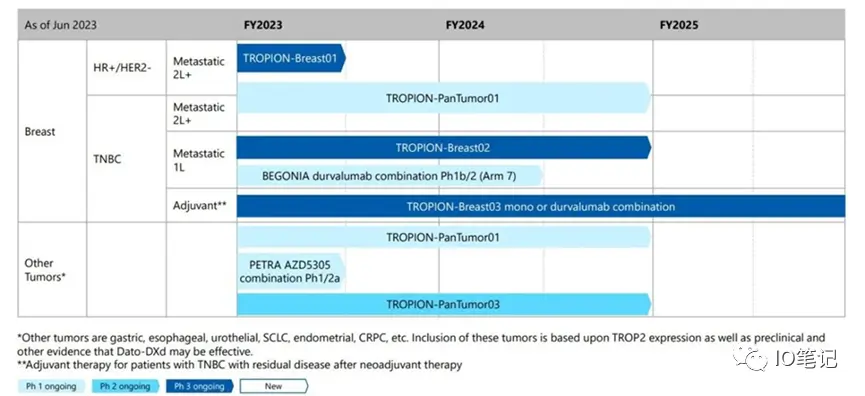
TROPION-Lung Pantumor01
TROPION-Lung Breat01:
HR阳性/HER2低表达或阴性乳腺癌二线等
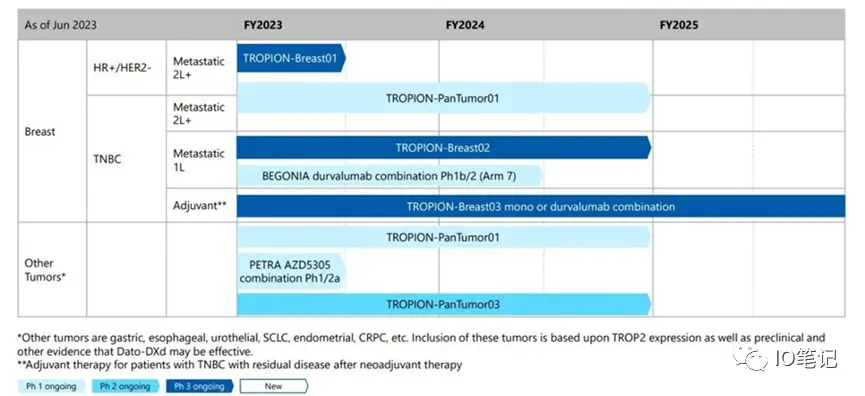
TROPION-Lung Breat02:
三阴性乳腺癌
出处:https://www.daiichisankyo.com.cn/data/upload/file/20220628/6379203009421877722984927.pdf


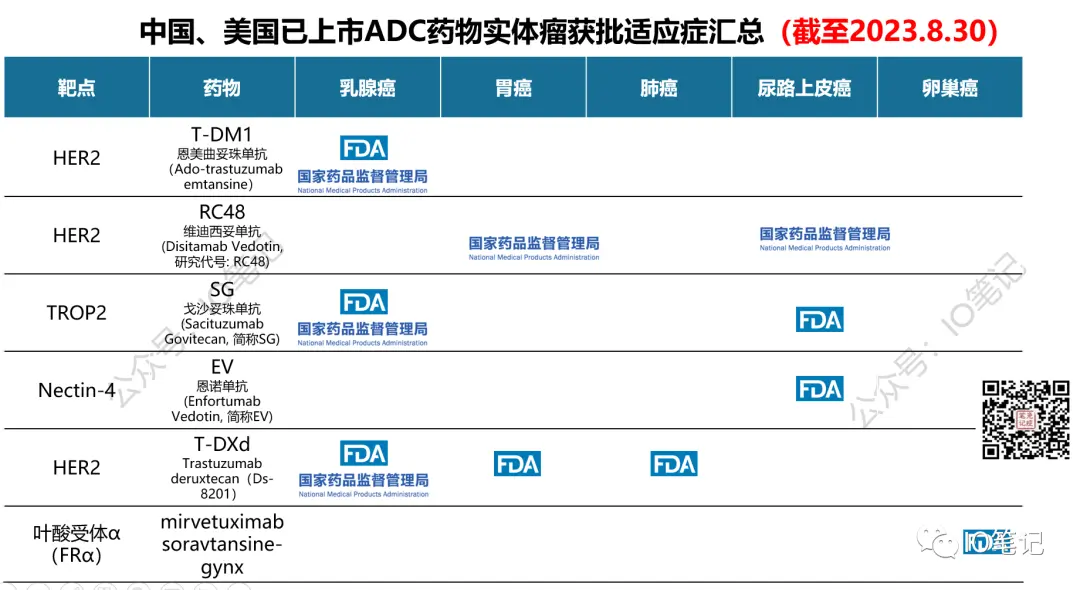
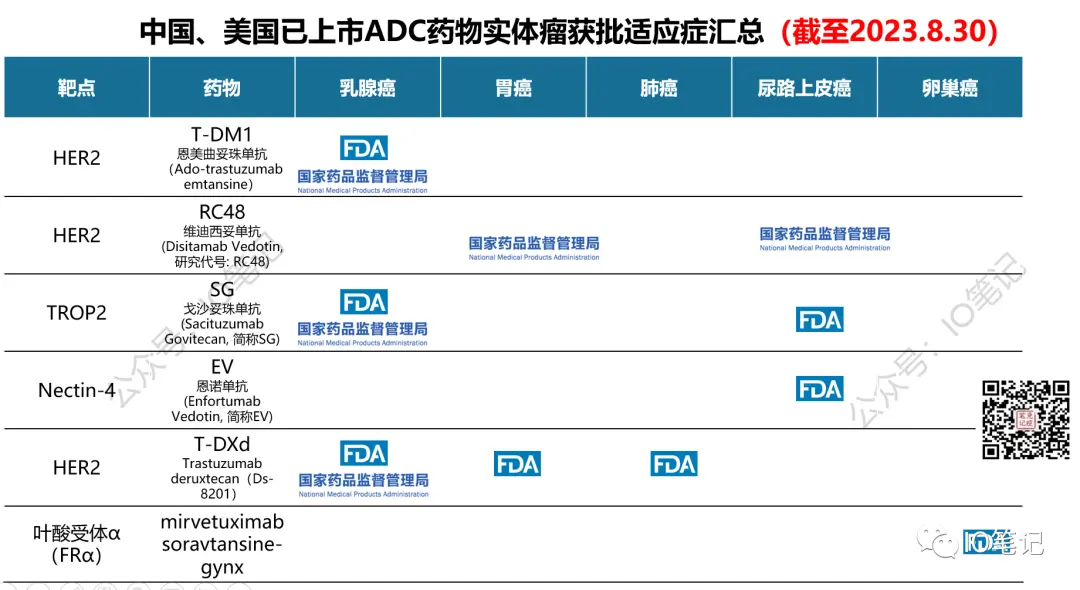
国内已上获批市ADC药物汇总:
截至2023年2月,全球共有15款获批上市的ADC药物。
详见 可点开链接:抗体偶联药物(ADC)合集已更新(合集01)
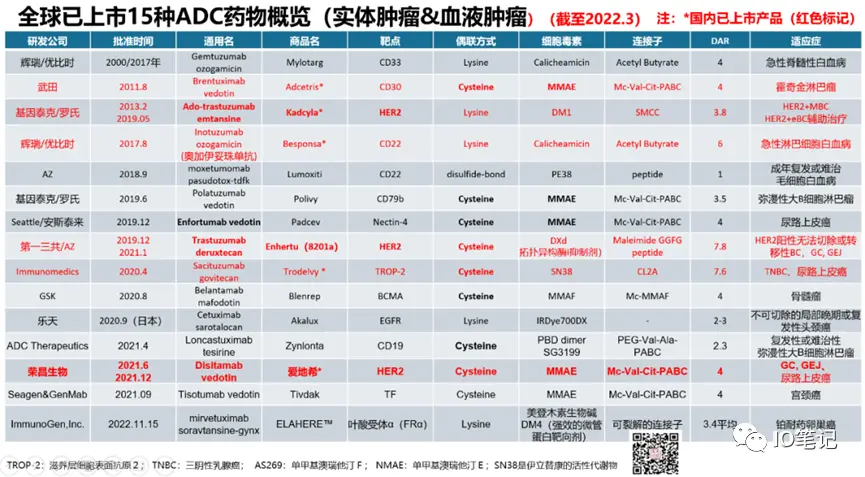
其中,中国获批上市的ADC药物有6个,分别是:
罗氏的恩美曲妥珠单抗(T-DM1)(HER2 ADC)、
Seagen/武田的维布妥昔单抗、
辉瑞的奥加伊妥珠单抗、
荣昌生物的维迪西妥单抗(HER2 ADC);
Immunomedics的戈沙妥珠单抗(TROP2 ADC);
阿斯利康和第一三共联合开发和商业化的优赫得®(英文商品名:Enhertu® 代号DS-8201,通用名:注射用德曲妥珠单抗,HER2 ADC)(2023.2.24国内首获批)。