免疫治疗的“喜”与“忧”:为何癌症患者会耐药?
在抗癌的漫漫征途中,免疫检查点抑制剂(如PD-1/PD-L1抗体)的出现,无疑为无数晚期癌症患者点亮了希望。这些药物通过“解除刹车”,让患者自身的免疫细胞重新识别并攻击肿瘤,使一部分患者实现了长期生存,甚至临床治愈。然而,现实是残酷的:大约只有20%-30%的患者能从这些疗法中显著获益。更令人沮丧的是,许多患者要么一开始就对治疗没有反应(原发性耐药),要么在治疗一段时间后,肿瘤又卷土重来(获得性耐药)。如何攻克免疫治疗耐药这座堡垒,让更多患者有机会拥抱生命的希望,是当前医学界面临的最紧迫挑战。MedFind深知患者的焦虑,致力于为您带来最前沿的抗癌资讯。
肿瘤的“帮凶”:转化生长因子-β1(TGF-β1)的真面目
科学家们一直在不懈地寻找导致免疫治疗耐药的“幕后黑手”。近年来,一个名为“转化生长因子-β1”(简称TGF-β1)的蛋白质逐渐浮出水面,它被形象地称为肿瘤微环境中的“免疫抑制大师”。TGF-β1就像肿瘤细胞的“帮凶”,它能做很多坏事:
- 帮助肿瘤“伪装”:让肿瘤细胞穿上“隐身衣”,逃避免疫系统的侦察和攻击。
- “策反”免疫细胞:它能让原本应该杀死肿瘤的免疫细胞变得疲惫、失去战斗力,甚至反过来帮助肿瘤生长。
- 促进肿瘤生长和转移:它不仅抑制免疫,还能直接促进肿瘤细胞的增殖和扩散,让病情雪上加霜。
因此,TGF-β1被认为是导致免疫疗法失效的关键机制之一。如果能精准地“擒住”这个帮凶,就有望打破免疫耐药的僵局。
创新突破:linavonkibart如何精准“擒住”肿瘤帮凶?
靶向TGF-β1并非易事。过去,许多针对它的药物都因为严重的毒副作用而被迫放弃。这是因为TGF-β家族不只有β1这一个“坏分子”,还有β2和β3这两个对维持心脏、血管等正常生理功能至关重要的“好公民”。过去的药物就像“地毯式轰炸”,不加区分地同时抑制三者,结果在攻击肿瘤的同时,也严重损伤了正常组织,导致无法耐受的毒性,比如不可控制的心血管事件和出血。这成了该领域长期无法逾越的障碍。
然而,一项突破性的I期临床研究带来了转机,一种名为linavonkibart的全新单克隆抗体有望成为破解免疫治疗耐药难题的“钥匙”。
linavonkibart的最大亮点在于其“精准”和“智慧”:
- 首创选择性:它是全球首款全人源、选择性靶向“潜伏态”TGF-β1的抗体。这就像一把“智能锁”,只精准结合并锁住处于“关闭”状态的TGF-β1,阻止其被激活,而对TGF-β2和β3这些“好公民”则“视而不见”。这种高度的选择性,理论上能大幅降低对正常组织的损伤,从而显著减少毒副作用。
- 全人源设计:这种抗体完全由人类自身的抗体结构组成,极大地降低了被人体免疫系统识别为“外来物”而产生抗药抗体的风险,这不仅提升了药物的安全性,也为潜在的长期疗效奠定了基础。
这种“智慧”的设计,让linavonkibart有望在有效抑制肿瘤的同时,最大程度地保护患者的身体健康。
DRAGON I期临床试验:linavonkibart联合帕博利珠单抗的初步战果
这项名为DRAGON的I期临床试验,旨在评估linavonkibart在晚期实体瘤患者中的安全性与有效性。试验分为三个部分:A1(单药剂量递增)、A2(联合帕博利珠单抗剂量递增)和B(联合剂量扩展)。

安全性数据:可控的风险,患者安心的基石
在总计112名患者中,linavonkibart联合帕博利珠单抗的总体安全性良好。其副作用谱与单独使用帕博利珠单抗时基本一致,仅皮肤反应被确定为新增的风险。更令人鼓舞的是,研究中未观察到任何剂量限制性毒性(DLT)或4/5级治疗相关严重不良事件,也未发生细胞因子释放综合征或输液中断。这初步验证了其选择性设计在安全性上的巨大优势,为后续的临床研究和患者用药奠定了安心的基石。
疗效数据:多癌种展现希望,耐药患者的新曙光
在78名对既往抗PD-1治疗耐药的晚期实体瘤患者中,联合治疗显示了令人振奋的抗肿瘤活性:
- 肾透明细胞癌:客观缓解率(ORR)高达20.0%。对于这些已经接受过多线治疗失败的患者来说,20%的缓解率是一个非常具有临床意义的数据,意味着五分之一的患者肿瘤明显缩小。
- 黑色素瘤、头颈鳞癌、尿路上皮癌:客观缓解率分别为18.2%、9.1%和9.1%。虽然数据不如肾癌亮眼,但对于这些同样面临免疫治疗耐药困境的患者群体,也带来了新的治疗选择和希望。
此外,研究还通过探索性生物标志物分析,为肾透明细胞癌患者提供了潜在的疗效预测标志物,这有助于未来更精准地筛选出最可能从该疗法中获益的患者,实现个体化治疗。
Timothy Yap教授表示,这项试验非常令人兴奋,因为医学界长期以来一直试图有效靶向TGF-β1这个蛋白质。linavonkibart的出现,可能是帮助患者克服耐药、进一步从免疫疗法中获益的重要一步。
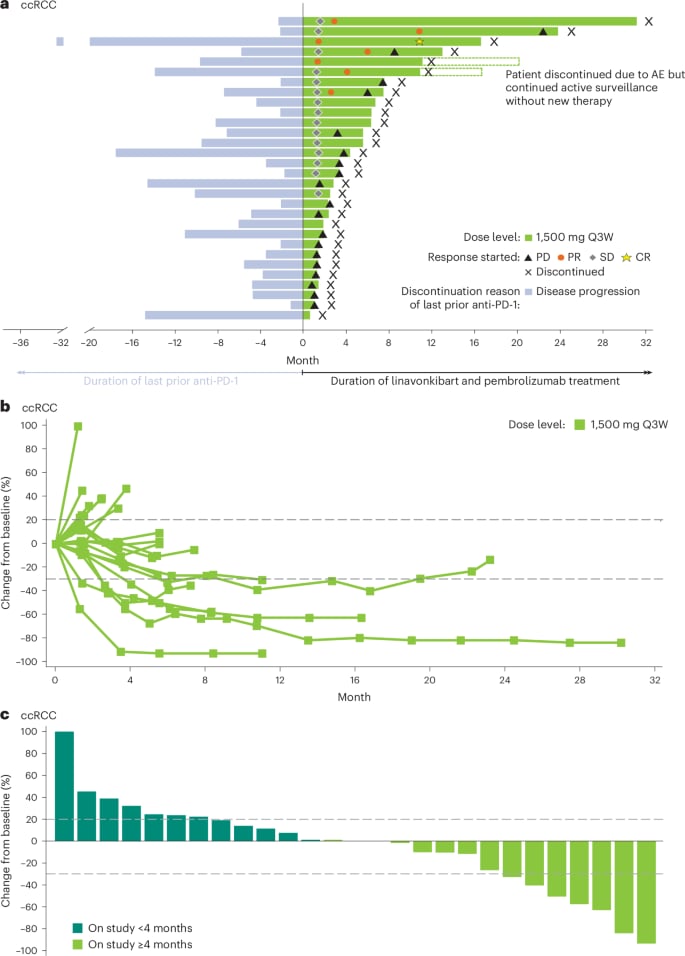
B部分剂量扩展中的临床疗效
这项研究的深远意义与未来展望
尽管I期结果积极,但我们必须清醒认识到,这仍是早期研究。药物的长期安全性、在更大规模人群中的疗效确认,都需要后续II/III期临床试验来验证。从新靶点确认到药物上市,通常需要数年甚至十年时间。但DRAGON试验无疑为这条艰难的道路点亮了一盏明灯,通过精巧的药物设计有可能“驯服”那些曾经令人望而生畏的靶点,从而为攻克肿瘤免疫耐药这座堡垒提供了新的武器和战术思路。
linavonkibart的出现,直击了当前癌症治疗的临床痛点——免疫治疗耐药。它不是放弃TGF-β1这个已验证的靶点,而是通过革命性的选择性抑制策略,巧妙地绕开了之前的毒性陷阱,体现了转化医学的智慧。更重要的是,在强效联合免疫治疗时,它保持了可接受的安全性,这是任何新方案能否走向临床的基石。MedFind将持续关注linavonkibart的后续研究进展,为患者带来最新的抗癌资讯。
MedFind:您的抗癌之路,我们与您同行
面对复杂的癌症治疗,特别是新药的研发和上市,患者和家属常常感到迷茫和无助。linavonkibart虽然前景光明,但距离正式上市仍需时日。然而,对于急需新希望的晚期癌症患者来说,时间就是生命。MedFind致力于为癌症患者提供全球最新的抗癌资讯和药物信息,并协助患者朋友构建海外购药渠道。如果您对linavonkibart或其他前沿抗癌药物有任何疑问,或希望了解更多治疗方案,欢迎随时咨询MedFind。我们专业的团队将为您提供AI辅助问诊服务,并协助您寻找合适的海外购药渠道,让您不再孤单面对疾病的挑战。MedFind,您的抗癌之路,我们与您同行,共同探索生命的无限可能!