胰腺癌治疗的困境与曙光
胰腺癌,素有“癌王”之称,是目前预后最差的恶性肿瘤之一。大多数患者在确诊时,癌细胞已经扩散至身体其他部位,进入转移阶段。对于转移性胰腺癌,五年生存率仅为惊人的2-3%,患者的中位生存期往往以月计算,而非年。数十年来,尽管医学不断进步,但胰腺癌的治疗进展却异常缓慢,这让无数患者和家庭陷入绝望。对于寻求前沿治疗方案的患者,了解最新的抗癌资讯至关重要。
然而,近期来自加州大学洛杉矶分校(UCLA)的一项研究为这一领域带来了全新的希望。研究人员开发出一种名为CAR-NKT细胞疗法的新型免疫疗法,在临床前研究中展现了追踪并摧毁胰腺癌肿瘤的强大能力,即使在肿瘤已经发生远端转移的情况下依然有效。这项发表于《美国国家科学院院刊》(PNAS)的研究,可能将彻底改变我们对抗这种顽固疾病的方式。

攻克坚固堡垒:CAR-NKT疗法如何多管齐下?
传统的CAR-T细胞疗法在治疗某些血液肿瘤方面取得了革命性成功,但在对抗如胰腺癌这样的实体瘤时却屡屡受挫。这主要是因为胰腺癌肿瘤会构建一个由致密结缔组织和抑制性免疫细胞组成的“保护屏障”,阻止治疗性细胞的渗透。更棘手的是,这些肿瘤细胞如同伪装大师,会不断改变其表面的分子标记(即抗原),以逃避免疫系统的识别和攻击。
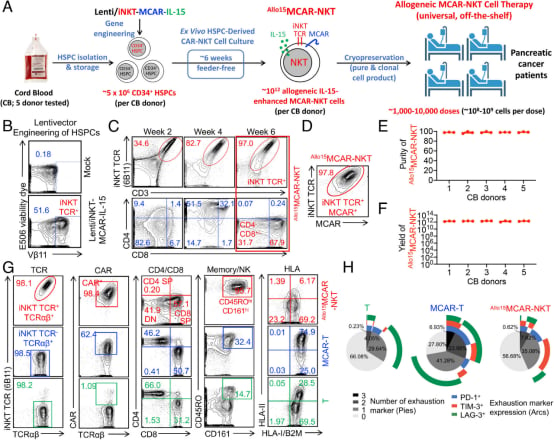
为了攻克这些障碍,UCLA的研究团队将目光投向了一种罕见但功能强大的免疫细胞——恒定自然杀伤T细胞(NKT细胞)。他们通过基因工程技术,为这些NKT细胞装上了能够识别间皮素(mesothelin)的嵌合抗原受体(CAR)。间皮素是一种在多种癌细胞(包括胰腺癌)表面高表达的蛋白质。
经过改造的CAR-NKT细胞获得了通过多种独立机制同时攻击肿瘤的能力。该研究的第一作者Yanruide Li博士形象地描述道:“我们基本上是在包围肿瘤,不给它任何逃脱路线。即使癌细胞试图通过改变其分子特征来逃避某一条攻击途径,我们的疗法也在同时从其他多个角度打击它。肿瘤根本来不及适应。”
精准导航:全面追踪并清除转移肿瘤
转移是导致胰腺癌高死亡率的主要原因,尤其是扩散到肝脏和肺部的肿瘤,极难被免疫细胞触及和浸润。传统的CAR-T细胞常常被阻挡在肿瘤外围,无法穿透这层致密的组织屏障。
为了验证新疗法的真实效力,研究团队采用了专门模拟人类胰腺癌恶劣微环境的先进临床前模型进行测试,这比标准测试方法的门槛要高得多。
结果令人振奋。在这些严格的测试中,CAR-NKT细胞展现了卓越的肿瘤归巢能力。Li博士解释说:“这些细胞高表达趋化因子受体,就像一个分子GPS系统,能引导它们直接到达肿瘤部位。无论肿瘤在肺部还是胰腺,它们都能主动寻找并浸润癌细胞,无论它藏在哪里。”
在不同的小鼠胰腺癌模型中,该疗法均一致性地减缓了肿瘤生长并显著延长了生存期。更重要的是,即使在充满炎症的恶劣肿瘤微环境中,这些CAR-NKT细胞也保持了其杀伤效力,并且几乎没有表现出“耗竭”的迹象——这是导致其他细胞疗法随时间推移而失效的常见问题。
“现货供应”的革命:降低治疗成本与等待时间
除了强大的抗癌能力,该平台还解决了当前细胞疗法面临的三大核心障碍:时间、生产复杂性和高昂的成本。
目前的个性化CAR-T疗法需要从每位患者体内采集免疫细胞,送至专门的设施进行基因改造,再回输到患者体内,整个过程耗时数周。对于病情危重的胰腺癌患者而言,数周的等待可能是致命的。此外,其高达数十万美元的费用也让许多家庭望而却步。而对于许多患者家庭而言,现有疗法的高昂费用是一大障碍。MedFind致力于提供高性价比的靶向药和免疫药直邮服务,帮助患者减轻经济负担。
UCLA团队的方法则完全不同。由于NKT细胞具有独特的免疫特性,天然不会引起宿主抗移植物病(GvHD)等危险的排斥反应,因此可以利用健康的捐赠者提供的造血干细胞进行大规模生产,制成“现货供应”的通用型细胞产品。这意味着一位捐赠者的细胞可能足以用于数千次治疗,每剂成本预计约为5000美元,大大降低了治疗门槛。
广阔前景:一种疗法,多种癌症治疗可能
该疗法的潜力不止于胰腺癌。由于其靶向的间皮素在乳腺癌(特别是三阴性乳腺癌)、卵巢癌和肺癌等多种实体瘤中也高度表达,因此同一种CAR-NKT细胞产品有望用于治疗多种不同类型的癌症。研究团队在独立的临床前研究中,已经证实了该疗法对三阴性乳腺癌和卵巢癌的有效性。
随着所有临床前研究的顺利完成,该团队正积极准备向美国食品药品监督管理局(FDA)提交申请,以启动人体临床试验。在等待新疗法上市期间,患者可以利用MedFind AI问诊等工具,获取个性化的治疗建议和前沿信息。
正如该研究的资深作者Lili Yang博士所说:“胰腺癌患者现在就需要更好的治疗选择。我们已经开发出一种强效、安全、可扩展且负担得起的疗法。下一个关键步骤是证明它能在患者身上产生与我们在临床前工作中看到的相同结果。”这项研究无疑为深陷困境的胰腺癌患者点燃了新的希望之火。





