很多胃癌患者和家属最担心的,不只是“肿瘤在不在”,而是“会不会转移”“为什么明明治疗了,病情还是往前走”。在胃癌的发生发展中,真正“推波助澜”的,往往不只有癌细胞本身,还包括它周围的肿瘤微环境。最新研究提示,胃癌细胞与癌症相关成纤维细胞之间,可能存在一条推动转移的关键通路。读懂这条通路,有助于我们理解胃癌转移机制、判断未来潜在靶点,也能帮助患者更理性地看待“前沿研究离临床还有多远”。
胃癌转移,为什么这么难缠
胃癌是全球常见恶性肿瘤之一,也是癌症相关死亡的重要原因。对很多患者来说,真正影响长期生存的关键问题,常常不是原发灶,而是转移。一旦进入转移性胃癌阶段,整体治疗难度会明显增加,患者中位总生存期大约只有1年左右。
为什么胃癌转移这么复杂?可以把肿瘤想象成一颗不断“改造周边环境”的种子。它不只是自己长大,还会“教育”周围的细胞,让这些原本正常的细胞帮助它生长、逃逸和扩散。其中,最值得警惕的一类“帮手”,就是癌症相关成纤维细胞,也就是常说的CAF。
CAF是什么?为什么它会帮着肿瘤转移
成纤维细胞本来是人体结缔组织中的“维修工”,负责组织修复和支撑。但在肿瘤微环境中,其中一部分会被“策反”,变成促进肿瘤进展的CAF。它们会分泌多种信号分子,重塑肿瘤周围的“土壤”,让癌细胞更容易生长、侵袭,甚至耐药。
过去研究已经发现,CAF可以通过分泌白细胞介素-6、肝细胞生长因子、白细胞介素-33等方式促进胃癌进展;某些特定亚型的CAF还会造成基质硬化,使胃癌对5-氟尿嘧啶出现获得性耐药。也就是说,CAF不是“围观群众”,而是胃癌转移和治疗失败的重要参与者。
这项研究进一步追问:CAF到底是通过什么更深层的机制,重新编程胃癌细胞,让它更容易转移的?
这项研究发现了什么核心机制
研究者通过分析胃癌细胞与CAF通讯后的转录组变化,找到了一个关键分子:GAL3ST1。结果提示,CAF会诱导胃癌细胞上调GAL3ST1,而GAL3ST1进一步促进胃癌细胞获得更强的转移潜能。
更重要的是,这不仅仅是“一个基因变多了”这么简单。研究发现,GAL3ST1可能是一种新的组蛋白磺基转移酶,它能在细胞质中对新生组蛋白H3的第99位酪氨酸进行磺基化修饰,也就是所谓的H3Y99sulf。
如果这些词看起来很陌生,可以这样理解:组蛋白就像缠绕DNA的“线轴”,决定哪些基因容易被打开、哪些基因被关上。给组蛋白加上不同的化学标记,就像给基因开关贴上不同颜色的标签。GAL3ST1做的事,就是给其中一个关键位置贴上了一个新的“标记”,而这个标记会进一步引发连锁反应,最终把促进转移的程序打开。

胃癌转移相关肿瘤微环境与表观遗传调控研究图示
从CAF信号到胃癌转移,整条通路怎么走
这项研究梳理出了一条相对完整的通路:
- CAF分泌SEMA7A;
- SEMA7A与胃癌细胞表面的ITGB1结合;
- 随后激活ERK1/2-CEBPB信号通路;
- 推动胃癌细胞转录上调GAL3ST1;
- GAL3ST1在细胞质中催化新生组蛋白H3发生H3Y99sulf修饰;
- 这些被修饰的组蛋白在AP2B1参与下进入细胞核;
- 进入细胞核后募集KAT2A,建立H3K56ac修饰;
- 最终激活β-连环蛋白转录,驱动上皮-间质转化,也就是EMT;
- EMT增强后,胃癌细胞更容易脱离原发灶、迁移并形成转移。
如果把这个过程比作一场“接力赛”,CAF是发令员,SEMA7A是第一棒,GAL3ST1是关键中继,最后冲线的是EMT和转移。任何一环异常活跃,都可能让胃癌细胞更“会跑”。
什么是EMT?为什么它和转移关系这么大
EMT是“上皮-间质转化”的简称。正常上皮细胞原本排列整齐、彼此粘得很紧,像一块块砌好的瓷砖;而一旦发生EMT,细胞会变得更松散、更灵活、更擅长移动,像从“固定砖块”变成“会游走的个体”。
对癌细胞来说,EMT意味着更强的侵袭能力、更高的远处播散风险,也常常与耐药、复发等问题相关。因此,任何能明显推动EMT的通路,都值得高度关注。
为什么说这是“表观遗传”层面的新发现
很多患者一听“基因”,容易以为一定是DNA发生了突变。其实,肿瘤进展不只靠突变,也靠“怎么用这些基因”。表观遗传调控,讲的是不改变DNA字母顺序,却改变基因表达方式。
这项研究的重要意义在于,它把胃癌转移与一种相对新的组蛋白修饰——H3Y99位点磺基化,联系在了一起。研究者认为,GAL3ST1并非只是普通代谢相关酶,还可能直接参与调控组蛋白修饰,进而改变肿瘤细胞的转录程序。这为理解胃癌“为什么越来越会转移”提供了一个新的解释框架。
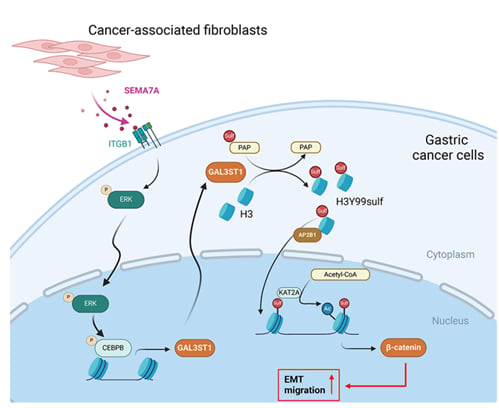
SEMA7A/GAL3ST1/H3Y99sulf轴促进胃癌转移的模式机制图
这项研究对患者意味着什么
首先,这是一项机制研究,核心价值在于“解释为什么”,而不是立刻改变现有标准治疗。它目前带来的最大意义,主要有三点:
- 帮助理解转移本质:胃癌转移并不是癌细胞单打独斗,微环境尤其是CAF的作用非常关键。
- 提示未来治疗新靶点:SEMA7A、ITGB1、GAL3ST1、AP2B1、KAT2A等节点,未来都可能成为药物开发方向。
- 为精准治疗提供思路:如果未来能识别出某些患者存在这条通路的异常激活,可能帮助筛选更适合的治疗策略。
但也要客观看待:发现新机制,不等于马上有新药可用。从实验室发现到真正变成临床可及的治疗方案,通常还需要更多动物实验、药物研发和临床试验验证。
现在临床上,胃癌转移治疗看什么
虽然这条新通路仍处于研究阶段,但对患者来说,更现实的问题是:现阶段转移性胃癌到底怎么治?临床上一般会综合考虑病理类型、分期、体能状态、生物标志物以及既往治疗情况,制定个体化方案。
常见评估重点
- HER2状态
- PD-L1表达
- MSI/MMR状态
- CLDN18.2表达
- 肿瘤负荷和转移部位
- 患者营养状况和体力评分
常见治疗方向
- 以化疗为基础的系统治疗;
- 符合条件者联合靶向治疗或免疫治疗;
- 部分患者可考虑后线新药或临床试验;
- 出现梗阻、出血、疼痛等问题时,需同步进行支持治疗和症状管理。
也就是说,前沿机制研究告诉我们“未来可能从哪里突破”,而规范化诊疗和生物标志物检测决定了“今天该怎么治”。两者并不矛盾,反而应该结合起来看。
患者最关心的几个现实问题
1. 这个发现能直接用于检测吗
目前更偏向科研层面的机制发现,尚不是常规临床检测项目。是否未来会发展成预后标志物、转移风险标志物,还需要更多研究确认。
2. 现在有专门针对GAL3ST1的成熟药物吗
根据目前公开信息,这项研究主要提供了潜在靶点和理论依据,并不意味着已有成熟标准药物可直接用于胃癌患者。患者不要轻信“新机制=立刻有特效药”的宣传。
3. 如果已经转移了,还有必要了解这些研究吗
有必要。因为前沿研究往往决定未来临床试验和新药方向。对于标准治疗选择有限、希望寻找下一步方案的患者来说,尽早理解关键通路和新靶点,有助于更高效地筛选试验机会或国际前沿药物信息。
治疗之外,转移性胃癌患者还能做什么
前沿研究很重要,但日常管理同样会直接影响治疗耐受性和生活质量。尤其是胃癌患者,常合并食欲差、体重下降、贫血、恶心、腹胀等问题,居家管理不能忽视。
营养管理
- 少量多餐,优先保证蛋白质和总热量摄入;
- 可选择鸡蛋、鱼肉、豆制品、酸奶等相对易消化食物;
- 进食后易腹胀者,避免一次吃太多、太快;
- 若出现明显吞咽困难、持续呕吐或体重快速下降,应尽快就医评估营养支持。
症状观察
- 警惕黑便、呕血、持续腹痛、进行性乏力;
- 若出现明显黄疸、持续发热、呼吸困难、骨痛加重,要及时复诊;
- 治疗期间保存好检查结果和用药记录,便于医生动态判断疗效和耐药风险。
心理调节
“转移”两个字会带来很大心理冲击,但它不等于没有办法。很多患者通过规范治疗、靶向或免疫治疗、营养支持以及症状管理,可以获得更长的疾病控制时间和更好的生活质量。家属要做的,不只是催着治疗,更是帮助患者把信息理清、把节奏稳住。
一张表看懂本研究的临床意义
| 问题 | 研究给出的答案 | 对患者的意义 |
|---|---|---|
| 谁在推动胃癌转移 | 不只是癌细胞,CAF也在积极参与 | 关注肿瘤微环境,理解转移更全面 |
| 关键分子是什么 | SEMA7A、ITGB1、GAL3ST1、H3Y99sulf等 | 提示未来潜在药物靶点 |
| 核心机制是什么 | CAF通过表观遗传重编程促进EMT和转移 | 为新疗法研发提供方向 |
| 现在能否替代标准治疗 | 不能 | 仍应以规范检测和标准治疗为基础 |
| 是否值得持续关注 | 值得 | 可能影响未来临床试验和新药布局 |
如何把“前沿研究”真正变成治疗机会
对患者和家属来说,最难的往往不是看不懂论文,而是不知道这些研究和自己有没有关系。真正有效的做法是把问题拆开:
- 先明确病理分型、分期和关键生物标志物;
- 再判断目前标准治疗是否已经用足;
- 如果疗效不佳或选择有限,再进一步寻找匹配的临床试验、前沿药物或跨境可及方案;
- 整个过程中,最好有专业团队帮助解读报告、梳理治疗路径和药物信息。
这也是很多家庭在抗癌路上最需要的支持:不是碎片化信息,而是可信、可执行、贴近临床现实的方案判断。
写在最后
这项研究让我们看到,胃癌转移背后并非单一事件,而是一整套由肿瘤微环境、表观遗传重编程和细胞命运改变共同推动的过程。CAF分泌的SEMA7A,经由ITGB1、ERK1/2、CEBPB上调GAL3ST1,再通过H3Y99sulf和后续转录激活推动EMT,这条新轴线为转移性胃癌提供了新的解释,也带来了新的希望。
如果您或家人正在面对胃癌,尤其是复发、转移、治疗选择有限,或对新药、新靶点、海外前沿方案有疑问,不妨尽早系统梳理病情。MedFind可以帮助患者和家属更高效地获取全球抗癌资讯、解读检测报告与治疗路径,并在合规前提下了解前沿药物可及性、辅助问诊及跨境直邮相关信息。很多时候,真正改变后续治疗节奏的第一步,就是把复杂信息看懂,把下一步方向找准。
参考文献:Cancer Research. 2026 Feb 13. GAL3ST1-Mediated Histone Tyrosine Sulfation Induced by Cancer-Associated Fibroblasts Promotes Gastric Cancer Metastasis. DOI: 10.1158/0008-5472.CAN-25-2452.