对于许多身处抗癌一线的患者及家属而言,“免疫逃逸”和“治疗耐药”是两个令人心碎的词汇。当我们寄予厚望的放化疗甚至免疫检查点抑制剂(如PD-1/PD-L1)在某些“冷肿瘤”面前束手无策时,医学界正不断探索更精准、更强效的打击手段。近日,来自中国医学科学院、天津中医药大学等机构的科研团队在国际权威学术期刊《ACS Nano》上发表了一项令人振奋的研究:他们利用天然产物姜黄素(Curcumin)改造出一种新型光敏剂Cur-T。这种药物就像一颗能够精准定位并爆破癌细胞“垃圾处理厂”的炸弹,通过激活铁死亡和焦亡等多种机制,彻底点燃抗肿瘤免疫反应。
什么是光动力疗法(PDT)?为什么需要“升级版”?
光动力疗法(PDT)简单来说就是“光+药+氧”的组合。患者使用光敏药物后,医生用特定波长的光照射肿瘤部位,药物在光的作用下产生大量的活性氧(ROS)。这些活性氧就像手术刀一样,能从内部切断肿瘤的生命线。然而,传统的PDT存在两个软肋:一是肿瘤内部往往缺氧,限制了杀伤力;二是癌细胞非常“狡猾”,它们会启动“自噬”机制,即通过自我修复来清理受损部分,从而死里逃生。为了破解这一难题,科研团队研发了Cur-T。
深度解析:Cur-T如何实现对肿瘤的“降维打击”?
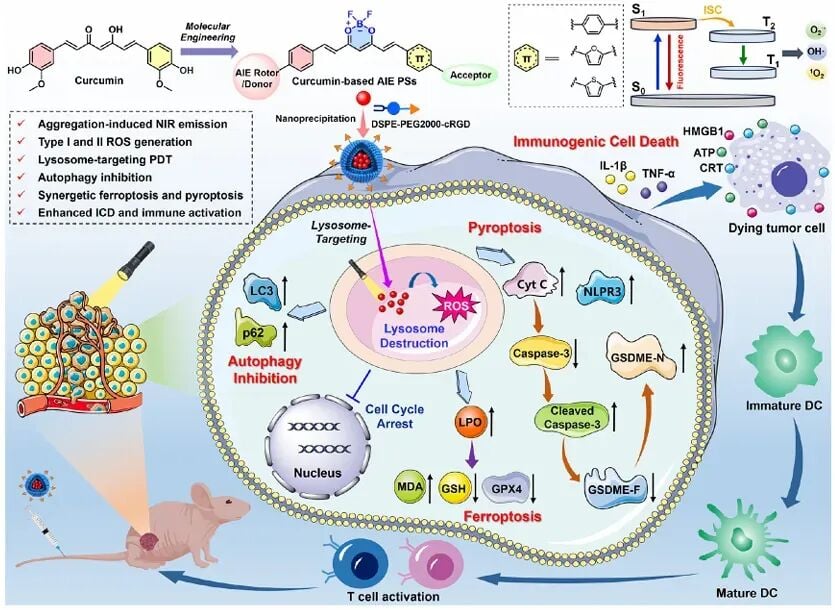
Cur-T的设计精妙之处在于它不仅保留了姜黄素的天然活性,还具备了“定点爆破”溶酶体的能力。溶酶体被形象地称为细胞的“垃圾回收站”或“自杀仓库”,里面充满了各种分解酶。
1. 摧毁“避难所”:抑制自噬流
研究发现,Cur-T能特异性地聚集在癌细胞的溶酶体中。在光照下,它产生的活性氧会直接刺破溶酶体膜。当“垃圾回收站”破裂,癌细胞不仅无法通过自噬作用进行自我修复,还会因为内部强酸性物质外泄而导致系统崩溃。
2. 激发“死亡之舞”:铁死亡与焦亡
与传统的细胞“凋亡”(一种相对温和、不引起免疫反应的自杀)不同,Cur-T诱导的是极其剧烈的铁死亡和焦亡。这两种死亡方式会向免疫系统释放强烈的“求救信号”,将原本死气沉沉的“冷肿瘤”转变为免疫系统能够识别并攻击的“热肿瘤”。

临床数据解读:抗癌效能的跨越式提升
为了验证Cur-T的实战能力,研究团队进行了多项实验对比,结果显示其在多个维度上优于传统方案。如需评估此类前沿方案是否适合您的具体病情,可使用 MedFind 的 AI 辅助问诊深度解读您的病历或直接与在线客服联络。
| 对比维度 | 普通姜黄素/传统光敏剂 | 新型光敏剂 Cur-T |
|---|---|---|
| 杀伤效力(IC50值) | 相对较高(药效弱) | 降低至0.15-0.33 μM(药效提升15.5倍) |
| 靶向精准度 | 全身分布,特异性差 | 精准靶向溶酶体 |
| 死亡诱导模式 | 主要为细胞凋亡 | 铁死亡 + 焦亡 + 抑制自噬 |
| 免疫激活能力 | 较弱,难以抑制远端转移 | 极强,可激活全身抗肿瘤免疫 |
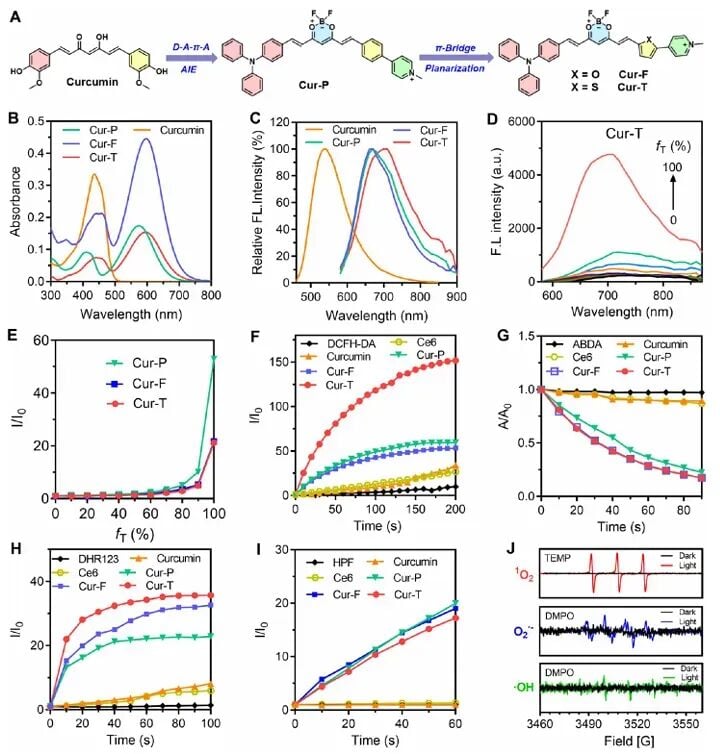
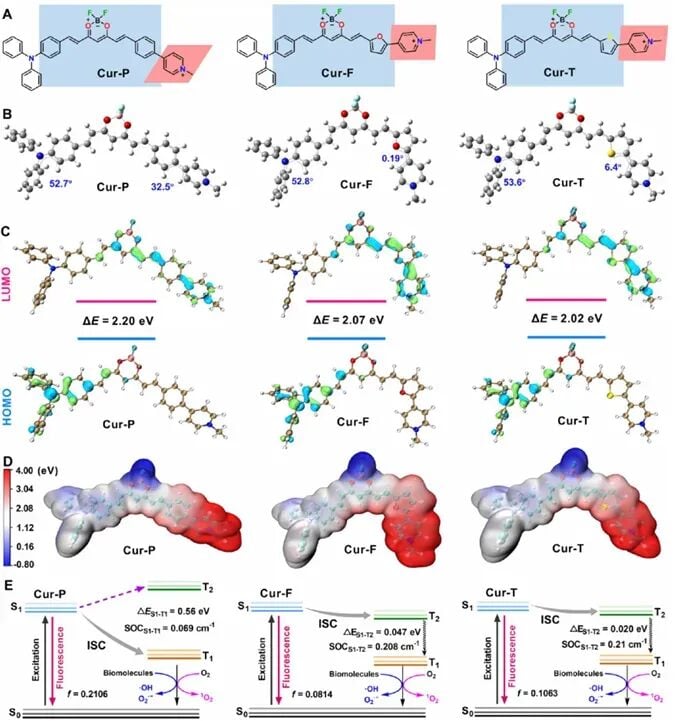
在动物实验中,研究者观察到,使用了Cur-T纳米粒(Cur-T NPs)并配合光照的小鼠,其原发肿瘤受到了显著抑制。更令人惊喜的是,即使是没有受到光照的对侧肿瘤(模拟临床上的远处转移灶),也因为全身免疫系统的激活而明显缩小。这说明该疗法具备了“打一处,管全身”的潜力。
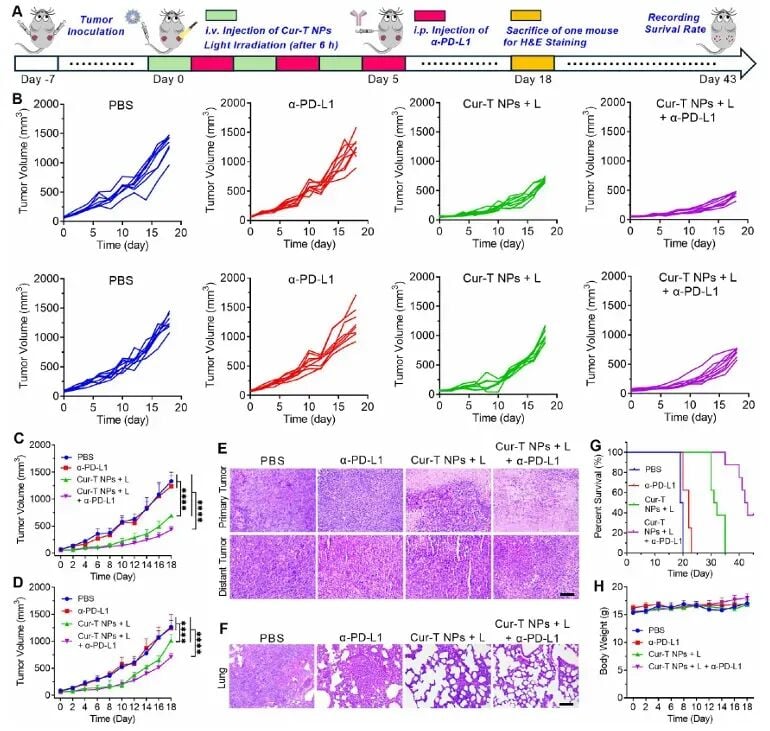
联合方案:与PD-L1抑制剂的“强强联手”
研究进一步证实,当Cur-T光动力疗法联合PD-L1抑制剂(α-PD-L1)时,抗癌效果达到了巅峰。在这种联合策略下,小鼠的生存期延长至43天,肺部转移病灶几乎消失。这一发现为那些对传统免疫药物反应不佳的患者提供了全新的思路:先用Cur-T光动力疗法“点燃”免疫火种,再用PD-L1抑制剂“火上浇油”,实现彻底清除肿瘤的目标。
居家管理与注意事项:光动力治疗后的“避光期”
虽然Cur-T目前仍处于科研和临床转化前阶段,但借鉴现有的光动力治疗经验,患者若接受此类治疗,需注意以下居家护理要点:
- 严格避光:治疗后一定时间内(通常为2-4周),皮肤和眼睛对光线高度敏感。应避免阳光直射,室内可使用厚窗帘,外出须佩戴墨镜、遮阳帽,穿着长袖长裤。
- 皮肤观察:注意照射部位是否有红肿、水疱。轻微红肿属正常反应,若出现剧烈疼痛或大面积破溃,应及时联系医生。
- 营养支持:铁死亡的诱导与体内微环境相关,建议在专业营养师指导下,均衡摄入抗氧化食物,保持身体机能。
结语:从实验室走向临床的“救命指南”
这项基于姜黄素的创新研究,不仅展示了中国科学家在生物医学前沿的探索能力,也为广大癌症患者带来了实实在在的希望。目前,该药物正处于向临床转化的关键阶段。MedFind 将持续关注其最新进展。对于急需获取全球已获批最前沿药物(如最新的PD-1/PD-L1药物及光敏剂辅助治疗药物)的患者,MedFind 提供专业的“全球抗癌药品跨境直邮服务”,确保药品来源正规、温控严苛、直达您手中。抗癌路上,您并不孤单,MedFind 与您一同寻找每一线生机。
参考信息:
“A Curcumin-Based Lysosome-Targeting Photosensitizer for Enhanced Photo-Immunotherapy”, ACS Nano, 2024. DOI: 10.1021/acsnano.5c18874





