胶质母细胞瘤(Glioblastoma, GBM)被医学界公认为“癌中之王”,是中枢神经系统最常见、也最具侵袭性的原发性恶性肿瘤。尽管现代医学在手术切除、精准放疗和系统化疗方面取得了显著进展,但GBM患者的中位生存期仍难以突破15个月,五年生存率极低。面对这种高度复杂且极易复发的疾病,科学家们一直在寻找能够攻克其“免疫防御阵地”的新武器。近日,来自厦门大学夏宁邵院士、黄承浩教授团队在国际顶级期刊《Nature Communications》上发表了一项重磅研究,揭示了帕金森病药物LRRK2抑制剂(LRRK2 inhibitors)能与溶瘤病毒产生强大的协同效应,为胶质母细胞瘤的治疗开辟了一条极具潜力的“老药新用”新路径。
胶质母细胞瘤治疗的重重困境:为何传统疗法屡屡受挫?
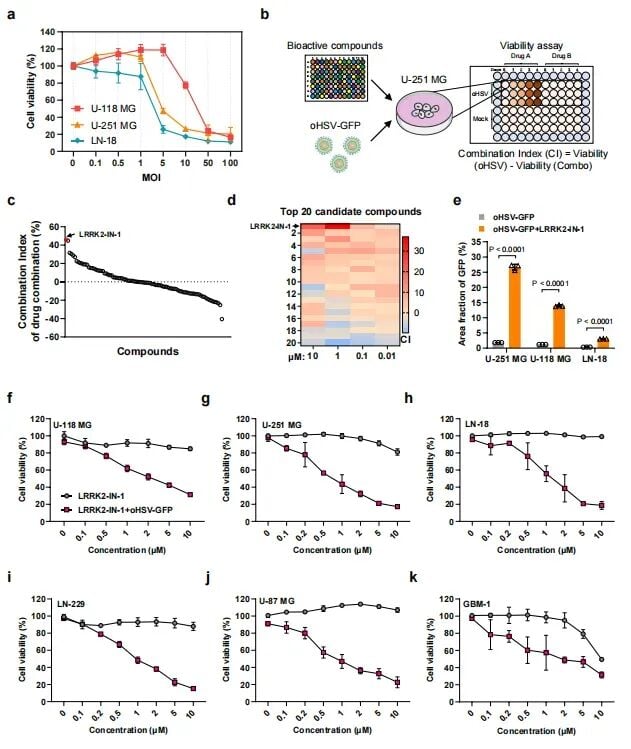
胶质母细胞瘤之所以难治,主要源于其三大特性:高度侵袭性、极强的异质性以及血脑屏障的阻隔。肿瘤细胞像树根一样深入正常的脑组织,导致手术很难完全切除。同时,肿瘤内部的细胞种类繁多,针对单一靶点的药物往往很快就会产生耐药性。近年来,溶瘤单纯疱疹病毒(Oncolytic Herpes Simplex Virus, oHSV)作为一种新型免疫疗法引起了广泛关注。这种病毒经过基因改造,能够特异性地识别、感染并裂解肿瘤细胞,同时释放出肿瘤相关抗原,激活患者自身的抗肿瘤免疫反应。然而,临床研究发现,单纯使用oHSV的效果并不理想,许多GBM细胞具有先天的抗病毒机制,就像给肿瘤穿上了一层“防弹衣”,让溶瘤病毒难以进入或大规模复制。
跨界联手:帕金森病靶点LRRK2成为攻克脑瘤的关键
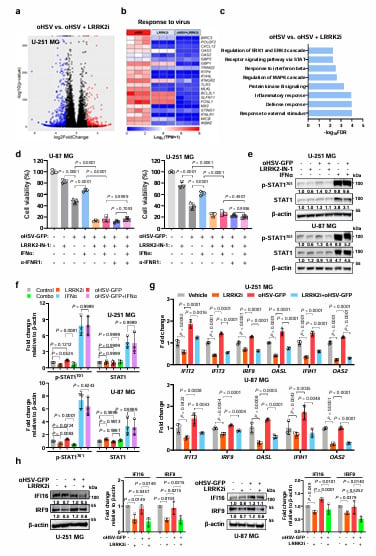
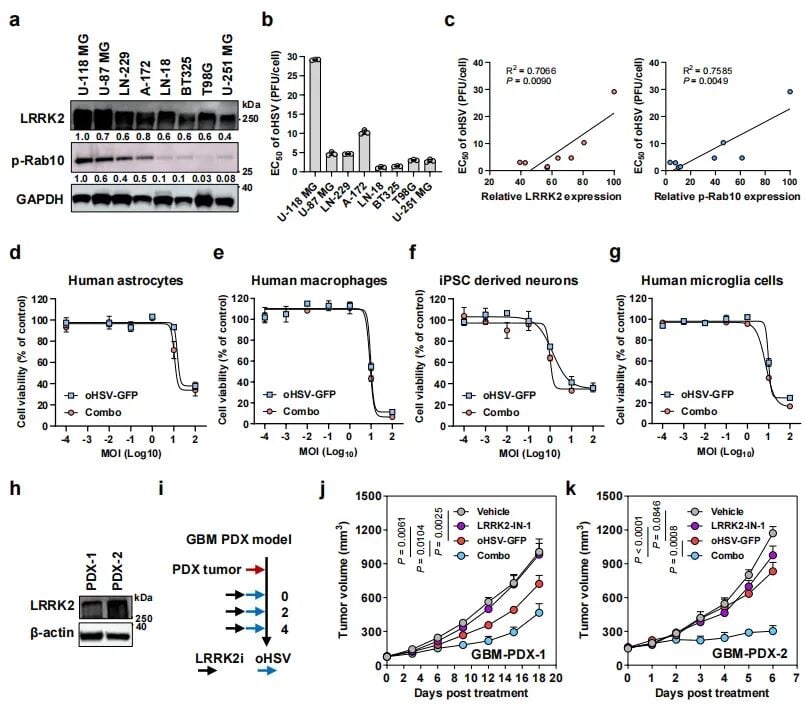
为了打破肿瘤的抗病毒防御,夏宁邵院士团队对1593种具有生物活性的化合物进行了大规模筛选。令人惊喜的是,他们发现针对富亮氨酸重复激酶2(LRRK2)的抑制剂展现出了最强的增敏效果。LRRK2原本是帕金森病(PD)领域的热门靶点,多种针对该靶点的小分子抑制剂已经进入临床试验阶段。研究发现,LRRK2在胶质母细胞瘤细胞中竟然呈现高表达状态,它就像是一个“保安队长”,专门负责开启肿瘤细胞的抗病毒防御系统。通过使用LRRK2-IN-1(LRRK2 inhibitor 1)或MLi-2(LRRK2 inhibitor)等抑制剂,科学家们成功撤下了这道防线,使oHSV在肿瘤内的复制效率提升了数倍。

深度解析:LRRK2-STAT1信号轴如何操纵肿瘤耐药?
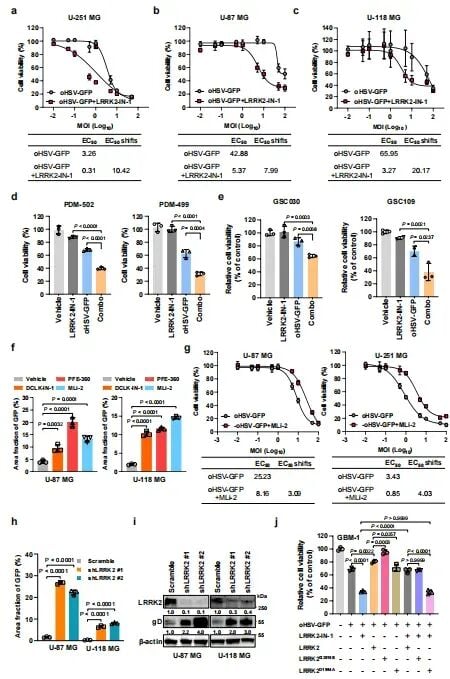
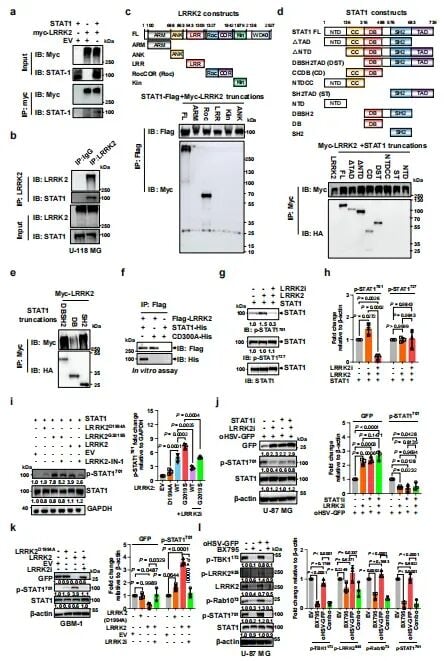
研究团队通过分子生物学手段深入探索了背后的机制。他们发现,LRRK2能与STAT1蛋白直接结合,并促进STAT1在酪氨酸701位点发生磷酸化。这一过程会激活一系列干扰素刺激基因(ISGs)的表达。简单来说,LRRK2通过激活STAT1,在肿瘤细胞内建立了一个强大的“抗病毒防御网”。当溶瘤病毒进攻时,这套防御系统会迅速产生干扰素,阻止病毒的复制和扩散。而当研究人员使用LRRK2抑制剂阻断这一通路后,STAT1的磷酸化程度显著下降,肿瘤细胞的抗病毒武装被“卸除”,oHSV得以大显身手,诱导肿瘤细胞发生大规模凋亡。
多维度验证:从细胞系到患者来源的干细胞
为了确保结论的可重复性和临床意义,研究者在多种模型中进行了验证。不仅在常规的GBM细胞系中,甚至在患者来源的原代脑瘤细胞(PDM)以及最具抗药性的胶质母细胞瘤干细胞(GSCs)中,LRRK2抑制剂均表现出了显著的降阈作用。这意味着,即使是对传统治疗高度不敏感的脑瘤干细胞,在这种联合疗法面前也变得“脆弱”起来。
不仅是进入:促进病毒在肿瘤组织间的“星火燎原”
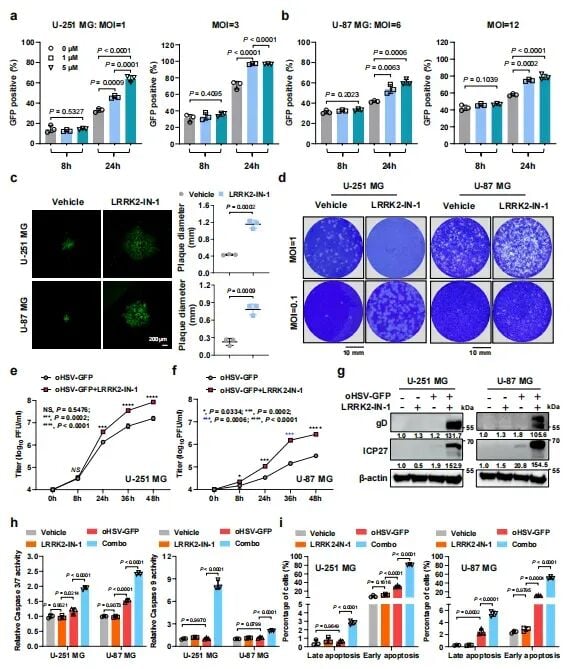
实验数据进一步揭示,LRRK2抑制剂并不影响病毒最初进入细胞的过程,但它能显著促进病毒在感染后的晚期扩散。在显微镜下可以观察到,加入抑制剂后,病毒形成的噬斑直径明显增大,病毒滴度大幅上升。这种“星火燎原”之势,确保了溶瘤病毒能深入肿瘤腹地,实现更彻底的杀伤。
惊人的动物实验数据:75%的小鼠达到完全缓解
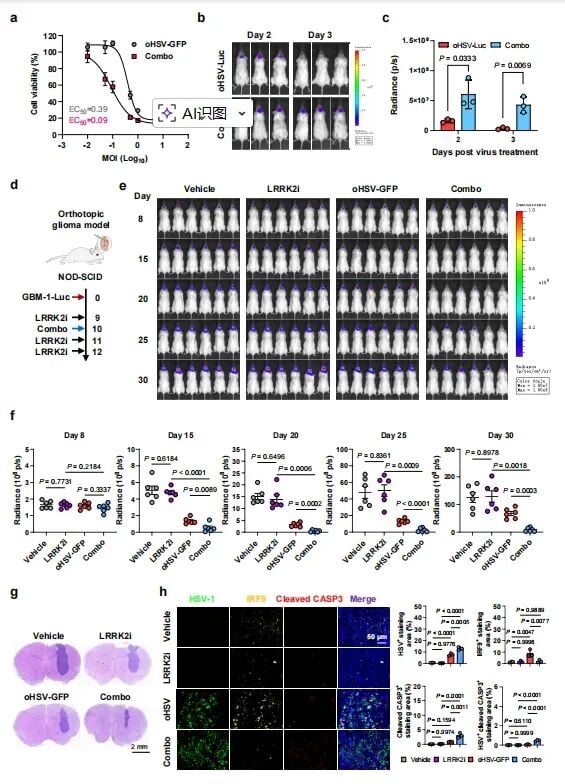
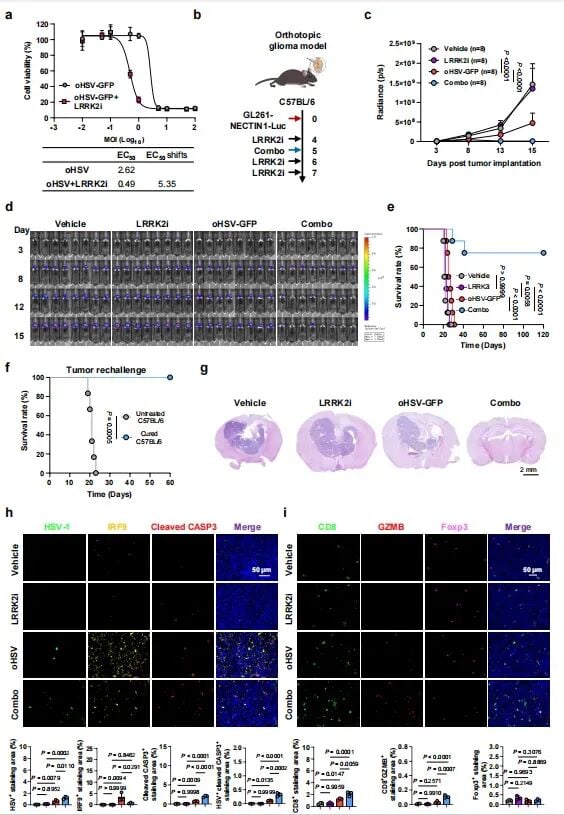
在更为复杂的原位脑瘤小鼠模型中,联合疗法的表现令人振奋。研究人员利用患者来源的异种移植(PDX)模型发现,联合使用oHSV和LRRK2抑制剂的小鼠,其肿瘤生长受到了剧烈抑制,生存期显著延长。而在免疫功能健全的模型中,效果更为惊人:约75%的小鼠达到了“完全缓解”(肿瘤消失),并且这些小鼠产生了长期的抗肿瘤免疫记忆。当研究人员再次尝试在这些小鼠体内接种肿瘤细胞时,小鼠体内的CD8⁺ T细胞(即免疫系统中的“杀手细胞”)迅速反应,阻止了肿瘤的再次生长。这说明联合疗法不仅杀伤了现有肿瘤,还给免疫系统“打了疫苗”。
老药新用的安全性优势:精准打击肿瘤,保护正常神经
脑瘤治疗最担心的就是副作用。幸运的是,研究发现LRRK2抑制剂与溶瘤病毒的联合治疗展现出了极佳的选择性。该策略对正常的星形胶质细胞、巨噬细胞和神经元几乎没有毒性。此外,由于LRRK2抑制剂本身就是为了治疗帕金森病而研发的,其具备良好的血脑屏障通透性——这是绝大多数抗癌药难以企及的优势。这意味着药物可以轻松进入大脑,直达病灶。同时,这些药物在帕金森病的临床试验中已经积累了大量的安全性数据,这为未来快速转化到GBM临床治疗奠定了坚实基础。
结语:让“抗病毒防御”成为肿瘤的软肋
夏宁邵院士团队的这项研究,巧妙地利用了帕金森病研究领域的成果,解决了胶质母细胞瘤对溶瘤病毒耐药的医学难题。通过阻断LRRK2-STAT1这一“分子开关”,曾经坚不可摧的肿瘤防御网变成了病毒进攻的突破口。虽然这一研究目前主要处于临床前阶段,但它为全球GBM患者点燃了新的希望。MedFind将持续关注此类“老药新用”的前沿动态,为患者提供最新的临床试验资讯和全球创新药物的获取路径。
参考文献
Li et al. Targeting leucine-rich repeat kinase 2 overcomes resistance to oncolytic herpes simplex virus-based therapies in glioblastoma. Nature Communications (2026). DOI: 10.1038/s41467-026-70132-9