原发性肝细胞癌(HCC),也就是我们常说的肝癌,是一种对人类健康构成巨大威胁的恶性肿瘤。它不仅是全球最常见的五大癌症之一,其致死率更是高居所有癌症的第四位。在中国,每年新诊断和死于肝癌的患者数量超过40万,几乎占全球的一半。这种严峻的现实,让每一个肝癌患者和他们的家庭都面临着巨大的身心考验。我国肝癌的特点是发病率高、诊断时常已是中晚期、预后差且复发率高,使得治疗之路异常艰难。然而,在早期肝癌阶段,通过积极有效的治疗,如手术切除或肝移植,患者仍有机会获得治愈。
在肝癌的治疗决策中,选择哪种手术方式,何时进行,以及预期的中长期效果如何,是患者和家属最为关心的核心问题。本文将深度解析肝癌的外科治疗策略,包括肝癌切除术和肝移植,并结合医学证据,帮助您更好地理解这些复杂的治疗选择。
肝癌的严峻现状与早期诊断的重要性
肝细胞癌(HCC)之所以如此棘手,与其独特的发病机制和高复发率息息相关。它不仅能无限制地生长,还具备极强的侵袭性和转移能力。肝癌细胞通过持续增殖、逃避生长抑制、抵抗细胞死亡以及诱导新生血管形成,不断侵犯周围组织甚至远处转移。多结节性肝癌的发生机制复杂,可能来源于肝内转移(IM)或多中心发生(MO),这直接影响治疗方案的选择和预发预测。
我国肝癌高发,主要与乙型肝炎病毒(HBV)感染、丙型肝炎病毒(HCV)感染、酒精性肝病、非酒精性脂肪性肝炎以及肝硬化等危险因素密切相关。这些慢性肝病是肝癌发生的温床,因此,对于高危人群,定期的肝功能检查、甲胎蛋白(AFP)检测以及腹部超声检查至关重要。早期发现的肝癌,往往肿瘤较小、数量较少,没有发生血管侵犯或远处转移,此时手术治疗的成功率最高,患者的生存希望也最大。因此,加强早期筛查、提高早期诊断率,是改善肝癌预后的关键。
肝癌治疗策略概览:根治与非根治手段
肝癌的治疗是一场综合战役,根据肿瘤的分期、肝功能状况和患者的全身条件,医生会制定个性化的治疗方案。治疗方式大体分为两大类:
- 手术治疗:包括肝癌切除术和肝移植,这两种方式理论上可以根治肝癌。
- 非手术治疗:包括局部治疗(如经动脉化疗栓塞(TACE)、射频消融、放射治疗)和系统治疗(如靶向药物、免疫治疗)。
通常情况下,如果条件允许,医生会优先考虑手术或消融等根治性治疗手段。然而,现实是残酷的,只有大约20%~30%的肝癌患者在初诊时具备手术根治的机会。对于那些暂时不符合根治性手术条件的患者,医生会努力通过非根治性手段来控制病情,甚至争取“转化”为可手术的机会:
- 转化治疗:对于原本无法手术的患者,通过如靶向治疗、免疫治疗等手段缩小肿瘤,使其达到手术条件。
- 新辅助治疗:对于有手术指征但预计根治效果不佳的患者,在手术前先行药物治疗,以期提高手术成功率和降低复发风险。
- 桥接治疗与降期治疗:主要用于肝移植前,前者是为了防止患者在等待供肝期间病情进展超出移植标准,后者则是将超出移植标准的患者通过治疗使其肿瘤负荷降低,重新符合移植标准。
- 辅助治疗:手术后,对于复发风险较高的患者,进行的进一步治疗以降低复发率。
如果上述努力仍未能实现根治,则会持续进行非根治性治疗,以延长患者生命,提高生活质量。
深入解读肝癌分期:BCLC与CNLC标准
准确的肝癌分期是制定治疗方案和评估预后的基石。目前国际上广泛采用的是BCLC(巴塞罗那临床肝癌)分期系统,同时我国也制定了更符合国情的CNLC(中国肝癌临床)分期系统。BCLC分期不仅考虑了肿瘤本身的特点,还结合了患者的肝功能状态和身体机能评分,这使得它能为不同阶段的患者提供明确的治疗推荐。
肝癌分期主要依据以下关键指标:
- 肿瘤大小与个数:这是判断肿瘤负荷和侵袭性的重要指标。
- 大血管癌栓:癌细胞侵犯肝内大血管是预后不良的显著标志。
- 淋巴结转移与远处转移:提示肿瘤已扩散至肝脏以外。
- 肝功能(如Child-Pugh分级)及全身状况(如ECOG评分):这些指标反映了患者对手术或药物治疗的耐受能力。
- 血清学肿瘤标志物(如甲胎蛋白AFP):有助于辅助诊断和监测疗效。
在外科医生眼中,影像学报告中的肿瘤大小、个数、侵犯范围以及与大血管的关系是决定能否手术、如何手术的关键信息。例如,大的单中心肿瘤如果恶性程度较低,通常会优先考虑切除;而多个肿瘤可能需要根据其分布和起源(单中心转移或多中心发生)来决定是消融、微创切除还是肝移植。
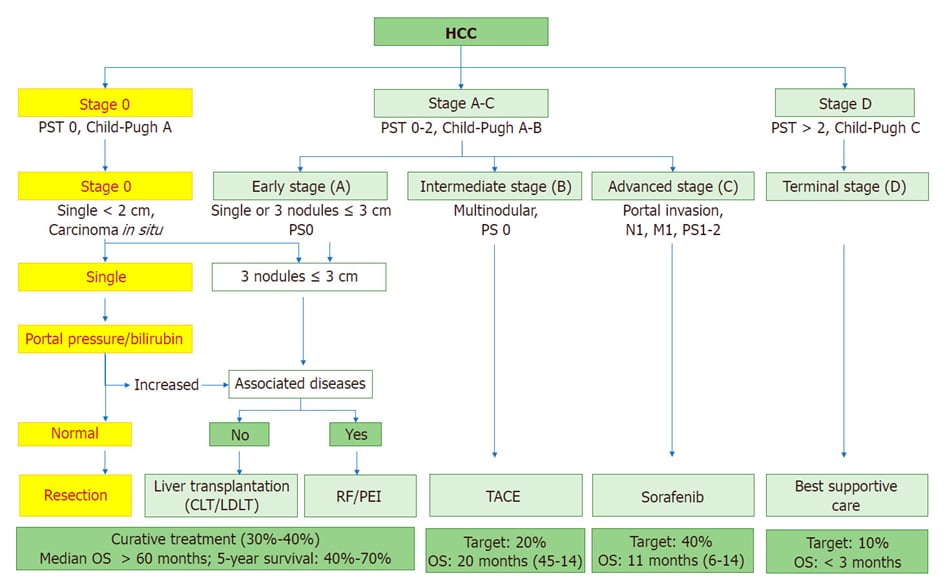
图1. HCC的BCLC分期
其中,肿瘤与大血管的关系最为关键。如果肿瘤紧邻或疑似侵犯可切除的大血管,可以考虑解剖性肝切除;但如果侵犯的是必须保留的大血管,则手术难度和风险会显著增加,甚至可能影响残肝功能,此时肝移植的优势就体现出来了。
肝切除术:根治肝癌的“黄金标准”
肝癌切除术是目前治疗早期肝癌最常用且最有效的根治性手段之一。它通过切除肿瘤及其周围部分肝组织,并在肝内离断血管胆管,以达到清除病灶的目的。成功的肝切除术要求剩余的肝脏组织质量和体积足够,以保证患者术后的肝功能。
解剖性与非解剖性肝切除术
肝切除术主要分为两种类型:
- 解剖性肝切除术:这是肝癌肝切除的首选方式。它遵循肝脏的解剖学分段,完整切除肿瘤及其所在肝段、亚段或联合肝段,包括相应的门静脉分支流域。这种方式的理论优势在于能够更彻底地清除可能存在的微小转移灶,降低肿瘤随门静脉血流在肝内播散的风险,从而提高患者的长期生存率和无瘤生存率。多项研究显示,解剖性肝切除术在5年生存率和无瘤生存率方面均优于非解剖性肝切除术。
- 非解剖性肝切除术:当肿瘤有完整包膜、患者肝硬化严重、肝功能储备差(如Child B级)、合并门静脉高压,或肿瘤紧邻必须保留的重要血管时,可考虑进行非解剖性切除。这种方式主要切除肿瘤本身及其边缘少量正常肝组织,旨在保留更多健康肝脏,减少手术创伤和并发症。
肝切除的范围需要根据肿瘤占据的肝段数量来决定,同时要确保切除后剩余肝段数量不低于患者安全生存所需的最低限度。需要注意的是,外生性肿瘤的大小通常不会直接影响手术的可行性,而是取决于其侵犯范围和与周围重要结构的关系。
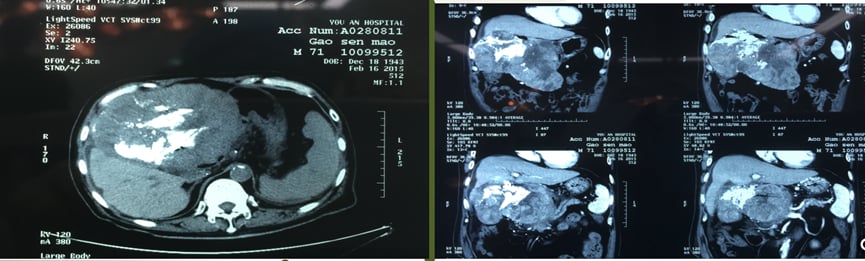
图2. IVb段局部肿瘤切除加胃、横结肠切除
肝功能储备与微创外科的进步
无论是肝切除还是肝移植,对患者的肝功能储备都有严格要求。医生在评估时不仅关注Child-Pugh分级,更重视肝脏的整体代偿能力。对于存在门静脉高压的患者,可能需要结合小范围切除、腹腔镜下消融、脾动脉结扎或脾切除等手段。近年来,微创外科技术(如腹腔镜和机器人辅助手术)在肝癌切除领域取得了显著进展,其手术效果已接近甚至在某些方面优于传统开腹手术,具有创伤小、恢复快、住院时间短等优点。微创技术还扩展了消融治疗的适应症,提高了治疗安全性,例如对紧邻胆囊、膈肌或与周围脏器相邻的表面肿瘤。
肝移植:为肝癌患者带来“重生”的希望
相对于肝切除术,肝移植在肝癌治疗中扮演着更为特殊和终极的角色。它不仅能够彻底切除病变的肝脏,同时解决肝癌与潜在肝硬化等肝脏疾病的双重问题。正如原文所述,肝移植具有“高风险、高投入、高回报”的突出特点。
- 高风险:肝移植是外科领域最复杂、风险最高的全身性手术之一。它涉及到供体和受体的匹配、术中大出血的风险、术后免疫排斥反应、感染以及长期服用免疫抑制剂带来的副作用。
- 高投入:肝移植的经济成本高昂,包括手术费、术后抗排斥药物费用、长期随访费用等,对患者家庭是巨大的经济负担。此外,供体肝脏的稀缺性也是一个重要挑战。
- 高回报:尽管风险和投入巨大,肝移植能为符合条件的肝癌患者带来无与伦比的“回报”。它不仅能根治肝癌病灶,还能替换掉患有严重肝硬化或慢性肝病的病肝,从根本上解决肝癌复发的土壤问题,显著提高患者的长期生存率和生活质量。据中国肝移植注册中心数据,肝癌肝移植在我国肝移植总数中占有相当大的比例。
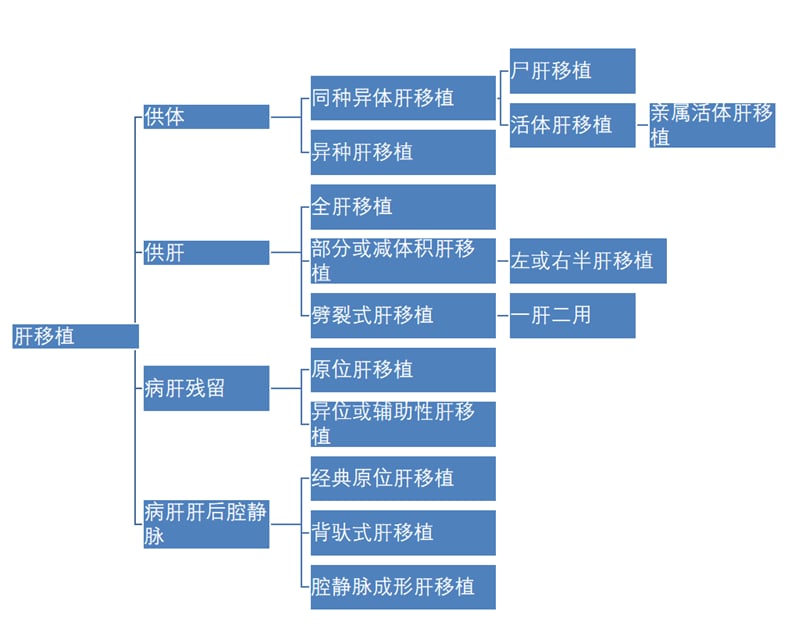
图3. 肝移植手术分类
肝移植的适应症与关键标准:米兰与UCSF
为了确保肝移植的成功率并合理利用有限的供体资源,国际上制定了一系列严格的肝癌肝移植标准。其中最著名且广泛使用的是米兰标准(Milan criteria)和美国加州大学旧金山分校(UCSF)标准。
- 米兰标准:主要指单个肿瘤直径≤5厘米,或2-3个肿瘤且最大直径≤3厘米,无大血管侵犯和淋巴结或远处转移。符合米兰标准的患者,肝移植后4年生存率可达75%,肿瘤复发率低于10%,效果显著。
- UCSF标准:在米兰标准基础上适度放宽,允许单个肿瘤直径≤6.5厘米,或2-3个肿瘤且最大直径≤4.5厘米,总肿瘤直径≤8厘米,无大血管侵犯和淋巴结或远处转移。UCSF标准下的肝移植患者,1年生存率可达90%,5年生存率为75.2%,同样取得了良好的效果。
这些标准的存在,是为了筛选出那些通过肝移植能获得最大生存获益的患者,避免供体浪费。同时,肝移植的目的也多种多样,从抢救生命到改善生活质量,如图4所示。
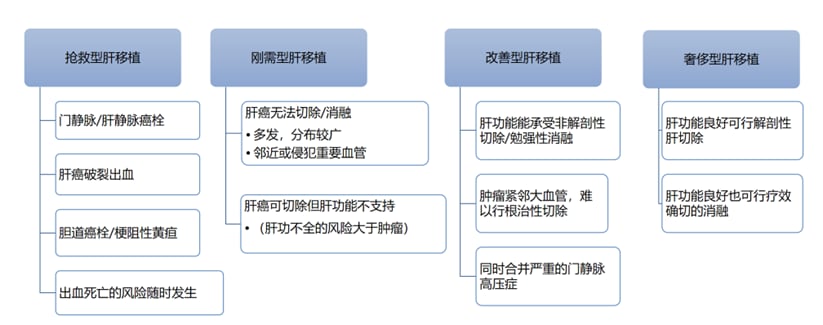
图4. 肝移植的目的分类
桥接治疗与降期治疗:为肝移植创造机会
由于供体肝脏的稀缺性,许多符合肝移植标准的患者不得不经历漫长的等待。在此期间,肿瘤可能会进展,导致患者失去移植机会。因此,桥接治疗(Bridging therapy)和降期治疗(Downstaging therapy)应运而生,成为争取移植机会的关键策略。
- 桥接治疗:针对已经符合移植标准但正在等待供肝的患者。其目的是在等待期内控制肿瘤生长,防止肿瘤进展超出移植标准。常用的桥接治疗手段包括微创治疗,如经动脉化疗栓塞(TACE)、射频消融,有时还会辅以靶向药物治疗来增强效果。
- 降期治疗:针对初步评估时超出移植标准(如米兰或UCSF标准)的患者。通过积极治疗,努力使肿瘤负荷降低,重新符合移植标准,从而获得肝移植的机会。降期治疗通常更为激进,可能涉及多种手段的联合应用,如消融、TACE、选择性体内放射治疗(Y-90放射栓塞)或立体定向放射治疗(SBRT)。对于较大肿瘤或合并大血管癌栓的患者,还会在这些局部治疗的基础上,辅以靶向药物治疗或免疫治疗。
临床实践证明,如果肝癌患者通过降期治疗成功使肿瘤缩小并符合米兰标准,其移植后的长期无复发生存率和总生存率,与一开始就符合米兰标准的患者是相当的。这为许多原本被判“无缘移植”的患者带来了新的希望。例如,对于巨大的左半肝肿瘤合并门静脉癌栓,或原发性肝癌消融后多发复发并伴有肺转移的复杂病例,经过介入治疗、放疗、靶向药物甚至免疫治疗的综合降期后,也有成功接受肝移植并获得良好预后的案例。
术后复发:肝癌治疗的持久战与策略
遗憾的是,无论是肝切除还是肝移植,术后肿瘤复发仍是肝癌治疗中面临的严峻挑战。复发不仅意味着疾病的卷土重来,往往也预示着更差的预后,尤其是复发常发生在术后2年内。
肝切除术后复发的原因
- 肿瘤残留:术前影像学检查可能未能发现的微小病灶,或手术中切除不彻底,导致肿瘤细胞残留。
- 术中播散:手术过程中对肿瘤的挤压可能导致癌细胞脱落,在肝内或腹腔内播散转移。
- 新生肿瘤:由于患者通常伴有肝硬化等基础肝病,剩余的肝脏仍有慢性炎症和损伤,可能诱发新的肝癌灶形成(多中心发生),尤其在乙肝病毒持续感染的患者中更为常见。
肝移植术后复发的原因
尽管肝移植清除了整个病肝,但仍有复发可能,原因包括:
- 超出移植标准:部分患者在术后病理中发现肿瘤负荷或恶性程度超出术前评估的移植标准。
- 肿瘤生物学特性:肿瘤分化程度低、存在微血管侵犯和卫星灶,或术前甲胎蛋白(AFP)水平极高(如>400mg/dL),都提示肿瘤恶性程度高,复发风险大。
- 免疫抑制剂影响:长期使用免疫抑制剂在抑制免疫排斥的同时,可能降低机体对癌细胞的监控和清除能力,从而增加肿瘤复发风险。
复发后的治疗往往需要多学科团队(MDT)的共同协作,采取综合治疗手段,包括再次手术切除、TACE、消融治疗、放射治疗,以及系统抗肿瘤治疗(如靶向药物、免疫检查点抑制剂)。值得注意的是,对于肝移植术前及术后使用免疫检查点抑制剂,由于可能与免疫抑制方案相互影响,目前仍需慎重,并在专业医生指导下进行。
肝切除还是肝移植:终极抉择的深度考量
“早期肝癌,究竟是首选肝切除,还是直接进行肝移植?”这是一个长期存在争议的问题。一些研究曾认为早期肝癌首选肝移植比“补救性肝移植”(即切除失败后再次移植)效果更好。然而,随着医学技术的发展和对手术适应症的精准把握,当前主流观点认为,在特定条件下,首选肝癌切除术可能更为合理。
支持“切除优先”的理由主要有:
- 相似的生存率:对于符合特定标准的早期肝癌,首选肝切除的患者长期生存率与首选肝移植的患者可能相似。这意味着在某些情况下,患者无需承担肝移植带来的巨大风险和负担,也能获得同样良好的治疗效果。
- 避免移植相关风险:肝移植最大的挑战之一是术后长期的免疫抑制治疗,这会增加感染、免疫排斥反应以及诱发其他恶性肿瘤的风险。如果能通过肝切除达到同样效果,则可避免这些风险。
- 缓解供体器官紧张:肝脏供体资源全球稀缺。如果将可切除的早期肝癌都用于肝移植,无疑会加剧供体紧张,使得那些真正需要肝移植续命的终末期肝病患者失去机会。
当然,“切除优先”并非适用于所有情况。在以下情况下,肝移植的优势会更加凸显:
- 合并严重肝硬化或肝功能储备极差:切除部分肝脏可能导致肝功能衰竭。
- 肿瘤数目多或分布广,难以通过切除彻底清除:肝移植可以一劳永逸地切除所有病灶肝脏。
- 无法通过其他手段控制的肿瘤复发:对于多次复发且不适合再次切除的患者,肝移植可能是最后的希望。
因此,对于肝癌患者而言,是选择肝切除还是肝移植,需要个体化评估。专业的医疗团队,特别是多学科团队(MDT),会综合考虑肿瘤的大小、数量、位置、侵犯情况,以及患者的肝功能、全身状况、有无合并症、经济能力和意愿等所有因素,为您制定最适合的治疗方案。我们强烈建议患者和家属积极与医生沟通,充分了解每种方案的利弊,做出最明智的抉择。
MedFind:您的抗癌之路的坚实伙伴
在面对肝癌这一复杂而残酷的疾病时,每一位患者和家属都需要全面、准确的信息支持和可靠的资源协助。在您面临如此复杂的肝癌治疗决策时,无论是寻求最新的治疗方案,还是了解前沿抗癌药物的跨境直邮渠道,MedFind都能为您提供专业、可靠的支持和帮助。我们致力于帮助患者和家属获取最全面的抗癌资讯,并提供AI辅助问诊,让每一步选择都更有依据、更有信心。
结语
肝癌的治疗是一个漫长而充满挑战的过程,但希望始终存在。无论是选择肝切除还是肝移植,亦或是其他综合治疗手段,最重要的都是早期发现、精准诊断、科学决策和积极配合。通过多学科团队的专业指导和患者自身的坚定信念,我们相信,越来越多的肝癌患者能够战胜病魔,重获健康。
参考文献
- [1] Reig M, Forner A, Rimola J, et al. BCLC strategy for prognosis prediction and treatment recommendation: The 2022 update[J]. J Hepatol, 2022, 76(3): 681-693.
- [2] Shindoh J, Makuuchi M, Matsuyama Y, et al. Complete removal of the tumor-bearing portal territory decreases local tumor recurrence and improves disease-specific survival of patients with hepatocellular carcinoma[J]. J Hepatol, 2016, 64(3): 594-600.





