乳腺癌:全球女性健康的严峻挑战与治疗新视野
乳腺癌是全球女性最常见的恶性肿瘤之一,其发病率高居不下,严重威胁着女性的生命健康。尽管医学科技不断进步,但乳腺癌的发生和发展机制仍有许多未解之谜,寻找更有效、更精准的治疗靶点和策略一直是医学研究的重点。深入理解肿瘤细胞内部的分子通路,对于开发创新疗法至关重要。
近期,一项由山东大学杨其峰团队在《Advanced Science》上发表的突破性研究,为乳腺癌的治疗带来了新的曙光。该研究深入探讨了TRIM38蛋白在乳腺癌进展中的抑制作用及其独特的分子机制,揭示了其作为潜在治疗靶点的巨大潜力。
TRIM38:乳腺癌进展的潜在抑制因子
TRIM38,全称为三组基序(TRIM家族)成员38,是一种E3泛素连接酶。此前,它主要因其在先天免疫和炎症反应中的调控作用而受到关注。然而,TRIM38在肿瘤,特别是乳腺癌中的具体功能,此前一直未被完全阐明。
这项研究发现,TRIM38在乳腺癌组织中的表达水平显著下调,并且这种低表达与乳腺癌患者的不良临床预后密切相关。这提示TRIM38可能在乳腺癌的发生发展中扮演着抑癌基因的角色。
TRIM38的抑癌作用证据
为了验证TRIM38的抑癌功能,研究团队进行了大量的体外细胞实验和体内动物实验。结果一致表明,增加TRIM38的表达能够显著抑制乳腺癌细胞的增殖(生长)、迁移(转移能力)和侵袭(浸润周围组织的能力)。这些实验证据强有力地支持了TRIM38在乳腺癌进展中具有抑制作用的结论。
TRIM38如何抑制乳腺癌?核心机制深度解析
研究进一步深入探讨了TRIM38抑制乳腺癌进展的分子机制,发现其关键作用在于调控细胞的自噬(Autophagy)过程。
自噬:肿瘤细胞的“双刃剑”
自噬是细胞内一种重要的自我降解和回收机制,它通过形成自噬体包裹细胞内的受损细胞器或蛋白质,并将其运送到溶酶体进行降解。在肿瘤发生发展中,自噬扮演着“双刃剑”的角色:在肿瘤早期,自噬可能通过清除受损细胞器和蛋白质来抑制肿瘤的发生;而在已建立的肿瘤中,自噬又可能帮助肿瘤细胞适应恶劣的微环境,抵抗治疗,从而促进肿瘤的生存和转移。因此,精准调控自噬是肿瘤治疗策略中的一个重要方向。
SQSTM1/p62:自噬通路的关键枢纽
SQSTM1/p62(隔离体1)是一种多功能的信号调控因子,也是自噬过程中常见的底物受体。它在自噬过程的多个阶段发挥关键作用,例如通过与LC3蛋白结合,将泛素化的底物募集到自噬体中进行降解。除了参与自噬通路,SQSTM1/p62还涉及细胞凋亡和氧化应激反应等多种细胞生物学过程。在乳腺癌中,SQSTM1/p62的作用也十分复杂,其积累可能增强肿瘤干性并降低化疗敏感性,因此对其调控机制的深入研究具有重要意义。
TRIM38通过泛素化修饰阻断自噬流
本研究最核心的发现是,TRIM38被鉴定为SQSTM1/p62的一种新型E3泛素连接酶。这意味着TRIM38能够特异性地识别并结合SQSTM1/p62,并在其赖氨酸420(K420)位点催化一种特殊的泛素化修饰——K63连接泛素化。与常见的导致蛋白质降解的K48连接泛素化不同,K63连接泛素化通常不导致蛋白质降解,而是改变蛋白质的功能或定位。
研究进一步揭示,这种由TRIM38介导的K63连接泛素化修饰,在空间上阻碍了SQSTM1/p62与LC3蛋白的相互作用。由于SQSTM1/p62与LC3的结合是自噬体形成和自噬流正常进行的关键步骤,一旦这种相互作用被破坏,自噬流就会被阻断。自噬流的受阻意味着细胞无法有效地清除细胞质中的物质,从而抑制了乳腺癌细胞的进展。

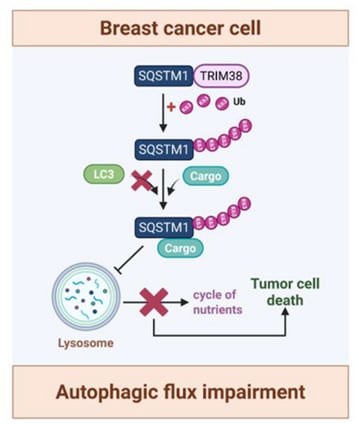
TRIM38调节自噬流的作用机制(摘自Advanced Science )
了解更多乳腺癌治疗方案及海外用药选择,可访问 MedFind 药物信息平台,获取最新的药物资讯和治疗进展。
TRIM38:乳腺癌治疗新靶点的巨大潜力
这项研究的发现,不仅深入阐明了TRIM38在乳腺癌进展中的抑制作用及其独特的分子机制,更重要的是,它为乳腺癌的治疗提供了新的、具有潜力的治疗靶点。
通过靶向TRIM38/SQSTM1/自噬通量轴,未来有可能开发出新型的抗乳腺癌药物。例如,通过药物手段上调TRIM38的表达或增强其E3泛素连接酶活性,从而恢复其对SQSTM1/p62的泛素化修饰,进而阻断自噬流,抑制乳腺癌细胞的生长和转移。这种策略有望克服现有治疗的局限性,为乳腺癌患者提供更有效、更精准的治疗选择。
如果您正在寻找乳腺癌相关药物,MedFind 国际直邮服务 可为您提供便捷的购药途径,确保您能及时获取所需的抗癌药物。
这项研究的成果,强调了TRIM38作为自噬调控的关键因子,在乳腺癌治疗中的潜在应用价值。它不仅为基础研究领域增添了新的知识,也为转化医学领域指明了方向,有望推动乳腺癌靶向治疗药物的研发进程。
通过 MedFind AI 辅助问诊,获取个性化的治疗建议和药物解读,帮助您更好地理解自身病情和治疗方案。
结语
山东大学杨其峰团队的这项研究,无疑是乳腺癌研究领域的一个重要里程碑。它不仅揭示了TRIM38在乳腺癌抑制中的关键作用及其精妙的分子机制,更重要的是,它为乳腺癌的精准治疗提供了全新的思路和潜在的靶点。随着对TRIM38及其相关通路的进一步研究,我们有理由相信,未来将会有更多创新的治疗策略被开发出来,最终惠及广大的乳腺癌患者,为她们带来更长的生存期和更高的生活质量。





