食管鳞癌免疫治疗没效果,问题一定出在PD-L1不高吗?越来越多证据提示,肠道菌群可能正在影响PD-1免疫治疗疗效。对局部晚期食管鳞癌患者而言,新辅助免疫治疗已经成为重要选择,但只有部分患者能达到病理学完全缓解,更多患者面临“影像缩小不明显”“术后仍有残留”“免疫联合治疗后进展”等现实问题。最新研究把关键线索指向一种肠道细菌及其代谢物:唾液乳杆菌和吲哚-3-乳酸。
这项发表于Cell Host & Microbe的研究,为食管鳞癌免疫耐药提供了一个清晰路径:特定肠道菌群富集,产生更高水平的吲哚-3-乳酸,激活T细胞上的AhR信号,抑制抗肿瘤免疫,最终削弱PD-1治疗效果。对患者和家属来说,它的意义不只是“发现了一个机制”,更重要的是提示:未来食管鳞癌免疫治疗的评估,可能不能只看肿瘤本身,也要看肠道微生态。

食管鳞癌免疫治疗耐药研究提示肠道菌群可能影响PD-1疗效
食管鳞癌为何会免疫耐药
食管鳞癌是我国高发的消化道恶性肿瘤之一。对于局部晚期患者,单纯手术往往难以解决微小转移和局部复发风险,新辅助治疗的目标是在手术前尽可能缩小肿瘤、清除隐匿病灶,并提高根治性切除机会。
以PD-1抑制剂为核心的新辅助免疫治疗,已经在食管鳞癌中显示出重要价值。但免疫治疗并非“人人有效”。研究背景数据显示,目前约20%的局部晚期食管鳞癌患者可实现病理学完全缓解,也就是手术标本中找不到存活肿瘤细胞。换句话说,大量患者仍可能出现反应不足或耐药。
免疫耐药并不等于“药物没有用”,它通常意味着肿瘤与人体免疫系统之间存在更复杂的制衡。常见原因包括:
- 肿瘤抗原呈递不足:免疫系统难以识别癌细胞。
- T细胞功能耗竭:能杀伤肿瘤的T细胞变得“有心无力”。
- 肿瘤微环境抑制:癌组织周围存在大量免疫抑制细胞、因子或代谢物。
- PD-L1并非唯一指标:PD-L1表达可以帮助判断部分患者获益概率,但不能完整解释所有疗效差异。
- 肠道菌群参与调控:肠道细菌及其代谢物可能改变全身免疫状态,影响免疫治疗反应。
这项研究发现了什么
研究团队对食管癌患者治疗过程中的粪便样本进行了纵向分析,重点观察免疫治疗前后肠道菌群如何变化。所谓纵向样本,意味着不是只在某一个时间点取样,而是跟踪治疗过程中的动态改变,因此更接近真实临床过程。
研究分析了122份纵向粪便样本,采用16S rDNA测序和宏基因组测序等技术。结果显示,治疗无应答患者的肠道微生物多样性显著低于应答患者,并且一种名为唾液乳杆菌的细菌在耐药患者肠道中持续富集。
更关键的是,研究并未停留在“相关性”。通过人源化菌群移植和原位食管鳞癌小鼠模型,研究者进一步证实:当唾液乳杆菌定植后,肿瘤对PD-1治疗出现明显耐药。这说明它不只是一个旁观指标,而可能直接参与了免疫治疗失败过程。
| 研究层面 | 核心发现 | 对患者的意义 |
|---|---|---|
| 临床样本 | 无应答患者肠道菌群多样性更低 | 肠道微生态状态可能影响免疫疗效 |
| 菌群测序 | 唾液乳杆菌在耐药患者中显著且持续富集 | 未来可能成为疗效预测线索 |
| 动物模型 | 定植唾液乳杆菌可导致PD-1治疗耐药 | 提示该菌可能具有功能性作用 |
| 治疗特异性 | 该过程影响免疫治疗,但不影响常用化疗药疗效 | 说明耐药机制更偏向免疫调控,而非一般性药物抵抗 |
ILA如何削弱PD-1疗效
肠道菌群影响免疫治疗,往往不是细菌直接“跑到肿瘤里”,而是通过代谢物改变人体免疫系统。该研究锁定的关键代谢物是吲哚-3-乳酸,英文简称ILA。它由唾液乳杆菌产生,在耐药患者的肠道和血清中水平均显著升高。
机制研究显示,ILA能够影响肿瘤微环境中的CD8+ T细胞。CD8+ T细胞本是免疫治疗中杀伤癌细胞的主力,但在长期抗原刺激和免疫抑制环境下,可能逐步进入耗竭状态。研究特别提到,ILA会诱导NKG7+ CD8+祖样耗竭T细胞向终末耗竭状态转化。
简单理解,祖样耗竭T细胞仍保留一定“再激活潜力”,PD-1治疗的一个关键目标,就是让这部分T细胞重新恢复抗癌能力;而终末耗竭T细胞则更接近“功能衰竭终点”,即使用PD-1抑制剂,也更难被唤醒。
ILA的作用路径主要与AhR有关。AhR全称为芳香烃受体,是一种能感知多种内源性和外源性代谢物的受体。研究发现,ILA可结合并激活T细胞上的AhR,继而抑制NF-κB信号通路,使抗肿瘤免疫反应下降。
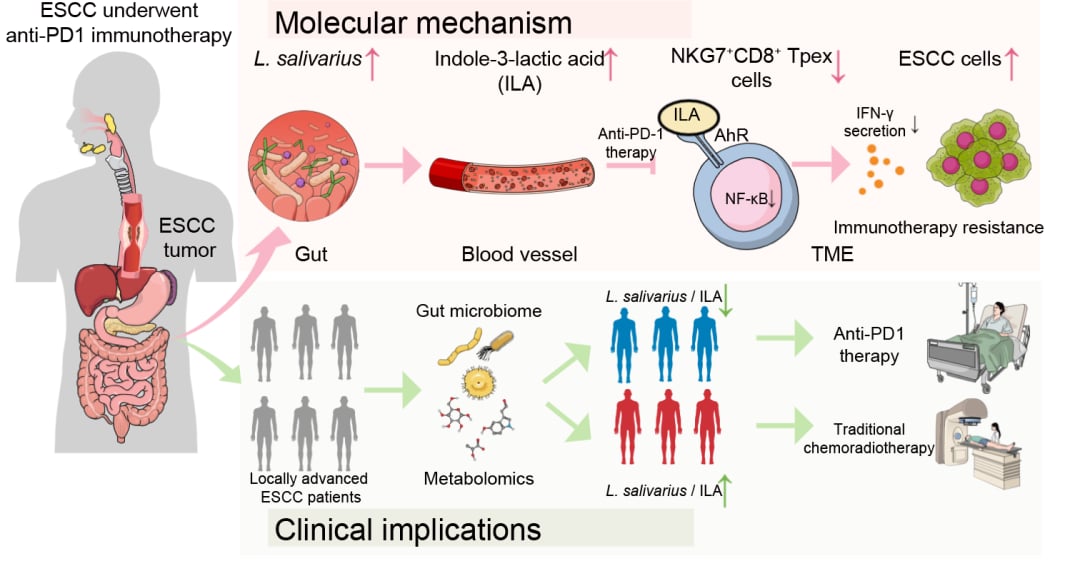
唾液乳杆菌及其代谢产物ILA影响食管鳞癌免疫治疗疗效的机制示意图
为什么偏偏是食管癌
一个重要问题是:如果ILA来自肠道,为什么它对食管鳞癌的免疫治疗影响如此突出?研究通过TCGA数据库分析发现,AhR在食管癌组织中的表达水平位居所有肿瘤类型之首。这为ILA表现出的“趋食管”特异性提供了合理解释。
这并不意味着所有食管癌患者都一定存在ILA升高,也不意味着检测到某个菌就必然免疫失败。更准确的理解是:在一部分食管鳞癌患者中,唾液乳杆菌和ILA可能构成了“菌群-代谢-免疫”耐药轴,削弱PD-1治疗本该激活的T细胞反应。
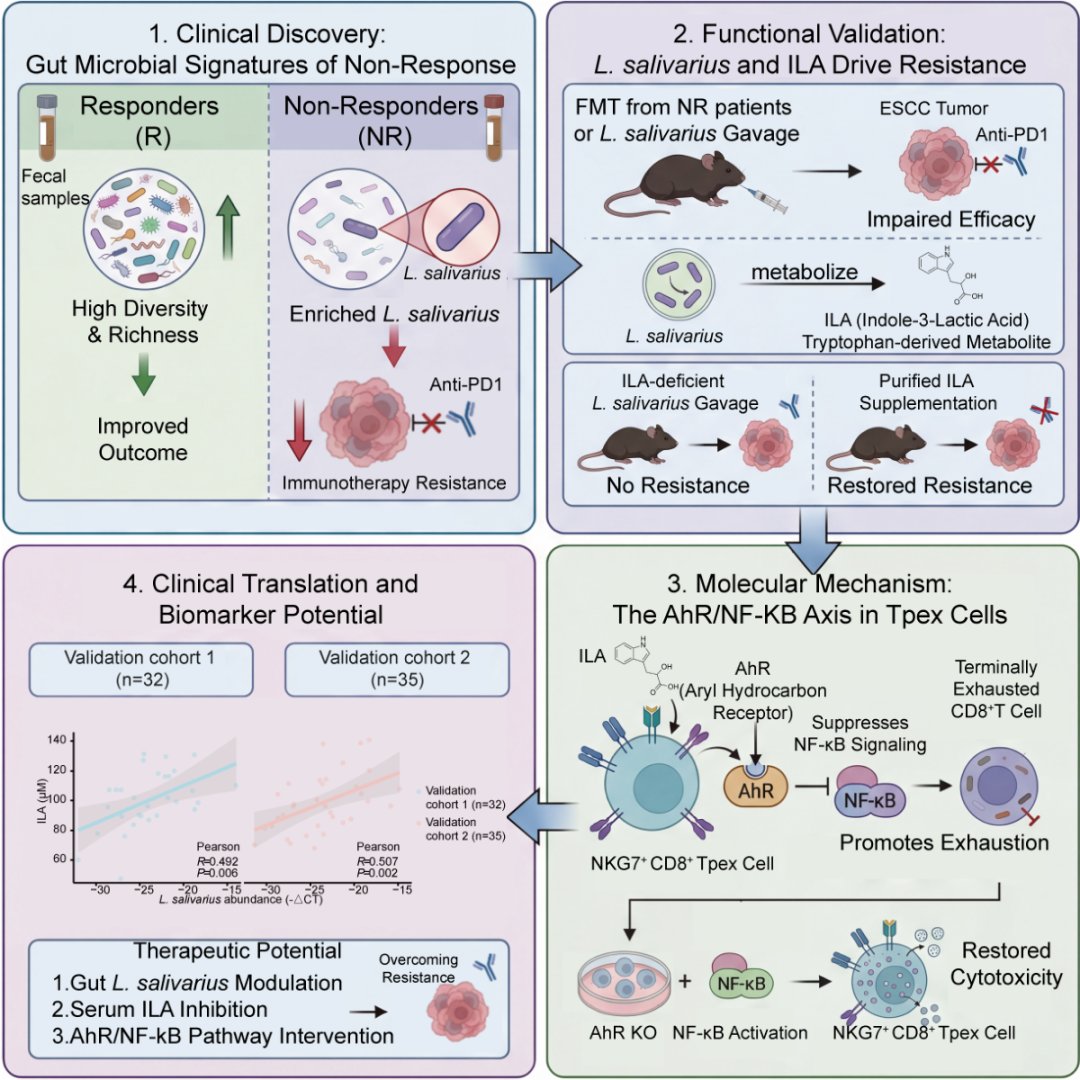
肠道菌群代谢物ILA介导食管鳞癌PD-1免疫耐药的可视化摘要
菌群检测能预测疗效吗
研究在两个独立临床验证队列中进一步确认,肠道唾液乳杆菌丰度在预测食管鳞癌患者免疫治疗反应方面具有较高准确性,AUC达到0.830,并且优于临床常用的PD-L1表达检测。AUC可以理解为一个预测模型区分“可能有效”和“可能无效”的能力,数值越接近1,区分能力越强。
更值得关注的是,唾液乳杆菌丰度和ILA水平还是患者总生存期的独立预测因子。这意味着它们可能不只是短期疗效指标,也可能反映更深层的疾病进程和免疫状态。
| 指标 | 研究结果 | 临床解读 |
|---|---|---|
| 唾液乳杆菌丰度 | 耐药患者中持续富集 | 可能提示PD-1治疗反应较差 |
| ILA水平 | 耐药患者肠道和血清中升高 | 可能代表菌群代谢驱动的免疫抑制状态 |
| 预测准确性 | AUC=0.830 | 显示出较强疗效预测潜力 |
| 与PD-L1比较 | 预测表现优于PD-L1表达检测 | 提示菌群指标可能补充现有评估体系 |
| 总生存期 | 菌丰度和ILA水平均为独立预测因子 | 可能帮助识别高风险患者 |
需要强调的是,这类菌群检测目前仍处于研究转化阶段。患者不应自行凭商业肠道菌群报告改变治疗方案,更不应因为某个菌“偏高”就停止免疫治疗。真正有价值的做法,是把菌群信息与分期、病理、影像、PD-L1、治疗反应、体能状态和医生判断结合起来。
患者现在能做什么
这项研究很前沿,但患者最关心的问题是:现在是否需要立刻做菌群检测、吃益生菌或调整饮食?答案要分层看。
不要盲目补充益生菌
很多患者一听到“肠道菌群影响免疫治疗”,第一反应是购买益生菌。但这项研究恰恰提醒我们:并非所有被称为“有益菌”的细菌,在所有肿瘤和所有治疗场景下都一定有益。某些菌在特定背景下可能帮助免疫,某些菌则可能削弱免疫治疗。
因此,接受PD-1治疗的食管鳞癌患者,不建议在没有医生指导的情况下长期、大剂量、混合使用益生菌产品,尤其是在新辅助治疗、免疫联合化疗、术前评估等关键阶段。
抗生素也不能随便用
抗生素可能改变肠道菌群结构,既可能清除不利菌,也可能破坏有益菌群。对于正在免疫治疗的患者,抗生素应遵循明确感染证据和医生处方,避免因为腹胀、轻微腹泻或“预防感染”自行使用。
饮食管理重在稳定
肠道微生态与饮食密切相关,但肿瘤治疗期间的饮食目标不是追求极端“抗癌食谱”,而是维持营养、减少炎症和保持肠道功能稳定。建议重点关注:
- 保证蛋白质:鱼、蛋、禽肉、瘦肉、奶制品或医学营养制剂,有助于手术和放化疗恢复。
- 适量膳食纤维:能进食者可选择软烂蔬菜、燕麦、杂粮粥等,但吞咽困难者需调整质地。
- 避免刺激食管:少吃过烫、辛辣、粗硬、腌制和酒精类食物。
- 腹泻时及时评估:免疫相关肠炎、感染、放疗反应、饮食不耐受都可能导致腹泻,处理方式不同。
- 吞咽困难要早干预:长期进食不足会降低体能状态,影响免疫治疗和手术耐受性。
免疫治疗无效后怎么办
如果食管鳞癌患者接受PD-1治疗后疗效不佳,第一步不是急着换药,而是明确“无效”的性质。临床上至少要区分三种情况:
- 原发耐药:治疗开始后肿瘤不缩小,甚至快速进展。
- 获得性耐药:初期有效,之后再次进展。
- 假性进展或炎症反应:影像上看似增大,但实际可能与免疫细胞浸润有关,需医生综合判断。
常见后续策略包括继续联合治疗、调整化疗方案、评估手术机会、放疗介入、参加临床试验、进行分子检测或重新评估病理与分期。对于局部晚期患者,治疗目标常常是争取根治;对于复发转移患者,目标则更多是延长生存、控制症状和维持生活质量。
| 临床情境 | 优先评估内容 | 可能讨论的方向 |
|---|---|---|
| 新辅助免疫后未达理想缓解 | 影像、内镜、病理、手术可切除性 | 手术时机、追加治疗、围术期方案调整 |
| 免疫联合化疗后进展 | 进展速度、转移部位、体能状态 | 二线化疗、局部治疗、临床试验 |
| 疑似免疫相关不良反应 | 腹泻、皮疹、肝酶、肺部症状、内分泌指标 | 暂停免疫、激素治疗、专科会诊 |
| 疗效判断不清 | 是否符合假性进展可能、是否需要复查 | 短期复评、多学科会诊、病灶活检 |
副作用如何居家识别
PD-1免疫治疗通过激活免疫系统抗癌,也可能让免疫系统攻击正常组织,形成免疫相关不良反应。食管鳞癌患者常同时接受化疗、放疗或手术,症状来源更复杂,因此居家监测非常重要。
- 腹泻:每天排便次数明显增加、便血、腹痛或发热,应警惕免疫相关肠炎,不要自行长期服止泻药掩盖症状。
- 咳嗽气促:新出现干咳、胸闷、活动后气短,需排查免疫性肺炎、感染或放射性肺炎。
- 皮疹瘙痒:轻度可拍照记录并联系医生,范围扩大、起水疱或伴发热需及时就医。
- 乏力心慌:除贫血和营养不足外,还要考虑甲状腺、肾上腺、垂体等内分泌异常。
- 肝功能异常:很多患者没有明显症状,需按治疗周期复查肝酶和胆红素。
出现中重度不良反应时,免疫治疗可能需要暂停,并由医生判断是否使用糖皮质激素或其他免疫抑制治疗。患者最应避免的是“两头极端”:一是轻视症状拖到危重,二是因轻微不适自行永久停药。
这会改变治疗指南吗
当前研究为食管鳞癌免疫耐药提供了高质量机制证据和临床验证线索,但从研究发现到写入指南,还需要更多前瞻性临床试验验证。未来可能出现的方向包括:
- 治疗前菌群风险分层:识别可能对PD-1疗效较差的患者。
- ILA血清检测:作为免疫耐药风险和预后评估指标之一。
- 微生态干预:通过饮食、定向菌群调节或代谢物干预改善免疫微环境。
- AhR相关靶向策略:探索阻断ILA-AhR轴以恢复T细胞功能。
- 联合治疗优化:把菌群信息纳入免疫、化疗、放疗和手术的综合决策。
对患者而言,最现实的价值是:当免疫治疗效果不理想时,不要只用“运气不好”解释,也不要只盯着PD-L1一个指标。更完整的评估,可能帮助找到新的转机。
如何获得前沿治疗信息
食管鳞癌治疗正在快速进入“免疫联合、围术期管理、微生态研究、精准分层”的阶段。患者真正需要的不是零散信息,而是把病理分型、分期、既往治疗、影像变化、基因检测、PD-L1结果、用药可及性和临床试验机会放在一起判断。
MedFind长期关注全球抗癌药物、权威指南和前沿研究进展,可帮助患者和家属梳理食管鳞癌PD-1治疗方案、免疫耐药后的下一步选择、海外新药信息及临床证据。对于国内暂未充分可及的抗癌药物需求,MedFind也提供合规路径下的抗癌药品跨境直邮信息支持;对于看不懂病理报告、影像复查和治疗方案差异的患者,可通过AI辅助问诊进行结构化解读,再带着更清晰的问题与主管医生沟通。
免疫治疗耐药并不代表治疗走到终点。更早识别风险,更准确理解证据,更快连接可及方案,往往就是患者争取下一次机会的关键。
【参考文献】
Zhou et al., Gut microbiota-derived indole-3-lactic acid suppresses anti-PD-1 efficacy in esophageal squamous cell carcinoma, Cell Host & Microbe (2026), https://doi.org/10.1016/j.chom.2026.02.019