神经鞘瘤反复长、双侧前庭神经鞘瘤来得早、家里还有类似病史,基因检测到底该怎么做才不容易漏?对NF2相关神经鞘瘤病患者和家属来说,最关键的不是只知道“有肿瘤”,而是尽快弄清楚:是不是NF2基因出了问题、属于胚系还是体细胞改变、有没有大段缺失、后续随访和治疗该怎么选。
这类肿瘤的难点在于,NF2改变并不只有常规测序容易识别的点突变,还可能是整基因缺失、拷贝数变化、框内缺失等复杂类型。如果检测方法单一,结果就可能“假阴性”。而一旦明确Merlin功能缺失,不仅关系到患者本人手术、放疗、随访和临床试验机会,也直接影响家属是否需要遗传咨询和风险筛查。
NF2相关神经鞘瘤病是什么
NF2相关神经鞘瘤病是一类由NF2基因致病改变引起的肿瘤易感综合征,最典型的表现是双侧前庭神经鞘瘤,也可出现其他颅内、脊柱或周围神经系统相关肿瘤。NF2基因编码的蛋白叫Merlin,它相当于细胞生长的“刹车系统”之一。只要NF2双等位基因相继失活,Merlin功能丢失,细胞就更容易走向异常增殖。
临床上,NF2改变大致可分为两类:
- 胚系变异:出生时就存在于全身细胞,提示遗传性风险,家属也可能受影响。
- 体细胞变异:只存在于肿瘤组织内,多见于散发病例,不一定会遗传给下一代。
真正决定诊疗价值的,不只是“有没有NF2变异”,而是要判断:变异类型是什么、是否导致Merlin失活、是否符合双等位基因失活模型。
为什么单做NGS还不够
很多患者做了二代测序却没查出异常,并不等于一定没有NF2问题。原因很简单:不同技术擅长识别的变异类型不同。
| 检测方法 | 更擅长发现什么 | 常见局限 | 适用场景 |
|---|---|---|---|
| 靶向NGS/Panel | 点突变、小片段插入缺失、部分剪接区改变 | 对整基因缺失、大片段拷贝数变化敏感性有限 | 初筛常用,适合快速寻找常见致病变异 |
| 全基因组测序 | 核苷酸变异、结构变异、部分拷贝数异常综合分析 | 成本和解读门槛更高 | 复杂病例、前次检测阴性但临床高度怀疑时 |
| MLPA | 整基因缺失、外显子级拷贝数变化 | 不能替代点突变检测 | 怀疑大缺失、大重复时非常关键 |
| 肿瘤-外周血配对检测 | 区分胚系和体细胞来源 | 需要同时获取肿瘤和正常样本 | 遗传风险评估、机制确认、临床决策 |
对NF2相关肿瘤来说,NGS+拷贝数分析+MLPA或全基因组测序的组合,往往比单一方法更接近真实答案。尤其是有以下情况时,更要警惕漏检:
- 年轻时就出现双侧前庭神经鞘瘤;
- 家族中多人有听神经瘤或相关肿瘤病史;
- 常规Panel未发现致病变异,但临床表现高度典型;
- 肿瘤免疫组化提示Merlin缺失。
两类NF2失活路径说明什么
临床上最容易被忽视的一点是:不同来源、不同形式的NF2改变,最后都可能走向同一个结局——Merlin缺失。
一类是胚系全基因缺失。这意味着患者先天就少了一份NF2拷贝,后续肿瘤中再发生第二次打击,例如剪接位点突变或移码突变,最终导致双等位基因失活。这是遗传性NF2相关肿瘤非常经典的发病机制。
另一类是体细胞框内缺失。这类改变不像截短突变那样一眼就容易判断致病性,往往需要结合更多证据:结构建模是否提示蛋白不稳定、免疫组化是否显示Merlin阴性、拷贝数分析是否支持另一个等位基因也已失活。如果这些证据能拼起来,就能把原本“不确定”的变异逐渐推向“可能致病”甚至更高证据等级。
影像和病理能提供哪些线索
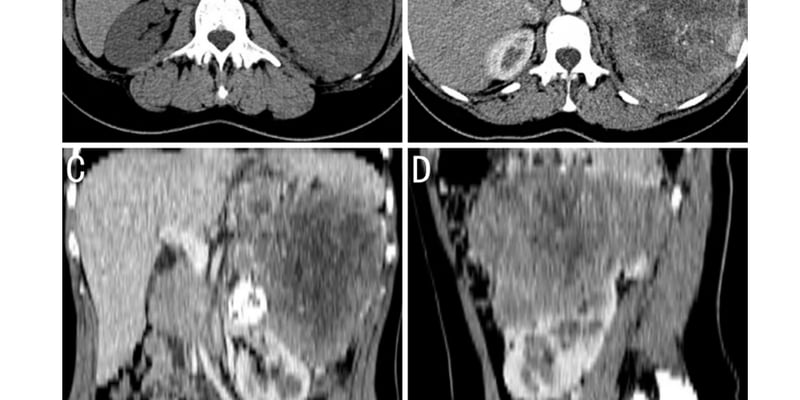
影像学和病理学不能替代基因检测,但常常是决定“要不要做更深入分子检测”的起点。前庭神经鞘瘤常见于桥小脑角和内听道区域,MRI可以帮助判断肿瘤大小、囊变、与周围结构关系以及生长速度。对于颈静脉孔等罕见部位神经鞘瘤,若影像提示边界清晰、伴囊性改变,也需要结合病理进一步确认。
病理上,神经鞘瘤常见Antoni A区、Antoni B区和Verocay小体。如果再加上Merlin免疫组化阴性,就更支持NF2功能缺失这一方向,提示有必要做更完整的分子检测。

NF2相关神经鞘瘤病患者的影像学与组织病理学特征,包括前庭神经鞘瘤和颈静脉孔神经鞘瘤表现。
胚系全基因缺失为何容易漏检
NF2全基因缺失并不常见,但临床意义很大。已知这类改变约占NF2胚系改变的2%—5%。问题在于,很多以外显子为主的常规NGS策略并不擅长识别“整个基因没了”这种拷贝数事件,尤其在没有专门CNV算法或验证手段时,更容易错过。
这就是为什么一部分患者在“基因检测阴性”后,仍然临床上非常像NF2相关神经鞘瘤病。遇到这种矛盾结果,下一步常常不是草率排除遗传性,而是补做MLPA、全基因组测序,或采用对拷贝数更敏感的方案。
一旦证实是胚系全基因缺失,临床价值至少体现在三方面:
- 明确家族风险:需要评估一级亲属是否携带同样改变。
- 优化随访策略:遗传性患者往往需要更系统的长期影像监测。
- 帮助生育与遗传咨询:对有生育计划的家庭尤其重要。

胚系NF2全基因缺失及肿瘤中第二次打击导致双等位基因失活的分子检测示意。
体细胞框内缺失怎么判断致病性
短片段框内缺失是NF2变异里相对棘手的一类。它不像无义突变、移码突变那样天然符合“蛋白提前截断”的直觉,因此经常落入“临床意义未明”区域。真正的判断,不能只看一个检测位点,而要看整套证据链。
当一个框内缺失同时满足以下几点时,致病可能性会明显升高:
- 发生在已知关键结构域或功能热点区域;
- 结构建模提示蛋白明显去稳定;
- 肿瘤组织Merlin免疫组化表达缺失;
- 存在拷贝中性杂合性缺失或其他证据支持双等位基因失活;
- 在人群数据库中罕见或未见报道;
- 与肿瘤表型高度一致。
这类综合判读非常考验分子病理和遗传解读能力,也解释了为什么同一份基因报告,在不同团队手里,结论深度可能差别很大。

体细胞NF2框内缺失的基因组特征及其对Merlin蛋白结构稳定性的潜在影响。
Merlin缺失后会激活哪些通路
Merlin缺失不是一个“静态结果”,它会带来下游信号通路重编程。现有证据提示,Merlin功能丢失后可影响mTOR、FAK及YAP/TAZ等信号网络,这也是为什么NF2缺陷肿瘤一直是靶向治疗研究的重要方向。
对患者来说,这意味着两件事:
- 第一,分子检测不是只为“确诊”,也在为后续临床试验筛选和治疗方向做准备。
- 第二,哪怕现阶段标准治疗仍以手术、放疗和随访为主,明确Merlin缺失也可能影响后续药物可选项。
NF2相关肿瘤有哪些治疗方向
目前,NF2相关神经鞘瘤的治疗仍以手术、放射外科/放疗、影像随访为核心。是否手术,主要看肿瘤位置、体积、生长速度、听力影响、脑干压迫风险以及既往治疗史。
在药物治疗方面,Merlin缺陷相关通路已成为研究重点。已有临床研究探索mTOR抑制剂在进展性前庭神经鞘瘤中的作用,包括西罗莫司和依维莫司(飞尼妥, Everolimus)这一写法是不允许的,因此这里应仅规范呈现为依维莫司(飞尼妥, Everolimus)。现有证据提示,这类药物可能对减缓肿瘤生长速度和延缓听力下降带来一定帮助,但总体仍属于有限获益,远不能替代局部治疗,也并非所有患者都适合。
另外,FAK和YAP/TAZ相关方向也具有研究潜力,但是否能真正转化为成熟临床方案,还要看后续试验结果。
| 治疗方向 | 当前角色 | 更适合哪些情况 | 患者最关心的问题 |
|---|---|---|---|
| 手术切除 | 局部控制核心手段 | 肿瘤增大明显、压迫症状、需要病理确诊 | 听力保留率、面神经功能、复发风险 |
| 伽马刀等放射外科 | 重要局部治疗方式 | 小到中等体积病灶、部分术后残留或复发 | 长期控制率、听力变化、放射后水肿 |
| mTOR抑制剂 | 探索性通路治疗方向 | 进展性、复发性、难切除或需临床试验评估者 | 疗效强不强、副作用大不大、能否长期用 |
| 临床试验 | 获取前沿方案的重要途径 | 标准治疗后仍进展,或存在明确分子靶点者 | 入组条件、药物可及性、跨境获取信息 |
依维莫司能用吗?副作用怎么管
如果医生评估后考虑mTOR抑制剂,患者最常问的是:依维莫司到底值不值得用。答案通常取决于肿瘤进展速度、既往手术或放疗情况、当前症状、听力变化以及是否有更合适的局部治疗机会。
依维莫司(飞尼妥, Everolimus)属于mTOR抑制剂。这类药物不是“立刻缩瘤”的典型代表,更多价值在于部分患者中对疾病进展的调控。是否使用,必须由有经验的神经肿瘤或遗传肿瘤团队综合判断。
常见不良反应管理要点包括:
- 口腔溃疡:保持口腔清洁,避免辛辣、过烫食物,必要时使用医生建议的局部护理方案。
- 皮疹:温和清洁、减少摩擦和暴晒,若加重需尽快反馈医生。
- 感染风险升高:出现发热、咳嗽、口腔白斑等情况不要硬扛。
- 血糖、血脂异常:用药期间通常需要定期抽血监测。
- 乏力和食欲下降:少量多餐,保证蛋白质摄入,体重连续下降要及时处理。
任何口服靶向药都不建议自行加减量。尤其是跨地区复诊不方便的患者,更需要在启动治疗前把监测计划、复查频率和不良反应处理路径提前说清楚。
患者最该做的随访清单
NF2相关神经鞘瘤病往往不是一次治疗就结束的疾病,长期管理比“单次手术是否成功”更重要。
- 保存完整病理和影像资料:包括手术记录、病理切片、免疫组化、MRI原始报告。
- 尽量做肿瘤-外周血配对检测:帮助区分胚系与体细胞变异。
- 检测阴性但高度怀疑时补做CNV分析或MLPA:不要因为一次阴性就草率否定。
- 有家族史者尽早遗传咨询:尤其是双侧前庭神经鞘瘤、起病年龄早者。
- 制定长期MRI复查计划:根据肿瘤位置、大小、生长速度和治疗史个体化安排。
- 关注听力和神经功能:听力下降、眩晕、吞咽困难、声音嘶哑等都可能提示病情变化。
报告看不懂时最怕错过什么
很多患者真正的困境,不是拿不到报告,而是拿到报告后不知道哪一句最关键。对于NF2相关神经鞘瘤病,最值得重点追问的是:
- 变异是胚系还是体细胞?
- 有没有做拷贝数分析?是否排除整基因缺失?
- 是否有证据支持双等位基因失活?
- Merlin免疫组化结果如何?
- 变异分类依据是什么?是否结合了结构和功能证据?
- 这份结果会不会影响家属筛查、随访频率和临床试验资格?
这些问题决定了报告是“只看见一个变异”,还是“真正进入临床决策”。
药物可及性和就医决策怎么走
对不少患者家庭来说,另一个现实问题是:即使知道了Merlin缺失和潜在通路,下一步去哪看、怎么评估方案、药物能否获得,往往同样困难。尤其是复发、残留、难切除、需要评估前沿治疗或临床试验机会的患者,信息差本身就是治疗障碍。
这时候,最有价值的不是碎片化搜索,而是把病理、影像、基因检测、既往治疗史放在一起系统解读,明确患者究竟属于:
- 适合继续随访;
- 优先考虑再次手术或放疗;
- 需要寻找靶向药或临床试验机会;
- 需要同步开展家族遗传咨询。
MedFind长期关注全球抗癌资讯、诊疗指南和前沿药物信息,尤其适合那些面对复杂分子报告、跨境药物信息、临床试验线索时无从下手的家庭。如果已经拿到NF2相关检测结果,或正在评估像依维莫司这样的通路治疗方案,先把资料系统梳理清楚,再决定是否需要进一步辅助问诊或药物可及性支持,往往能少走很多弯路。对部分存在明确治疗需求、且经医生评估适合的患者,跨境直邮与方案解读服务也能帮助更快打通“知道方案”到“真正用上方案”的最后一段路。
【参考文献】
Nakamura, K., Tamura, R., Sogano, J. et al. Diverse NF2 alterations in cranial schwannomas: a two-case series of germline whole-gene deletion and somatic in-frame deletion. Brain Tumor Pathol (2026). https://doi.org/10.1007/s10014-026-00532-8