胃癌出现腹膜转移、腹水越来越多,甚至反复梗阻时还能怎么办?本文围绕“胃癌腹膜转移”这一最棘手的晚期类型,讲清NIPS腹腔内常温灌注化疗是什么、为什么要和全身治疗联合、它可能改善哪些症状与结局、哪些人更可能获益、治疗前后需要做哪些检查与居家护理,以及当药物在国内可及性有限时如何更快地获得规范用药与第二诊疗意见。
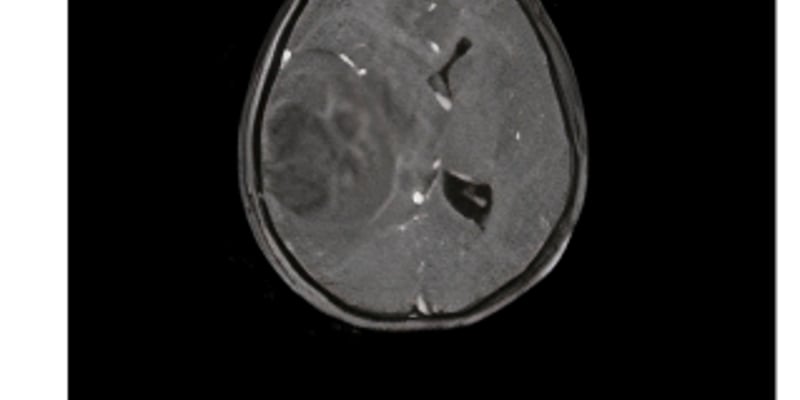
一、为什么胃癌腹膜转移特别难治?
腹膜转移是胃癌晚期常见且影响生活质量最明显的类型之一。临床中,大约17%–27%的胃癌患者会在术前或术中发现腹膜转移。它带来的问题往往不是“一个转移灶”,而是一连串连锁反应:
- 大量癌性腹水:腹胀、食欲差、呼吸费力、行动困难,反复穿刺引流又容易蛋白丢失与感染。
- 消化道梗阻:吃不下、呕吐、无法维持营养,治疗难以持续。
- 输尿管梗阻(肾盂积水):腰痛、肾功能受损,影响化疗与用药选择。
- 胆管梗阻(阻塞性黄疸):皮肤黄、瘙痒、胆红素升高,很多药物需要减量甚至暂停。
更核心的难点在于“腹膜屏障”。你可以把腹膜想成一层“半透明的保护膜”,全身静脉化疗药物要从血液到腹腔表面和游离癌细胞,往往会被稀释、被阻隔、到达浓度不够,于是控制腹水和腹膜病灶就更难。也正因为如此,东西方多部胃癌诊疗指南都将胃癌腹膜转移视为晚期胃癌的“特殊类型”,治疗策略往往要区别于肝转移、肺转移等其他部位。
从已给出的临床观察来看,胃癌腹膜转移患者总体预后较差:中位生存时间约7–10个月,2年生存率不足10%,也是晚期胃癌患者死亡的重要原因之一。这些数字并不是要吓人,而是用来说明:仅靠“传统全身治疗”很多时候不够,我们需要更有针对性的腹腔局部策略。
二、NIPS到底是什么?
NIPS常被描述为腹腔内常温灌注化疗联合全身治疗的一种技术与策略组合。通俗地说:在静脉化疗(全身治疗)之外,额外把化疗药物“直接送进腹腔”,让药物在腹腔内与腹膜表面更充分接触,以期更有效地控制腹膜病灶与癌性腹水。
很多患者会把它和“热灌注(HIPEC)”混在一起。这里要点是:NIPS强调常温与腹腔局部给药,其核心目的仍是“提高腹腔局部有效药物暴露”。是否采用加温、是否在手术中进行、具体给药方案如何实施,会因中心经验与患者情况而异,必须由专科团队评估。
NIPS为什么可能有用
如果把腹膜转移想成“地毯上撒满了细沙”,全身化疗好比“从窗外往屋里喷雾”,能进来但浓度有限;而腹腔内给药更像“直接在屋里均匀喷洒”,更容易覆盖地毯表面。对腹膜表面微小病灶、游离癌细胞、腹水环境中的肿瘤细胞而言,腹腔内给药在理论上更有机会形成更高的局部药物浓度,从而改善腹水和腹膜控制。
此外,输入文章提到:临床团队观察到NIPS联合全身系统治疗可能降低耗竭CD8+ T细胞水平。你可以把CD8+ T细胞理解为免疫系统里的“前线战士”;“耗竭”意味着它们长期作战后变得疲惫、杀伤力下降。如果治疗能在一定程度上改善这种“疲惫状态”,理论上可能让机体的抗肿瘤免疫更有力量。不过需要强调:这是一个值得关注的免疫学方向,但在不同患者中效果差异可能很大,仍需要更多高质量研究来进一步验证与量化。

NIPS用于胃癌腹膜转移的治疗思路:腹腔局部+全身联合
三、NIPS联合全身治疗:患者最关心的“能带来什么改变”
对腹膜转移患者来说,“有效”往往不只等于影像缩小,还包括能否把生活从“每天被腹胀与梗阻绑住”拉回到“能吃、能走、能继续治疗”。从输入文章给出的方向,NIPS联合全身治疗的潜在价值集中在三点:
- 改善恶性腹水:腹水减少意味着腹胀缓解、食量改善、呼吸更顺畅,也能减少反复穿刺带来的风险。
- 突破腹膜屏障:增加腹腔局部治疗强度,有机会提高腹膜病灶控制。
- 争取“转化治疗”机会:当腹膜负荷下降、全身状况改善时,部分患者可能从“只能姑息”走向“有机会进行更积极的综合治疗”。

疗效评估常同时关注腹水、症状与整体治疗耐受性
需要把话说得更稳一点:输入文章强调“可能达到转化治疗效果、使患者获得长期生存”。这代表临床上确实见到希望,但并不意味着所有患者都能达到同样结局。腹膜转移的异质性很强,治疗能否带来“长期生存”,常取决于腹膜病灶范围、全身转移情况、体能状态、营养状况、肿瘤生物学特征、以及治疗是否规范持续等多因素。
四、哪些患者更可能适合考虑NIPS?
是否适合做NIPS,核心是“安全”和“能否获益”。一般需要专科团队从以下维度综合评估(不同医院具体标准可能不同):
- 确认为胃癌腹膜转移:影像学、腹水细胞学、腹腔镜探查等证据链越完整越好。
- 主要问题在腹膜与腹水:腹胀、腹水、腹膜播散负荷是主要矛盾;如果全身多器官转移负荷极重,局部策略获益可能有限。
- 体能状态允许反复治疗:体力评分、营养、白蛋白水平、血象储备等影响能否完成疗程。
- 无严重感染或不可控出血风险:腹腔操作与化疗会增加感染与出血相关风险。
- 肾功能、肝功能可承受:尤其有肾盂积水或黄疸者,需先处理梗阻(如置管引流)再谈系统治疗强度。

开始局部-全身联合前,先把“梗阻、感染、营养”三件事评估清楚
五、治疗前你需要和医生逐条确认的关键问题
为了避免“听起来很先进,但我到底该不该做”的信息差,我们建议把以下问题写在纸上,面诊时逐条对齐:
- 我的腹膜转移范围大概到什么程度?是否有腹腔镜评估或其他分级?腹水量如何?是否有肠梗阻迹象?
- 这套NIPS方案具体怎么做?是否需要置管?灌注频率与疗程安排?是否需要住院?每次观察指标是什么?
- 会联合什么全身治疗?化疗为主还是还会合并免疫/靶向(是否适合取决于HER2、PD-L1、MSI等检测结果以及指南推荐)。
- 疗效怎么评估?仅看CT不够,还要看腹水变化、症状、营养、体能、肿瘤标志物趋势等。
- 最常见风险是什么?我如何提前预防?例如感染、腹痛、发热、骨髓抑制、电解质紊乱、肾功能波动等。

把问题清单化,能显著减少决策焦虑与遗漏
六、可能的不良反应与居家管理:把“可控”做到前面
任何强化治疗都伴随副作用。输入文章未逐条展开不良反应细节,但从腹腔化疗与全身治疗的一般规律出发,患者家庭最需要提前准备的是“识别风险信号”和“可操作的处理步骤”。以下为通用科普建议,具体以主治团队告知为准:
1)发热、腹痛、腹膜刺激症状
- 可能原因:灌注刺激、局部炎症反应、导管相关感染等。
- 居家怎么做:每日测体温;记录腹痛位置与程度;保持穿刺/置管部位清洁干燥。
- 何时立刻就医:体温≥38.3℃持续或反复、腹痛进行性加重、出现寒战或意识改变、穿刺口红肿渗液明显。
2)恶心、呕吐、食欲差与营养下降
- 核心目标:不追求“吃很多”,追求“吃得下、吃得稳”。
- 饮食策略:少量多餐;优先高蛋白(蛋、鱼、瘦肉、豆制品、乳制品按耐受选择);腹水明显时减少高盐加工食品;若有梗阻风险,遵医嘱选择流质/半流质或肠内营养制剂。
- 实用技巧:把一天目标拆分为6–8次进食;每次吃到“七分饱不胀”为宜;必要时请营养科制定方案。
3)骨髓抑制(白细胞/血小板下降)
- 你需要盯紧什么:发热、咽痛、口腔溃疡、皮下出血点、牙龈出血、黑便等。
- 居家要点:勤洗手、避免人群密集处;刷牙用软毛牙刷;避免生冷海鲜与不洁饮食;按医嘱复查血常规。
- 何时急诊:发热伴乏力明显、出血不止、头晕心悸、黑便或呕血。
4)腹水反复与电解质/蛋白丢失
- 为什么会虚:腹水和反复引流会带走蛋白与电解质,人会更乏力、腿肿、血压低。
- 居家记录:每日体重、腹围(同一时间同一位置)、尿量;一周至少1次把记录带给医生。
- 别自己乱补:白蛋白、利尿剂、补钾补钠都应在医生指导下进行,尤其合并肾功能问题者。

体重、腹围、尿量是腹水管理的三个“家庭指标”
七、把治疗做“稳”:复查节奏与疗效判断别只盯一张片子
腹膜转移的变化不总能在短期CT上“清清楚楚”。我们建议与医生共同建立一套更贴近生活的评估框架:
| 评估维度 | 你能观察到什么 | 提示意义 |
|---|---|---|
| 腹水/腹围 | 腹围下降、穿刺间隔变长 | 腹腔控制可能改善 |
| 进食与体力 | 能吃下蛋白质、能走动、睡眠改善 | 综合耐受性提升,有利于完成疗程 |
| 梗阻相关 | 呕吐减少、排气排便恢复 | 肠道功能改善,营养更稳 |
| 实验室指标 | 白蛋白、电解质、肾肝功能、血象 | 决定能否加量/继续治疗 |
| 影像与医生评估 | CT/超声、必要时腹腔镜 | 更客观判断病灶负荷 |

腹膜转移疗效评估更强调“症状+腹水+耐受性”的综合视角
八、药物与治疗的可及性:为什么要提前做“方案与用药”规划?
腹膜转移常需要多学科与多轮治疗组合:局部治疗、静脉系统治疗、针对分子分型的靶向/免疫、以及支持治疗(营养、镇痛、引流、抗感染等)。现实中,很多家庭会遇到三个困境:
- 方案信息差:不同中心做法差异大,患者不知道哪种更适合自己。
- 用药可及性差:部分药物在不同国家/地区上市时间与适应症范围不同,导致等待与错过窗口期。
- 路径碎片化:今天管腹水、明天管梗阻、后天再讨论化疗,缺少一条“连续可执行”的主线。
在MedFind,我们更希望你把精力放在“最值得做的决定”上:第一,尽快明确分期与腹膜负荷;第二,确认是否具备联合治疗的条件;第三,把可能用到的药物与支持治疗提前列清单,减少中途因供药或流程延误导致的中断。

把治疗路径“画出来”,更利于家庭执行与复盘
九、家属最容易忽略的三件事:疼痛、睡眠与情绪
腹膜转移患者常处在“身体不适+不确定性强”的双重压力中。很多家庭只盯指标,忽略了真正影响坚持治疗的基础:
- 疼痛管理:不要硬扛。疼痛会让睡眠崩塌、进食减少、焦虑加重。镇痛应在医生指导下阶梯化使用。
- 睡眠修复:夜间腹胀、反酸、疼痛会干扰睡眠。可尝试抬高床头、分次少量进食、晚间减少产气食物;若失眠持续,向医生寻求药物或心理支持。
- 情绪与沟通:建议家属把“治疗目标”说清楚(例如先把腹水压下去、让他能吃能走),把目标拆成一周可完成的小任务,能显著降低无力感。

照护不是“陪着受苦”,而是把可控因素逐个抓住
十、你可以立刻采取的行动清单
如果你正在面对“胃癌腹膜转移+腹水/梗阻”,建议按优先级做三件事:
- 把病情资料整理成一份“可转诊包”:病理报告、影像(含光盘/云胶片)、腹水细胞学、手术记录、近期血常规与肝肾功能、电解质、用药清单与不良反应记录。
- 与专科团队讨论是否适合NIPS联合全身治疗:明确目标是“控制腹水、改善生活质量”还是“争取转化”。
- 提前规划用药与支持治疗的连续性:包括止吐、止痛、营养支持、置管护理、可能需要的抗肿瘤药物获取路径。

资料齐全=少走弯路,也更容易获得一致的治疗建议
结语:把希望落到“可执行的方案”上
胃癌腹膜转移并不等于“只能等”。真正改变结局的,往往是尽早识别这是一类需要“腹腔局部+全身系统”共同发力的特殊晚期胃癌,并在安全前提下把治疗做得连续、规范、可评估。NIPS联合全身治疗提供了一个值得认真讨论的方向:不仅可能改善腹水与症状,也可能为部分患者争取到更积极的综合治疗窗口。
如果你正卡在“方案看不懂、用药不确定、时间被拖慢”的焦虑里,MedFind可以提供两类直接帮助:其一,协助你梳理病历与检测结果,获得更清晰的辅助问诊与治疗方案解读;其二,当涉及海外已上市或国内一时难以及时获得的抗肿瘤药物时,提供合规路径下的跨境直邮信息支持,尽量减少因等待造成的治疗中断。你只需要记住一句话:把每一步都做“稳”,就更接近你想要的结果。

长期管理的核心:症状控制、营养体能、并发症预防与按期复查
【参考文献】
输入文章给出的数据与结论要点:胃癌患者术前/术中发现腹膜转移约17%–27%;中位生存时间7–10个月;2年生存率不足10%;NIPS联合全身系统治疗可能降低耗竭CD8+ T细胞水平并带来转化治疗潜力。