很多肝癌患者和家属都会困惑:明明肿瘤“抢营养”很凶,可在肿瘤内部经常又是缺氧、缺血、缺营养的“饥荒环境”,为什么癌细胞还能撑得住,甚至对治疗越来越“耐受”?这背后往往不是单一基因的变化,而是一整套“求生应激系统”在工作。
近期一项针对肝细胞癌的研究提示:当肿瘤遭遇“谷氨酰胺不足”这种常见的营养压力时,肝癌细胞会通过上调TRIB3,并招募DDX5去“解开”一种会卡住复制与转录的特殊DNA结构——G-四链体DNA(G4-DNA),从而维持关键DNA修复通路的正常转录,避免DNA损伤越积越多,最终帮助肿瘤在饥饿中存活。更重要的是,这条TRIB3-DDX5-G4轴可能成为HCC及其他TRIB3高表达肿瘤的潜在治疗靶点。
下面我们用尽量通俗的方式,讲清楚这项发现意味着什么、和患者最关心的治疗有什么关系、以及在就医沟通中可以抓住哪些重点。
先把概念讲明白:什么是HCC?
肝癌主要分为两大类型:肝细胞癌(HCC)和肝内胆管癌(ICC)。其中HCC占全球肝癌病例的80%以上。早期肝癌可能有机会通过手术切除、射频消融、经动脉化疗栓塞(TACE)和肝移植等手段获得较好控制;但现实中不少患者确诊已偏晚期,系统治疗(靶向、免疫、联合治疗)成为主线。
肿瘤之所以难缠,一个核心原因是它非常“会适应环境”。肿瘤微环境里常常营养不足、缺氧、代谢废物堆积,癌细胞为了活下去,会启动代谢重编程,换一套“吃饭方式”和“修房子方式”。这项研究聚焦的,正是其中一种常见压力:谷氨酰胺受限。
为什么谷氨酰胺这么关键?
谷氨酰胺(Gln)是血液循环里最丰富的氨基酸之一,对很多肿瘤细胞来说几乎是“必需品”。有些肿瘤存在所谓“谷氨酰胺成瘾”:它们会增加谷氨酰胺相关酶活性、调整吸收与利用方式,并依赖谷氨酰胺衍生的代谢物来维持生存。
用一个比喻帮助理解:如果把细胞看成一座城市,谷氨酰胺既像“燃料”(供能),又像“建材”(合成核苷酸、蛋白质等),还像“消防系统的灭火剂原料”(参与抗氧化体系)。研究中提到的关键点包括:
- 谷氨酰胺为TCA循环提供碳源,帮助获取能量和核苷酸前体;同时提供氮源,支持生物合成与基因组维护。
- 谷氨酰胺还是合成谷胱甘肽(GSH)的重要前体,并促进NADPH生成以维持氧化还原稳态。
当谷氨酰胺不足时,细胞会面临双重打击:一方面dNTP供应受损(复制“原料”不足),另一方面氧化还原失控导致氧化性DNA损伤,进而引发复制应激、细胞周期停滞。理论上这是肿瘤的脆弱点,所以过去很多策略尝试用谷氨酰胺摄取抑制剂或代谢抑制剂“饿死肿瘤”。但现实并不理想:不少临床试验疗效有限,提示肿瘤存在强大的适应性耐受机制。
这项研究的核心发现:TRIB3让肝癌“饿而不乱”
研究提出:在谷氨酰胺受限时,HCC细胞会以c-Jun依赖方式上调TRIB3。TRIB3属于Tribbles伪激酶家族成员之一,更像“分子支架”,通过蛋白-蛋白相互作用把关键因子组织起来,帮助细胞在压力下做出“活下去”的选择。
在这项工作中,TRIB3不只是被动升高,而是进入细胞核发挥关键作用:它能够结合全基因组范围的G-四链体DNA(G4-DNA)结构,并招募解旋酶DDX5形成复合物,共同解开G4结构,保证转录顺畅,同时维持DNA损伤修复系统的转录激活,从而提高DNA修复的“忠实度”,避免复制灾难。
G4-DNA到底是什么?为什么“解不开”会出事?
G4-DNA可以理解为DNA在某些富含鸟嘌呤(G)的区域,会折叠成一种更“立体、更紧”的四链体结构。它并不一定是坏东西:在生理状态下,G4结构广泛存在,也参与基因表达调控。
问题在于:当压力状态下G4结构变得异常稳定或堆积,它会像“路障”一样卡在DNA复制与转录的关键路段,导致:
- 复制叉受阻,复制应激加重;
- 转录受阻,关键基因表达下降;
- 重要蛋白-DNA相互作用被干扰;
- DNA损伤增加,修复不及时则可能触发细胞死亡。
因此,肿瘤细胞如果能在饥饿压力下把这些“路障”清掉,就更容易活下来。TRIB3在这里做的事,可以类比成“应急指挥中心”:发现道路拥堵后,迅速调来DDX5这台“破障车”,把G4路障清开,让维修队(DNA修复系统)能继续工作。
关键证据:敲掉TRIB3或DDX5会发生什么?
研究显示:在HCC细胞中敲除TRIB3或DDX5,会导致G4-DNA过度蓄积,并伴随DNA损伤修复(DDR)通路下调,DNA损伤进一步加剧。
研究还用同源重组(HR)通路基因做了例证:TRIB3-DDX5复合物可以阻止BRCA1和RAD51AP1启动子区域的G4-DNA蓄积;如果G4堆在那里,会抑制这些基因的转录。对于细胞来说,这相当于“修复DNA的大工程队被断了粮”,损伤越积越多,最终更容易走向凋亡。
动物与临床提示:TRIB3高表达与不良预后相关
在体内实验中,沉默TRIB3可抑制HCC异种移植瘤的生长;当小鼠饲喂谷氨酰胺缺乏饮食时,TRIB3沉默会显著增加瘤内DNA损伤与细胞凋亡。
临床层面,TRIB3在HCC中高表达,并与患者不良预后相关。综合这些证据,研究提出TRIB3-DDX5-G4轴可作为HCC及其他TRIB3高表达恶性肿瘤的潜在治疗靶点。

研究示意图:谷氨酰胺受限诱发应激,TRIB3介入并维持DNA修复与肿瘤存活(图源为原文配图)
与现有治疗的关系:为什么这可能影响“耐药”?
原文提到,HCC细胞模型中的研究提示TRIB3参与索拉非尼(多吉美, Sorafenib)耐药,且有研究认为这种耐药与ROS介导的内质网应激及未折叠蛋白反应(UPR)激活相关。需要强调的是:这并不等于“TRIB3一定导致所有患者索拉非尼无效”,而是提示TRIB3可能位于肿瘤应激网络的关键节点——当治疗或微环境压力增加时,肿瘤可能更依赖这类“自救机制”。
从患者角度,这个信息带来两点现实意义:
- 第一,肿瘤的耐药常常不是“突然变坏”,而是“越饿越会找路”。理解这些通路,有助于未来开发更精准的联合策略。
- 第二,当科学界在寻找“代谢抑制剂+其他靶点”的组合时,TRIB3-DDX5-G4轴提供了一个可能的切入点:在谷氨酰胺受限的压力环境里,如果同时掐断肿瘤清障与修复能力,肿瘤可能更难存活。
患者最关心的三个问题:现在能用上吗?怎么检查?要不要改变饮食?
1)这是不是已经有成熟药物可以用?
这项研究属于机制与靶点层面的前沿探索,提出了“可作为治疗靶点”的方向,但并不等于目前临床上已经有成熟、获批的TRIB3或DDX5靶向药可以常规用于肝癌治疗。对患者而言,最重要的是把它理解为“未来可能出现的新组合、新药物研发方向”。
如果您正在接受系统治疗(靶向、免疫或联合),请不要因为看到“谷氨酰胺剥夺”“缺乏饮食”等字样就自行调整用药或极端节食。任何治疗调整都应由主管肿瘤科医生评估。
2)临床上能检测TRIB3高不高吗?
研究提到TRIB3在HCC中高表达且与预后相关,但在日常临床中,TRIB3并不是所有医院都会常规检测的项目。理论上可通过肿瘤组织的免疫组化或分子检测进行评估,但是否有必要做、做了是否改变治疗决策,需要结合:
- 您目前的分期与治疗阶段;
- 是否在考虑临床试验;
- 是否有足够的肿瘤组织样本;
- 检测结果是否能对应到可用药物或可入组的研究。
如果您想更进一步把“前沿靶点”转化为“可行动的方案”,建议把病理报告、基因检测结果、用药史与影像资料整理齐全,与医生讨论是否存在相关临床研究机会。
3)能不能通过饮食“控谷氨酰胺”来抗癌?
研究在小鼠层面做了谷氨酰胺缺乏饮食的条件探索,但这不等同于建议肝癌患者在现实生活中采用极端“去谷氨酰胺”饮食。原因很现实:
- 谷氨酰胺是人体重要氨基酸,长期或极端限制可能带来肌肉流失、免疫下降、营养不良;
- 肝癌患者常合并肝硬化、食欲差、蛋白摄入不足,盲目限制更易导致体力下降与治疗耐受变差;
- 肿瘤的代谢适应是网络式的,单靠饮食很难“精准饿死肿瘤”,反而可能先“饿坏自己”。
更可取的居家营养策略是:在医生或营养师指导下,保证足够热量与优质蛋白,尽量维持体重与肌肉量,让您更有机会完成系统治疗并减少并发症风险。
居家管理:在“代谢压力”和“治疗压力”下怎么更稳?
肝癌治疗常常是长期战役,除了用药,生活管理能显著影响耐受性与生活质量。结合“应激—修复—存活”这一思路,给出更落地的建议:
1)营养与体重:先保住“体力资本”
- 优先目标:稳定体重、维持肌肉量。短期体重快速下降往往意味着肌肉丢失,会降低治疗耐受。
- 蛋白选择:在肝功能允许的前提下,优先鱼、蛋、奶、豆制品、瘦肉等;若合并肝性脑病风险或血氨偏高,应遵医嘱调整蛋白总量与类型。
- 少量多餐:食欲差时,比起硬撑“三顿”,更推荐“5-6次少量进食”。
- 警惕误区:不要自行采用极端断食、生酮或“去某种氨基酸”的做法来对抗肿瘤。
2)疲劳、睡眠与压力:降低“应激叠加”
研究里TRIB3被描述为多种应激通路可诱导的分子开关。现实中,长期睡眠不足、强烈焦虑、疼痛控制不佳,也会让机体处在应激状态,影响恢复与耐受。可尝试:
- 固定作息,把“能睡着”放在优先级;
- 把每天目标拆小,例如“散步10分钟+拉伸5分钟”;
- 用可执行的方式缓解焦虑:记录每日症状、体温、饮食与大便情况,把不确定性变成可描述的信息,复诊沟通更高效。
3)复诊沟通清单:把问题问到点子上
当您看到“TRIB3、DDX5、G4-DNA、DNA修复”这类前沿词汇时,建议用更临床友好的方式与医生沟通:
- “我目前的治疗方案(靶向/免疫/局部治疗)是否有明确的下一步预案?”
- “如果出现耐药或进展,我是否适合临床试验?有没有代谢相关或DNA修复相关方向的研究可考虑?”
- “我是否需要补做基因检测/复检影像/重新取样?”
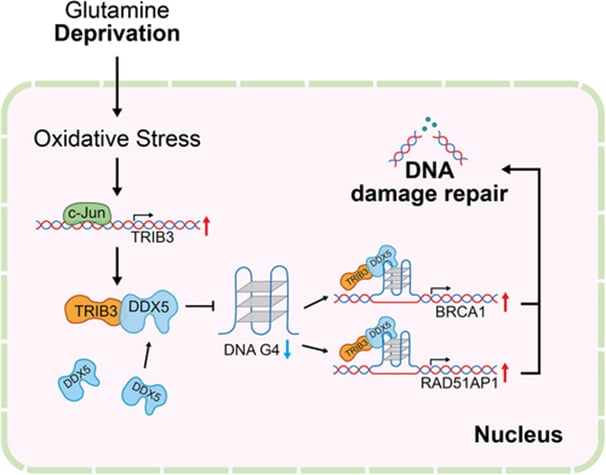
机制模式图:TRIB3与DDX5协同解开G4-DNA,支持DNA修复相关基因转录(图源为原文配图)
药物可及性与下一步:患者可以怎么用“前沿信息”帮助自己?
截至目前,针对TRIB3-DDX5-G4轴的治疗策略仍以研究探索为主;但对患者而言,“现在能做的”并不是等待,而是把治疗路径走得更清晰:
- 如果您在用靶向药:请与医生一起评估疗效与耐受性,按时复查;出现不良反应及时处理,避免因为副作用而被迫中断有效治疗。
- 如果您在寻找更前沿的选择:建议优先整理完整病历资料,关注权威机构的临床试验信息,并评估自身是否具备入组条件。
- 不要自行尝试“代谢饿疗”:研究揭示的是肿瘤在饥饿中的适应机制,而不是患者通过饥饿就能战胜肿瘤的处方。
我们能为你做什么:把“论文靶点”变成“可执行方案”
很多家属读到这类研究,最难的是从“我懂了一些机制”走到“我接下来该怎么办”。在MedFind,我们更关注把前沿信息转化成可落地的行动:
- AI辅助问诊与方案解读:帮助你把病理、影像、基因检测、既往用药史梳理成医生能快速抓重点的摘要,减少沟通成本;同时解释“为什么医生这样选方案”“下一步有哪些路径”。
- 跨境直邮:如果医生评估后需要用到国内暂未充分可及的药物或规格,我们可以协助了解合法合规的获取路径与用药信息,尽量缩短等待时间与信息差。
如果你愿意,现在就可以把“确诊类型与分期、是否合并肝硬化、当前用药与最近一次影像结果、是否做过基因检测”这四项信息整理出来,我们会更高效地帮你把问题问到关键点,找到更适合的下一步。
参考文献
Advanced Science. Glutamine Deprivation Triggers Tribbles Homolog 3 Dependent G-Quadruplex Resolution to Maintain DNA Repair and Tumor Survival. DOI: 10.1002/advs.202520798