在抗癌的战场上,我们一直在寻找能够精准降伏癌细胞的“终极武器”。许多患者在经历了长期的化疗、放疗后,往往会面临耐药和转移的困境。此时,科学家们发现了一种全新的细胞死亡方式——铜死亡。不同于以往我们熟知的凋亡或坏死,这种方式通过精准诱导癌细胞内部的金属失衡,让肿瘤细胞从内部“崩溃”。近期,来自新加坡南洋理工大学的研究团队在国际顶尖学术期刊《ACS Nano》上发表了一项重磅研究,他们开发了一种名为CaP/Cu-F的多功能纳米平台。这不仅仅是一种送药工具,它更像是一个“特种作战分队”,能够同时发动铜过载、钙过载和抗血管生成的三重攻击,为中晚期癌症患者带来了新的曙光。
深度科普:什么是“铜死亡”与“钙过载”?
要理解这项新技术,我们首先要明白癌细胞是如何被“撑死”的。铜是人体必需的微量元素,但癌细胞对铜有着异乎寻常的渴求。铜死亡(Cuproptosis)是2022年才被正式命名的一种细胞死亡机制。简单来说,当细胞内的铜离子浓度超过阈值时,它们会直接干扰线粒体的代谢过程,导致蛋白质发生异常聚集,最终让癌细胞像“电路过载”一样烧毁。然而,狡猾的癌细胞通常会利用泵蛋白(如ATP7A/ATP7B)把多余的铜排出去。这项新技术的核心,就是封锁这些出口,让铜在癌细胞内蓄积。
与此同时,该研究还引入了钙过载的概念。钙离子是细胞信号传导的指挥官,但如果大量的钙瞬间涌入,线粒体就会功能衰竭,ATP(细胞的能量货币)耗尽。当“铜死亡”与“钙过载”双管齐下,癌细胞的能量供应被切断,自我防御系统崩溃,自救无望。
技术解析:CaP/Cu-F纳米平台的“三步走”战略
研究团队构建的这个纳米平台,其结构设计精妙。它以磷酸钙为载体,内部包裹了呋喹替尼(Fruquintinib)和谷胱甘肽抑制剂(BSO)。
第一步:解除武装,制造氧化压力
癌细胞内有一种天然的抗氧化剂叫谷胱甘肽(GSH),它像是一层“防弹衣”,能抵消治疗带来的损伤。纳米平台释放的BSO和铜离子会双重消耗GSH,撕开癌细胞的防线,并诱发强烈的氧化应激反应,制造出大量“生锈”的自由基,破坏细胞结构。
第二步:精准爆破,诱发铜/钙双重死亡
在肿瘤微环境的酸性条件下,纳米颗粒迅速降解,释放出大量的钙离子和铜离子。钙离子不仅直接导致线粒体损坏,还间接下调了排水泵蛋白ATP7A的表达。这意味着癌细胞不仅在“中毒”,而且连排水管也被堵死了,铜离子迅速积累,触发铜死亡。
第三步:切断粮草,重塑免疫环境
这也是该方案的精妙之处——加入了呋喹替尼。作为一种强效的血管内皮生长因子受体(VEGFR)抑制剂,其主要作用是让畸形的肿瘤血管“正常化”或直接萎缩。这不仅切断了肿瘤的营养供应(断粮),还让免疫细胞(如CD8+ T细胞)更容易进入肿瘤内部实施杀伤。

图中清晰地展示了纳米平台如何进入细胞,释放药物并最终导致癌细胞瓦解的过程。
实验数据:80%抑制率与生存率的飞跃
在针对4T1原位乳腺癌(一种极具侵袭性的机体模型)的实验中,CaP/Cu-F展现出了令人振奋的数据:
| 评估指标 | 常规对照组 | CaP/Cu-F 纳米平台组 |
|---|---|---|
| 肿瘤生长抑制率 | 较低/不明显 | 80% 以上 |
| 42天生存率 | 大部分死亡 | 100% 存活 |
| 肺部转移情况 | 可见大量转移灶 | 几乎完全消失 |
| 免疫细胞浸润 | 极少 | 显著增加(CD8+/CD4+ T细胞) |
数据显示,该方案不仅能有效缩小原发肿瘤,更能通过调节免疫环境,防止最致命的“癌细胞转移”。这对于乳腺癌、肺癌等容易发生远处转移的癌种具有极高的临床参考价值。
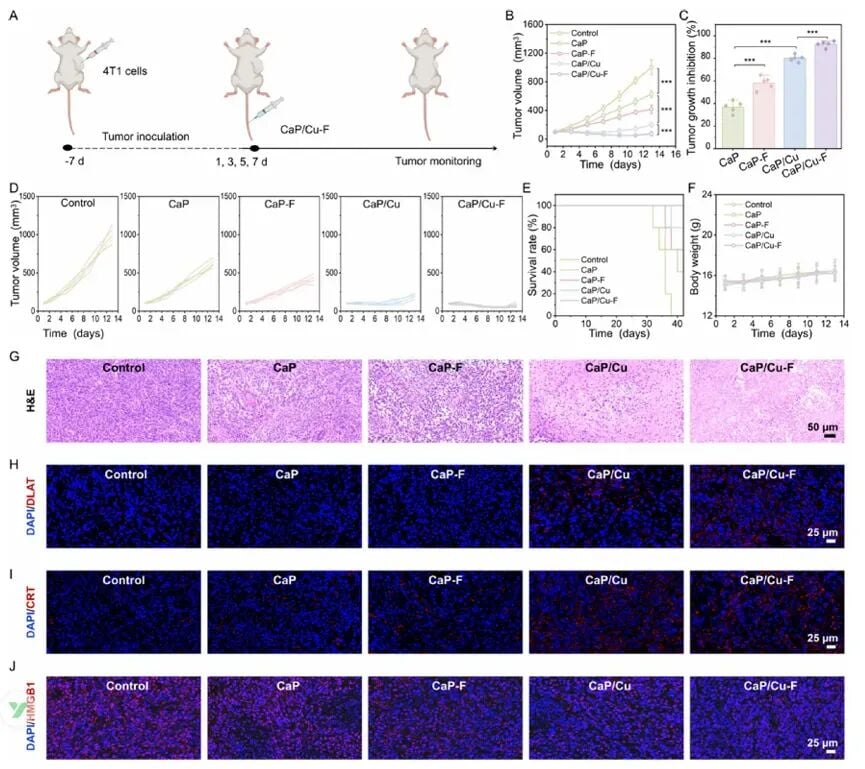
通过H&E染色可以看到,接受治疗后的肿瘤组织出现了大面积的坏死,而健康器官并未受到毒性损害,证明了该疗法的优异安全性。
前沿药物:呋喹替尼的临床意义与副作用管理
本研究中使用的核心药物之一呋喹替尼,已经在国内获批上市。虽然纳米平台技术目前仍处于实验室阶段,但呋喹替尼在临床上的应用已经非常成熟。
临床现状
呋喹替尼主要用于既往接受过氟嘧啶类、奥沙利铂和伊立替康治疗的转移性结直肠癌患者。在本次研究中,科学家们将其跨界应用到乳腺癌及纳米协同方案中,探索了其在“血管正常化”方面的新潜力。
居家管理干货
对于正在使用或即将使用呋喹替尼的患者,以下副作用及应对措施值得收藏:
- 手足皮肤反应:表现为手掌和足底的红肿、脱皮或疼痛。建议减少摩擦,每天温水泡脚后涂抹含尿素的护肤霜,穿着松软的棉袜。
- 高血压:这是抗血管药物的常见副作用。患者需每天早晚监测血压,若收缩压超过140mmHg,应及时联系医生,必要时加用降压药。
- 蛋白尿:定期进行尿常规检查。日常饮食注意优质蛋白摄入,避免增加肾脏负担。
结语:MedFind 为您的生命寻找更多可能
这项来自南洋理工大学的研究为我们揭示了未来癌症治疗的新趋势:不再依赖单一的打击,而是通过多机制的协同作战。通过诱导铜死亡、钙过载和抗血管生成,我们能够以极低的副作用,换取更强的抗癌效果。
目前,呋喹替尼等靶向药物在国内已进入医保,极大减轻了患者负担。然而,对于某些尚未在国内获批的罕见靶点药物或最前沿的联合方案,信息差往往成了救命的障碍。MedFind 作为专业的抗癌信息共享平台,提供全球抗癌药品跨境直邮服务,确保患者能够同步获取全球最新、合法的抗癌药物。同时,我们的AI辅助问诊系统能为您解读复杂的检查报告,助您在治疗决策中更有底气。如果您想了解更多关于铜死亡疗法或相关靶向药的获取途径,请联系 MedFind 专业医学顾问。科学抗癌,我们与您并肩同行。
参考信息
- Liu, Y., et al. (2025). A Multifunctional Calcium Phosphate Nanoplatform Inducing Synergistic Copper/Calcium Overload and Antiangiogenesis for Enhanced Cancer Therapy. ACS Nano.
- Tsvetkov, P., et al. (2022). Copper induces cell death by targeting lipoylated TCA cycle proteins. Science.