食管癌,这个消化道常见的恶性肿瘤,在中国患者群体中尤为严峻。每年,我国都有近一半的食管癌新发和死亡病例,给无数家庭带来沉重负担。面对晚期诊断率高、恶性程度强、治疗难度大的挑战,传统的治疗方式已难以满足患者对长期生存的渴望。然而,医学的飞速发展为食管癌患者带来了曙光——以分子检测为核心的精准治疗,正逐步改变着食管癌的治疗格局,为患者开启了新的生存希望。
在精准医学时代,深入了解肿瘤的分子特征是制定个性化治疗方案的关键。通过基因检测,医生能够识别肿瘤细胞的“弱点”,从而选择更具针对性的靶向药物或免疫疗法,最大限度地提高疗效,降低副作用。本文将作为一份全面的科普指南,旨在帮助食管癌患者及其家属通俗易懂地了解NCCN等国内外权威指南推荐的分子检测项目,以及当前和未来可能改变治疗前景的免疫治疗和新型抗体偶联药物(ADC)的最新进展。无论您是初次诊断、正在治疗中,还是希望了解更多前沿信息,本文都将为您提供宝贵且实用的参考。MedFind致力于为癌症患者提供最新的抗癌资讯和药物信息,协助患者构建跨境购药渠道,我们希望这些信息能帮助您更好地了解食管癌的精准治疗路径,坚定抗癌信心。
食管癌在中国:严峻形势与精准治疗的崛起
食管癌,在我国是发病率和死亡率均居前列的恶性肿瘤。根据国家癌症中心的最新数据,2022年我国食管癌新发病例数超过22万例,死亡病例数近19万例,均位居世界首位。其早期识别率低、恶性程度高、且多发于老年群体,使得许多患者确诊时已是中晚期。
食管癌的分期对其预后有着决定性影响:I期患者的5年生存率可达90%,而III期、IV期患者则骤降至33%和26%。这种显著的差异,凸显了开发高效新型治疗方案以改善中晚期患者生存状况的迫切性。近年来,随着肿瘤分子生物学研究的深入,靶向治疗和免疫治疗等新型疗法在食管癌领域取得了突破性进展,将食管癌治疗带入了精准医学时代。而分子检测,正是开启精准治疗大门的“金钥匙”。
NCCN指南推荐:食管癌精准治疗的分子检测全景
面对日益丰富的靶向和免疫治疗药物,如何准确筛选出可能受益的患者,成为了临床治疗中的关键。NCCN指南作为国际权威的肿瘤临床实践指南,为食管癌患者的分子检测提供了明确的指导。它推荐了一系列生物标志物,这些标志物能够预测特定药物的疗效。
1. 靶向治疗相关分子靶点
靶向治疗药物通过识别并攻击癌细胞特有的分子靶点来发挥作用,因此,检测这些靶点的状态至关重要:
- HER2过表达/扩增:HER2(人表皮生长因子受体2)是一种在某些癌细胞表面过量表达的蛋白质,它会促进癌细胞的生长和分裂。对于HER2过表达或基因扩增的食管癌患者,佐妥昔单抗(Zolbetuximab)和德曲妥珠单抗(Trastuzumab deruxtecan)等靶向药物可能带来显著疗效。
- BRAF V600突变:BRAF基因的V600突变在多种癌症中可见,它导致细胞信号通路异常活跃,驱动肿瘤生长。针对这一突变的靶向药物已被开发,食管癌患者若检测到此突变,也可能受益。
- CLDN18.2表达:CLDN18.2(密蛋白18.2)是胃肠道上皮细胞上的一个特异性蛋白,在癌变后可能大量表达。针对CLDN18.2的靶向药物,如佐妥昔单抗,已在临床上展现出治疗食管腺癌的潜力。
- NTRK1/2/3融合及RET融合:NTRK(神经营养性酪氨酸受体激酶)和RET(重排转染)是两种不同的基因,当它们发生融合突变时,会产生异常的融合蛋白,驱动癌细胞生长。针对这些“广谱”融合基因的靶向药物,在多种携带此类突变的肿瘤中都显示出良好疗效,食管癌也不例外。


2. 免疫治疗相关生物标志物
免疫治疗通过激活患者自身的免疫系统来攻击癌细胞,而特定的生物标志物可以帮助预测患者对免疫治疗的反应:
- MMR/MSI(错配修复缺陷/微卫星不稳定性):MMR(DNA错配修复)基因功能缺失会导致MSI-H(高微卫星不稳定性),使得癌细胞内累积大量基因突变,被免疫系统识别的可能性大大增加。因此,MMR缺陷或MSI-H的食管癌患者通常对免疫检查点抑制剂表现出更好的响应。
- PD-L1表达:PD-L1(程序性死亡配体1)是癌细胞表面的一种蛋白质,它能与免疫细胞上的PD-1受体结合,从而抑制免疫细胞的活性。当PD-L1在肿瘤细胞或免疫细胞上高表达时,使用靶向PD-1/PD-L1通路的免疫治疗药物(如度伐利尤单抗、纳武利尤单抗、帕博利珠单抗等)能够阻断这一“免疫刹车”,重新激活免疫系统攻击癌细胞。
- TMB(肿瘤突变负荷):TMB是指肿瘤细胞基因组中体细胞突变的总数。高TMB的肿瘤通常产生更多的新抗原,这些新抗原更容易被免疫系统识别,因此高TMB的患者也可能从免疫治疗中获益。
3. 检测样本的选择:组织VS液体活检
分子检测通常首选肿瘤组织标本,因为它能提供最直接的肿瘤细胞信息。然而,对于某些患者,获取肿瘤组织可能存在困难(如转移性、晚期食管癌患者无法耐受传统活检),或组织标本不足。在这种情况下,NCCN指南建议可以检测食管癌释放入血的ctDNA(循环肿瘤DNA)。
ctDNA检测是一种“液体活检”技术,只需抽取患者外周血即可。它通过分析血液中肿瘤来源的DNA片段,检测其中的基因突变、融合等情况,不仅能筛选出可靶向的基因变异类型,还能动态监测肿瘤克隆的进化和治疗应答。这种微创、便捷的检测方式,为无法获取组织标本或需要实时监测的患者提供了重要的选择。

围手术期治疗新篇章:免疫治疗为食管癌患者带来更多生存机会
食管癌的传统治疗以手术、放化疗为主。然而,由于许多患者确诊时病情已进展,且食管癌早期易发生淋巴结转移,单纯手术预后往往不尽如人意。因此,现代食管癌治疗模式已逐渐转向以手术为核心的综合治疗,即在手术前后联合其他治疗手段,以期根治肿瘤,降低复发风险。
目前,FLOT方案(氟尿嘧啶、亚叶酸钙、奥沙利铂及多西他赛)是可切除食管癌围手术期的标准治疗方案。尽管如此,仍有相当一部分患者在术后出现复发转移。近年来,免疫治疗的加入,为围手术期食管癌患者带来了革命性的突破,开启了新的治疗方向。
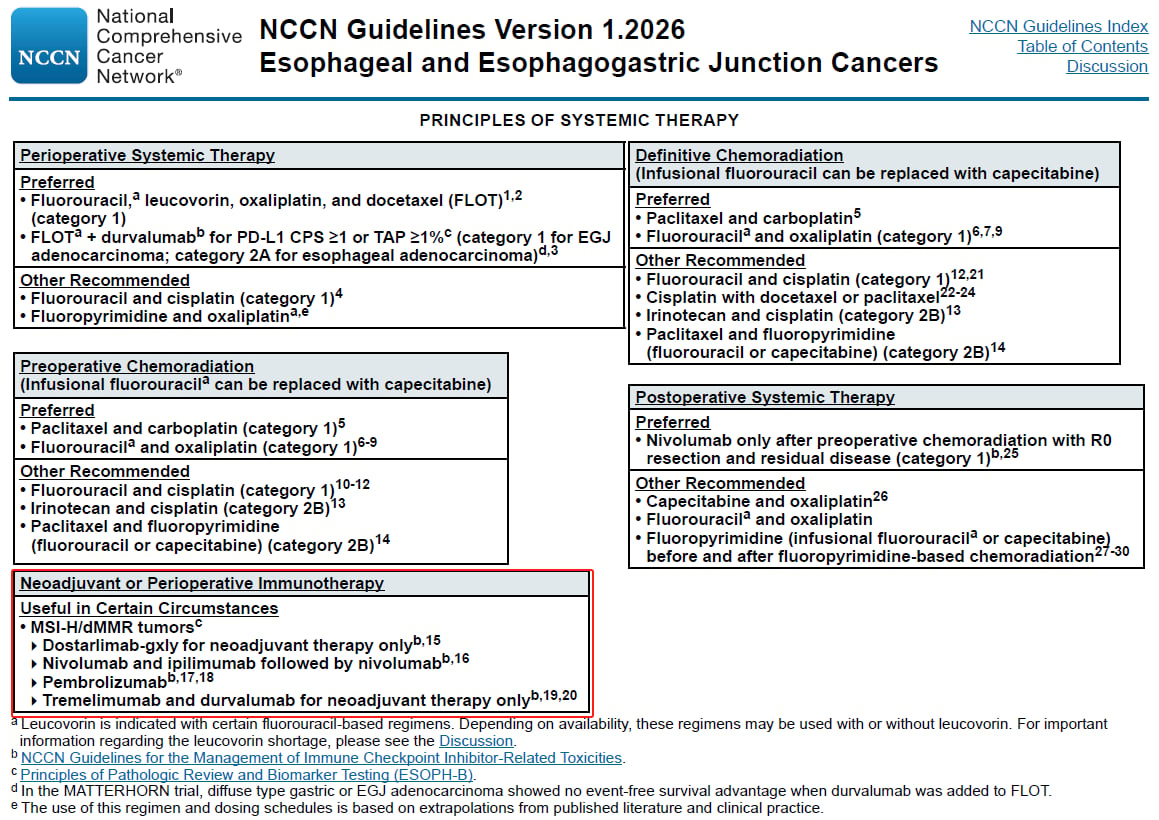
1. 度伐利尤单抗联合FLOT方案:NCCN指南的1类推荐
MATTERHORN研究是一项里程碑式的临床试验,其结果表明,对于可切除的胃或胃食管结合部(EGJ)腺癌患者,围手术期使用免疫检查点抑制剂度伐利尤单抗联合FLOT方案,能够显著延长患者的无事件生存期(EFS),优于单纯FLOT方案。基于此,NCCN指南明确推荐:对于PD-L1 CPS≥1或TAP≥1%的患者,围手术期系统治疗可首选度伐利尤单抗+FLOT方案。其中,对于胃食管结合部腺癌,这已成为1类推荐(最高级别推荐),而食管腺癌则为2A类推荐,显示了其在临床实践中的重要地位。


2. MSI-H或dMMR患者:免疫治疗的黄金机会
NCCN指南还强调,所有新诊断的食管癌患者都应通过PCR或NGS技术检测MSI,或通过IHC平台检测MMR。如果可切除食管癌患者被检出为MSI-H(高微卫星不稳定性)或dMMR(错配修复缺陷),则其对免疫治疗的响应率通常较高,应积极考虑免疫治疗。
对于这类患者,新辅助或围手术期可选择的免疫治疗方案包括:
- 纳武利尤单抗联合伊匹木单抗新辅助治疗后序贯纳武利尤单抗维持治疗。
- 帕博利珠单抗单药治疗。
- 曲美木单抗和度伐利尤单抗联合治疗(目前主要适用于新辅助治疗)。
- 新增的多塔利单抗治疗方案也为新辅助治疗提供了更多选择。
这些方案的加入,极大地丰富了MSI-H/dMMR食管癌患者的治疗选择,为他们带来了更精准、更有效的抗肿瘤策略。


PD-L1蛋白表达检测:样本选择与异质性的考量
PD-L1表达是指导免疫治疗选择的重要生物标志物,但其检测过程中的样本选择和结果解读需要特别注意,以确保检测结果的准确性和临床指导意义。
1. 优选肿瘤组织标本及其处理
在PD-L1蛋白表达检测中,优先推荐采用经4%甲醛充分固定、石蜡包埋处理的肿瘤组织标本。这种标准的病理处理方式能较好地保留蛋白抗原性,从而保障检测结果的准确性。如果存在多个肿瘤组织蜡块,病理医生会结合病理形态学特征,选择最具代表性的蜡块进行检测,以确保样本能真实反映肿瘤的PD-L1表达情况。
同时,必须严格规避以下不合格蜡块:
- 含大面积坏死组织:坏死组织中的蛋白降解,可能导致检测结果失真。
- 细胞挤压严重:细胞结构受损可能影响抗原的完整性。
- 固定不及时或固定液浓度异常:不当的固定条件可能导致抗原丢失或假阴性结果。
这些不合格标本易导致抗原丢失或假阴性结果,从而误导治疗决策。
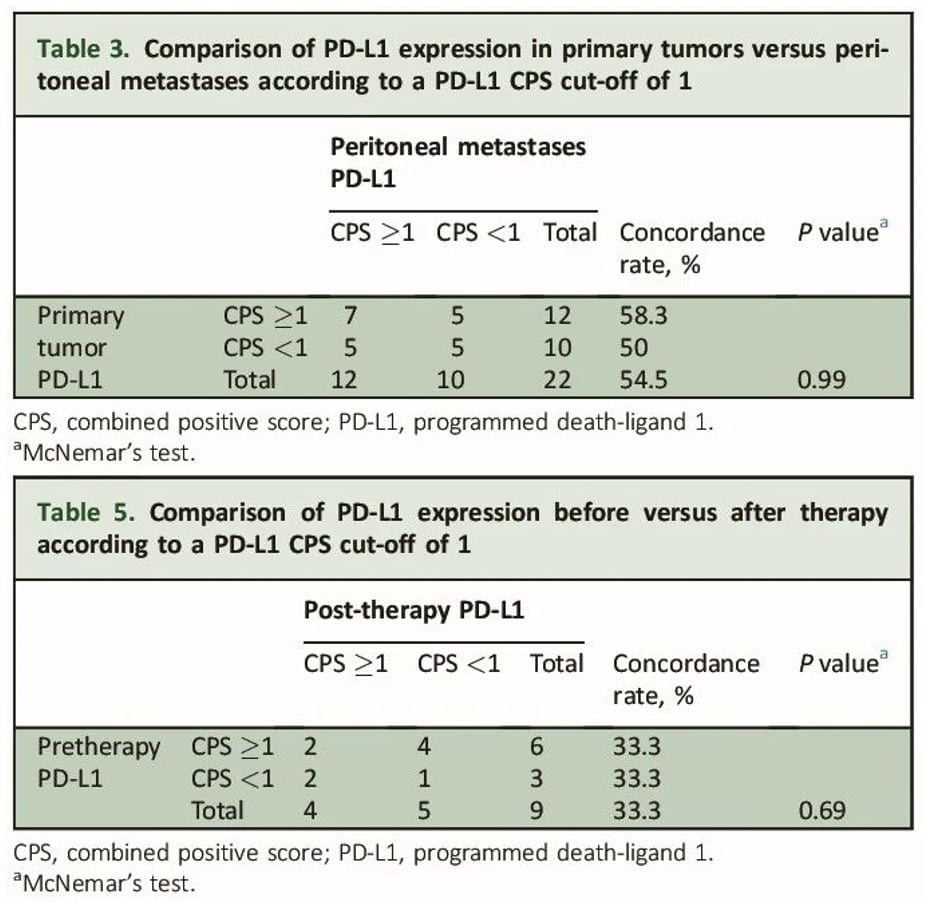


2. 原发灶与转移灶的异质性
肿瘤是一个高度异质性的疾病,这意味着在同一个患者体内,原发灶和不同部位的转移灶之间,甚至肿瘤内部不同区域之间,都可能存在分子特征的差异。PD-L1表达也不例外。已有研究针对转移性胃食管腺癌进行分析,发现PD-L1表达存在显著的“空间异质性”(即原发灶与转移灶之间可能不同),并且可能随着治疗周期呈现“时间异质性”(即治疗前后表达可能变化)。
这种异质性对治疗方案的制定具有重要参考价值。因此,《中国食管癌PD-L1蛋白表达检测临床病理专家共识》明确建议,在临床标本可及的前提下,应同时对原发灶和转移灶进行PD-L1检测。这样做能够为免疫治疗方案的精准制定提供更全面、更可靠的依据,避免因局部样本的局限性而错过有效的治疗机会。

靶向ADC药物:晚期食管癌治疗的突破性方向
近年来,抗体偶联药物(ADC)凭借其独特的“智能导弹”作用机制,在食管癌治疗领域取得了突破性进展,成为晚期患者的重要治疗选择。ADC药物结合了抗体的靶向特异性和化疗药物的高效杀伤力:一个抗体(导弹的导航系统)能精准识别癌细胞表面的特定靶点,然后通过一个连接子(导弹的连接部分)将一个强效的化疗药物(炸药)精准递送至癌细胞内部,从而在杀伤癌细胞的同时,最大限度地减少对正常组织的损伤,降低全身性毒副作用。
1. 晚期食管腺癌的ADC治疗进展
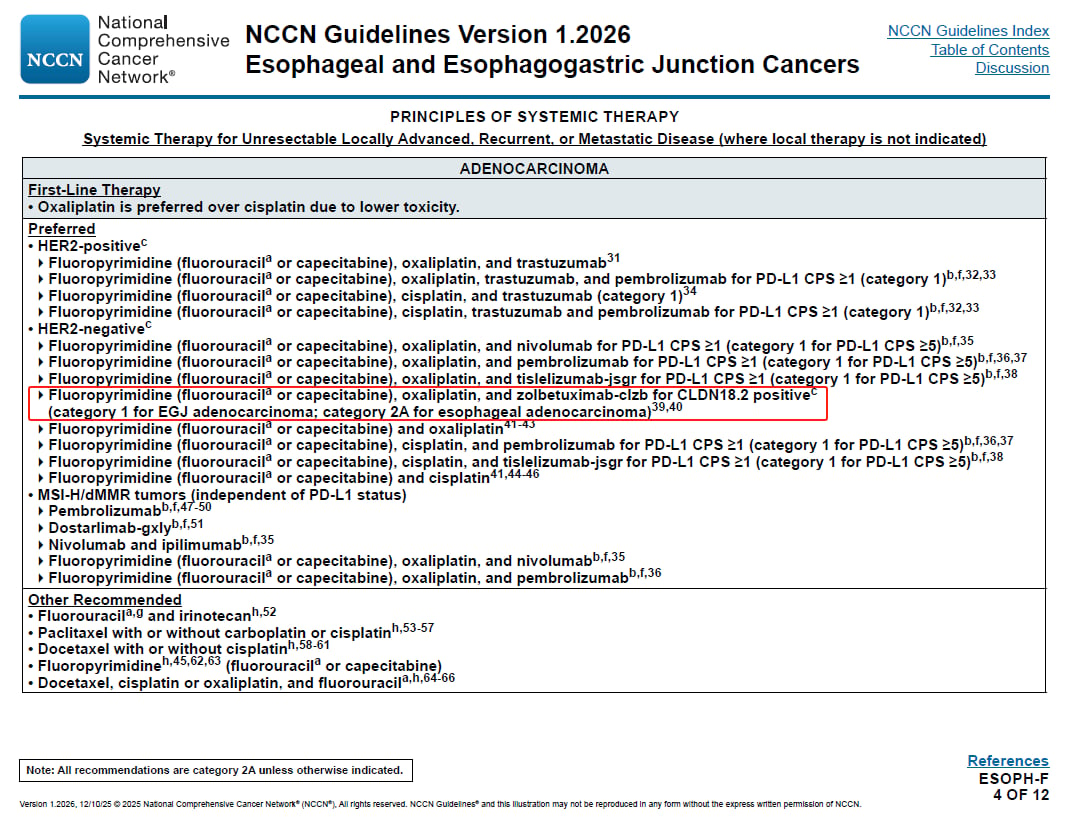
NCCN指南已将多款靶向ADC药物纳入晚期食管腺癌的系统治疗推荐方案:
- 一线治疗:对于HER2阴性、CLDN18.2阳性的患者,推荐使用氟尿嘧啶类药物(氟尿嘧啶或卡培他滨)联合奥沙利铂与佐妥昔单抗。这为这类特定分子特征的患者提供了精准的一线选择。
- 二线及后线治疗:对于HER2阳性的患者,德曲妥珠单抗已成为首选药物之一。这款高效ADC药物通过靶向HER2,为多次治疗失败的HER2阳性食管腺癌患者带来了显著的生存改善。
这些ADC药物的获批和推荐,为不同亚型的食管腺癌患者提供了更精准、更有效的治疗策略。


2. 食管鳞癌的新兴ADC靶点与突破
尽管NCCN指南尚未在食管鳞癌中推荐上述特定ADC治疗方案,但其他靶向ADC药物已在该类患者中展现出巨大潜力。
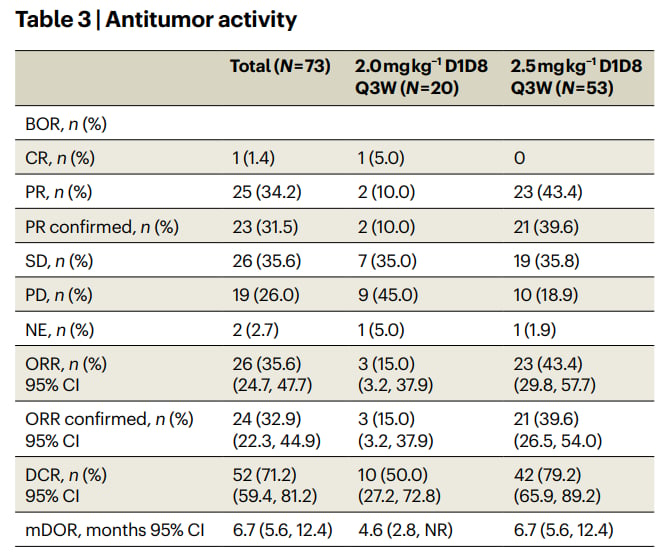
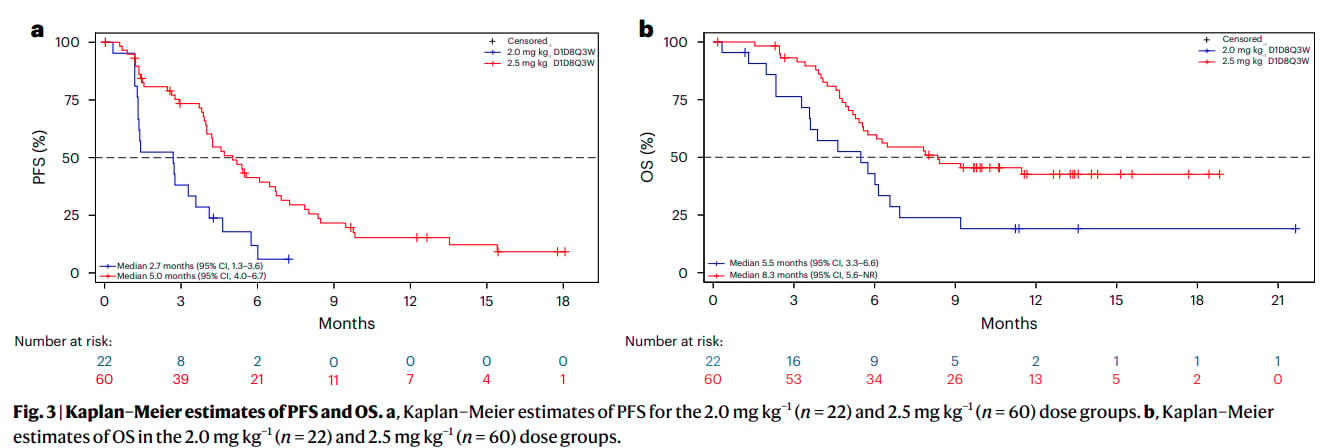
- 靶向EGFR/HER3的ADC药物BL-B01D1:EGFR(表皮生长因子受体)编码的受体属于ErbB家族,其扩增在约16%的食管鳞癌患者中可见,并与EGFR过表达显著相关,是潜在的靶向位点。近期《Nature Medicine》期刊发表的一项Ib期临床试验,评估了靶向EGFR/HER3的ADC药物BL-B01D1在既往治疗进展的转移性食管鳞癌患者中的安全性和有效性。结果令人鼓舞:在2.5 mg/kg剂量组,确认客观缓解率(cORR)高达39.6%,疾病控制率(DCR)为79.2%,中位总生存期(OS)达到11.5个月。这一疗效显著优于现有的二线治疗方案,为免疫耐药的食管鳞癌患者提供了全新的治疗思路和策略。BL-B01D1已被纳入优先审评,其III期随机对照试验正在积极开展,旨在进一步验证其疗效,并探索EGFR/HER3突变、下游信号通路状态等生物标志物,以优化适用人群的筛选。
- 靶向Trop2和Nectin-4的ADC药物:除了EGFR/HER3,靶向Trop2和Nectin-4表达的ADC药物也在食管鳞癌治疗中展现出良好的抗肿瘤潜力。这些新兴靶点为该亚型肿瘤的治疗拓展了新方向,值得开展更多临床研究深入探索。



食管癌遗传风险评估:易感基因检测的意义
虽然大多数食管癌是散发性的,但遗传因素在高危人群筛查与干预中扮演着重要角色。了解家族遗传风险,可以帮助患者和其亲属进行更早期的筛查和预防性干预。
1. 哪些患者需要进行胚系突变检测?
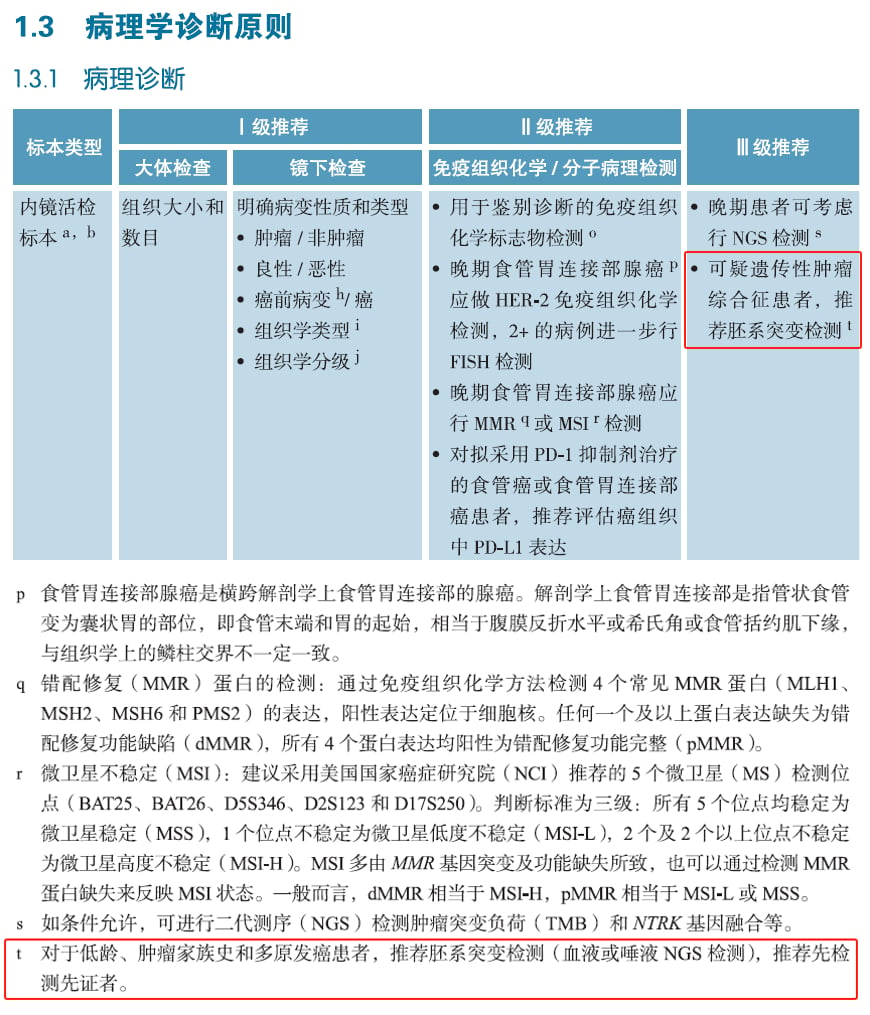
CSCO(中国临床肿瘤学会)指南明确指出,对于以下食管癌患者,推荐进行胚系突变检测:
- 发病年龄偏低:相对于一般人群,如果患者在较年轻时被诊断出食管癌,可能提示存在遗传因素。
- 有肿瘤家族史:家族中有多位成员患有癌症,特别是食管癌或其他相关癌症,应高度警惕。
- 合并多原发癌:如果患者同时或先后被诊断出两种或多种原发性癌症,也可能与遗传易感性相关。
检测通常采用血液或唾液样本进行NGS(二代测序)检测。为提高效率和准确性,优先建议对家族中的先证者(即家族中最早或最典型患病的成员)进行检测,以便发现致病性基因突变,为整个家族的遗传风险评估提供依据。
2. NCCN指南列出的食管癌相关遗传易感综合征
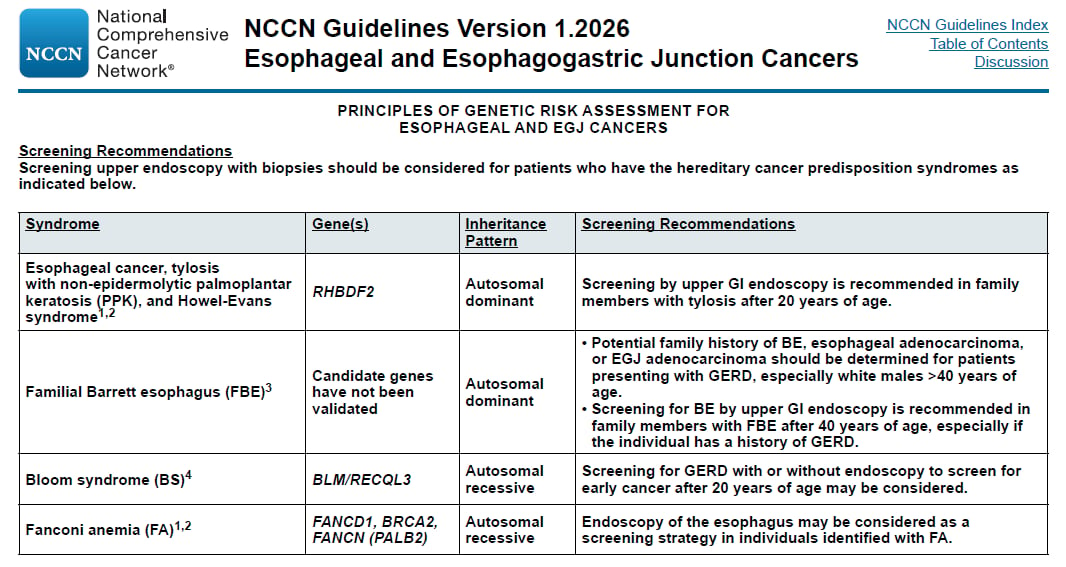
NCCN指南进一步详细罗列了与食管癌发病风险增加相关的遗传性癌症易感综合征及其对应的致病基因,这为临床精准识别遗传易感人群、制定个体化筛查策略提供了明确参考:
- RHBDF2基因突变:可引发食管癌,并伴有胼胝症伴非表皮松解性掌跖角化症(PPK),也被称为豪威尔-埃文斯综合征。
- BLM/RECQL3基因突变:导致布卢姆综合征,该综合征患者罹患多种癌症的风险增加,包括食管癌。
- FANCD1、BRCA2、FANCN(PALB2)等基因突变:这些基因突变可能导致范可尼贫血,该综合征同样与多种恶性肿瘤的风险升高有关,包括食管癌。
对这些易感基因的检测,不仅能帮助明确患者的患病风险,还能指导其家族成员进行遗传咨询和风险评估,从而实现早期筛查、早期干预甚至预防。
结语:食管癌精准治疗的未来展望
食管癌的治疗正在经历一场深刻的变革,从传统的“一刀切”模式,逐渐走向以分子检测为导向的“精准定制”。NCCN等权威指南的不断更新,以及免疫治疗和ADC药物的突破性进展,为食管癌患者带来了前所未有的生存希望。分子检测不再仅仅是辅助诊断手段,更是指导治疗选择、预测疗效、评估遗传风险的关键工具。
作为患者和家属,了解这些前沿信息,积极与医生沟通,进行必要的分子检测,选择最适合自己的精准治疗方案至关重要。未来,随着更多新靶点和新药物的发现,食管癌的治疗将更加个性化、高效化。我们坚信,在精准医学的引领下,食管癌不再是无法战胜的难题,越来越多的患者将获得更长的生存期和更好的生活质量。
如果您或您的家人正面临食管癌的挑战,并希望了解更多关于最新治疗方案、跨境购药渠道或寻求AI辅助问诊,请访问MedFind平台,我们将竭诚为您提供帮助,与您携手抗癌。





