激素受体阳性(HR+)/人表皮生长因子受体2阴性(HER2-)晚期乳腺癌(ABC)是临床上常见的乳腺癌亚型。近年来,细胞周期蛋白依赖性激酶4和6(CDK4/6)抑制剂联合内分泌治疗已成为这类患者的一线标准疗法。包括帕博西尼(Palbociclib)在内的CDK4/6抑制剂,与内分泌治疗联用,已在多项关键临床试验中证实能显著改善患者的无进展生存期(PFS)和客观缓解率(ORR)。然而,尽管疗效显著,大多数患者最终仍会面临疾病进展。对于在一线CDK4/6抑制剂治疗后出现进展的患者,后续治疗方案的选择尚无明确共识。重新使用相同的CDK4/6抑制剂联合二线内分泌治疗是否有效,一直是临床关注的焦点。PALMIRA试验正是一项旨在评估帕博西尼作为再挑战策略,联合二线内分泌治疗,在先前接受帕博西尼一线治疗后进展的HR+/HER2-晚期乳腺癌患者中的抗肿瘤活性。

研究方法概览
PALMIRA是一项国际多中心、随机、开放标签的II期临床研究。研究纳入了在一线帕博西尼联合内分泌治疗后影像学确认疾病进展,且先前治疗有临床获益(客观缓解或疾病稳定≥24周),或在辅助治疗阶段接受帕博西尼方案后复发并符合特定条件的HR+/HER2-晚期乳腺癌患者。患者被随机分配至两组:一组接受帕博西尼重新挑战联合二线内分泌治疗,另一组仅接受二线内分泌治疗。帕博西尼的剂量与患者先前完成一线治疗时的剂量相同(125mg、100mg或75mg),联合氟维司群或来曲唑等二线内分泌药物。主要研究终点是研究者评估的无进展生存期(PFS),次要终点包括客观缓解率(ORR)、总生存期(OS)和安全性等。
关键研究结果
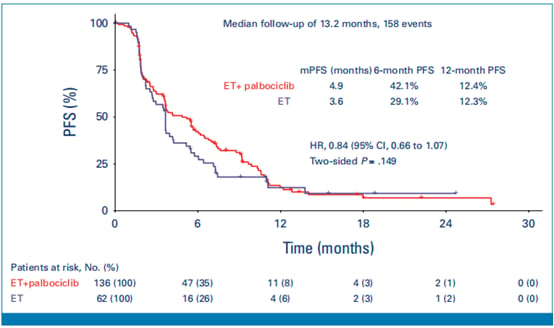
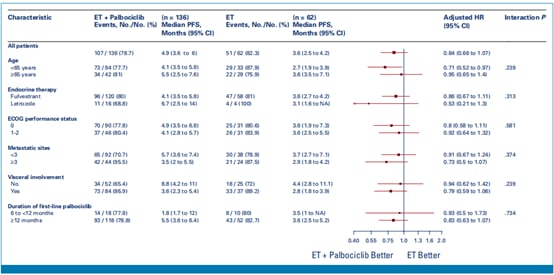
根据主要疗效分析的数据,帕博西尼重新挑战联合内分泌治疗组的中位PFS为4.9个月(95% CI, 3.6 – 6.1),而单纯内分泌治疗组为3.6个月(95% CI, 2.5 – 4.2)。两组间的风险比(HR)为0.84(95% CI, 0.66 – 1.07),统计学差异不显著(P = 0.149)。这意味着在PALMIRA试验中,帕博西尼作为再挑战策略未能显著延长患者的无进展生存期。总生存期(OS)数据在本次分析时尚未成熟,两组的中位OS数据接近,差异不显著。尽管主要终点未达到,但研究观察到帕博西尼联合内分泌治疗组的临床获益率(CBR)为41.9%,高于单纯内分泌治疗组的27.4%,这一差异具有统计学意义(P = 0.044)。
安全性分析
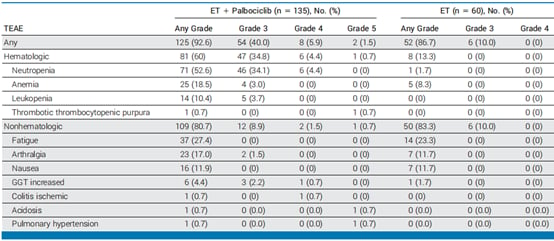
安全性方面,帕博西尼联合内分泌治疗组的治疗相关不良事件(TEAEs)发生率高于单纯内分泌治疗组,尤其是≥3级的TEAEs发生率(47.4% vs 10.0%)。帕博西尼组最常见的≥3级血液学不良事件是中性粒细胞减少(38.5%),这与帕博西尼已知的安全性特征一致。其他血液学不良事件如白细胞减少、贫血和血小板减少也有发生。研究中未报告治疗相关的死亡事件。
结论与展望
PALMIRA试验是首个专门评估在HR+/HER2-晚期乳腺癌患者中,一线帕博西尼治疗进展后,重新挑战帕博西尼联合二线内分泌治疗有效性的随机试验。尽管研究未达到显著改善PFS的主要终点,其安全性特征与既往研究一致。这一结果与PACE研究的发现相符,提示在疾病进展后继续使用相同的CDK4/6抑制剂(至少是帕博西尼)可能不是一个普遍有效的策略。然而,值得注意的是,其他一些研究(如MAINTAIN和postMONARCH试验)显示了不同的结果,这可能提示CDK4/6抑制剂之间存在非完全交叉耐药性,或者患者选择至关重要。未来的研究需要进一步探索能够预测哪些患者可能从CDK4/6抑制剂再挑战中获益的临床和分子生物标志物。
对于正在寻求帕博西尼、其他CDK4/6抑制剂或相关靶向药、抗癌药治疗方案的患者及家属,了解最新的临床研究进展至关重要。获取这些药物,尤其是海外上市的创新药或仿制药,有时会面临挑战。通过海外靶向药代购服务,可以帮助患者获取所需的药物。同时,利用AI问诊工具或查阅药物信息与诊疗指南,能够更好地理解病情和治疗选择。
原始出处:Llombart-Cussac, A., et al. (2025). Second-Line Endocrine Therapy With or Without Palbociclib Rechallenge in Patients With Hormone Receptor-Positive/Human Epidermal Growth Factor Receptor 2-Negative Advanced Breast Cancer: PALMIRA Trial. Journal of Clinical Oncology, DOI: https://doi.org/10.1200/JCO-24-01865.





